Содержание
- 2. «Мало знать, надо применять» Й. Гёте Цель урока: Обучающая: продолжить формирование понятий о количестве вещества и
- 3. В чем измеряется жидкость? V (л) (мл)
- 4. В чем измеряется твердые вещества? m (г) (кг)
- 5. Одна порция В чем измеряется количество вещества? n (моль)
- 6. Постоянная Авогадро Определим число атомов С в 12 г углерода. Для этого разделим 0,012 кг на
- 8. Количество вещества n = N/NA n
- 9. КОЛИЧЕСТВО ВЕЩЕСТВА ДЛЯ ТВЕРДЫХ ВЕЩЕСТВ ДЛЯ ГАЗООБРАЗНЫХ ВЕЩЕСТВ n = m(в-ва)/M(в-ва) Закон Авогадро 1 моль любого
- 10. РЕШЕНИЕ ТИПОВЫХ ЗАДАЧ
- 11. Типовая задача № 1. Сколько молей составляют и сколько молекул содержат 8 г кислорода 02 ?
- 12. Типовая задача № 2 Определите массу 0,25 моль серной кислоты Д а н о: n(H2 S04
- 13. Типовая задача № 3 Какой объём при нормальных условиях занимают 2 моль любого газа? Д а
- 14. Типовая задача № 4 Какой объём при нормальных условиях занимают 7г азота N2 ? Д а
- 16. Скачать презентацию












 Трубчатые печи. Классификация и принцип работы трубчатых печей
Трубчатые печи. Классификация и принцип работы трубчатых печей Современное состояние и тенденции развития мировой ветроэнергетики и ветроэнергетики России
Современное состояние и тенденции развития мировой ветроэнергетики и ветроэнергетики России Современное высшее образование: формирование компетентности специалиста
Современное высшее образование: формирование компетентности специалиста Проводник пассажирского вагона. Этика. Имидж. Служебный этикет. Культура обслуживания. Психология. Конфликтные ситуации
Проводник пассажирского вагона. Этика. Имидж. Служебный этикет. Культура обслуживания. Психология. Конфликтные ситуации Численное дифференцирование и интегрирование функций
Численное дифференцирование и интегрирование функций Форматы и варианты оформления печатных изданий. Полосы набора
Форматы и варианты оформления печатных изданий. Полосы набора Эксплуатация и ремонт быстродецствующего выключателя электровоза ВЛ-10
Эксплуатация и ремонт быстродецствующего выключателя электровоза ВЛ-10 Внутренняя политика Александра I после войны 1812 года. Аракчеевщина
Внутренняя политика Александра I после войны 1812 года. Аракчеевщина Проект Символы Тбилисского района
Проект Символы Тбилисского района Презентация Познакомимся с нашими зубами
Презентация Познакомимся с нашими зубами Невербальные средства общения
Невербальные средства общения АО Сахатранснефтегаз. Отчёт по практике
АО Сахатранснефтегаз. Отчёт по практике Бабушкин юбилей
Бабушкин юбилей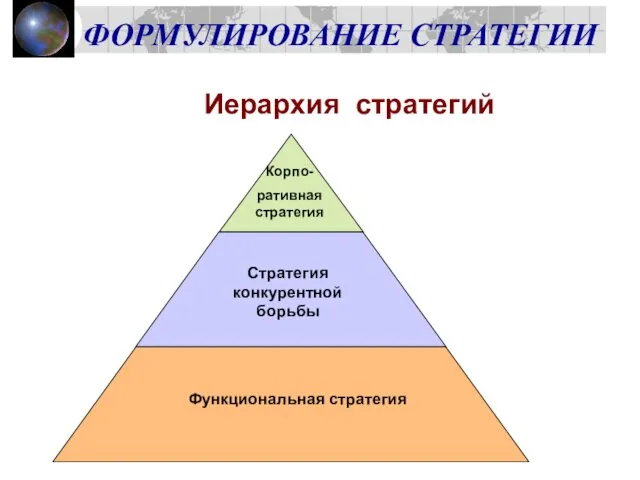 Формулирование стратегии. Иерархия стратегий
Формулирование стратегии. Иерархия стратегий Экономика ведущих стран Западной Европы (ФРГ, Франция, Великобритания, Италия, Испания)
Экономика ведущих стран Западной Европы (ФРГ, Франция, Великобритания, Италия, Испания) Бинарные соединения
Бинарные соединения Мини-викторина Основы агрономии
Мини-викторина Основы агрономии Гипсокартон
Гипсокартон Экономическая основа МСУ
Экономическая основа МСУ Диагностика речевого развития
Диагностика речевого развития Детская агрессия
Детская агрессия Декоративно-прикладное искусство
Декоративно-прикладное искусство Мой прекрасный город. Город мой – Зеленоград. Немного об истории Зеленограда
Мой прекрасный город. Город мой – Зеленоград. Немного об истории Зеленограда Город Старый Оскол
Город Старый Оскол Плоскость, прямая, луч. 5 класс
Плоскость, прямая, луч. 5 класс Установка системы беспроводного учета расхода воды в домах микрорайона Южные ворота
Установка системы беспроводного учета расхода воды в домах микрорайона Южные ворота Первый признак подобия треугольников
Первый признак подобия треугольников Гражданская война в России 1917-1922 гг
Гражданская война в России 1917-1922 гг