В последние годы в мире активно развиваются исследования, направленные на идентификацию
наноструктур в биологических жидкостях с помощью оптических средств.
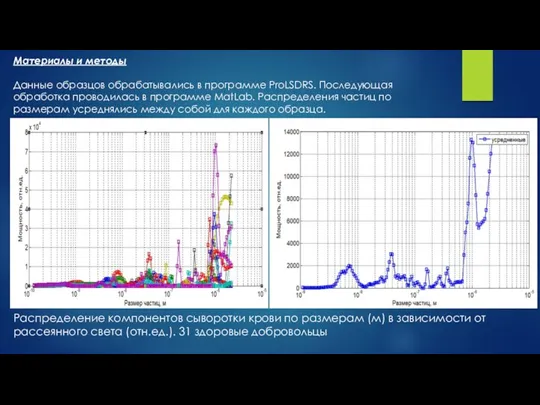
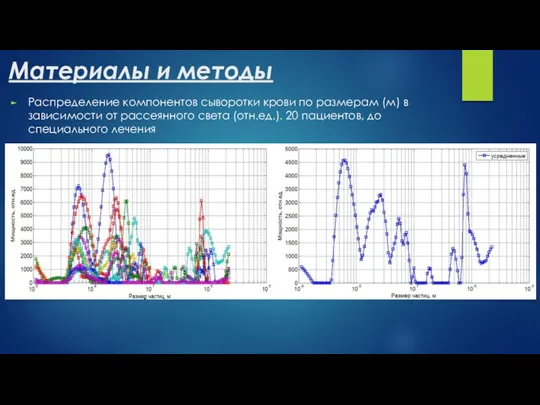
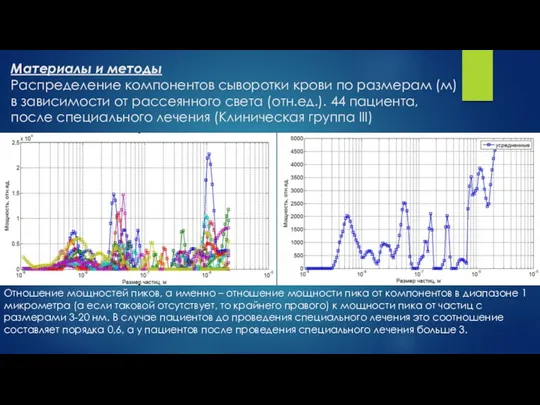
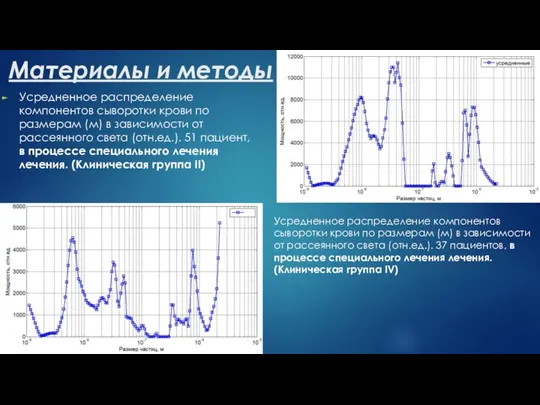
Большинство методов основано на экспериментальной оценке характеристических параметров: частоты максимума (mF), интенсивности (I) и ширины (dF) выделяемого ядра характеристической спектральной функции динамического рассеяния света
Известен метод исследования слабых водных растворов нативной плазмы или нативной сыворотки крови пациентов с добавлением щелочи в один раствор, а в другой – кислоты. (С. Г. Алексеев с соавт. 2005г.)
Разработан метод лазерной нанодиагностики онкоурологических заболеваний в котором в качестве биологической жидкости используют фильтрованную мочу пациентов (В.Г. Меледин и соавт., 2014).
Количественный, субфракционный состав и характер межмолекулярного взаимодействия биологических жидкостей, которые определяют молекулярную динамику в тестируемом растворе, находятся в сильной корреляционной зависимости от системы гомеостаза, функциональное состояние которой непосредственно связано с физиологическим состоянием основных биосистем жизнеобеспечения. Следовательно, наличие патологических процессов в организме сопровождается изменениями указанных выше физических параметров биологических жидкостей, которые влекут за собой соответствующие изменения структуры молекулярной динамики в тестируемых растворах.











 Презентация Организация театрализованной деятельности в детском саду
Презентация Организация театрализованной деятельности в детском саду Скажи здоровью Да!
Скажи здоровью Да! Городской семинар Организация и функционирование психолого-медико-педагогического консилиумами образовательной организации. Включение детей с ОВЗ в образовательное пространство
Городской семинар Организация и функционирование психолого-медико-педагогического консилиумами образовательной организации. Включение детей с ОВЗ в образовательное пространство Мировой океан и его части
Мировой океан и его части PREZENTATsIYa_ZUEVA-2
PREZENTATsIYa_ZUEVA-2 Организация просветительской работы по профилактике безопасности несовершеннолетних
Организация просветительской работы по профилактике безопасности несовершеннолетних PHP. Реферат по информатике
PHP. Реферат по информатике Как построить бизнес в Интернете
Как построить бизнес в Интернете Бактерии. Место бактерий в системе органического мира
Бактерии. Место бактерий в системе органического мира Дошкольное образование в Великобритании.
Дошкольное образование в Великобритании. Энергоснабжение. Договор энергоснабжения
Энергоснабжение. Договор энергоснабжения Проблемы мобильного гейминга и возможные пути их решения
Проблемы мобильного гейминга и возможные пути их решения Я, ты, Интернет-проблем нет!
Я, ты, Интернет-проблем нет! Строительная компания АРТ Строй
Строительная компания АРТ Строй Поставщик отказался от исполнения/заключения контракта
Поставщик отказался от исполнения/заключения контракта Надкласс рыбы
Надкласс рыбы Мой любимый певец, Lil Peep
Мой любимый певец, Lil Peep Құрақты шитті мақтаны тазалау
Құрақты шитті мақтаны тазалау Нарушение опорно-двигательного аппарата
Нарушение опорно-двигательного аппарата Air Cargo Overview
Air Cargo Overview День качества
День качества Мировой океан
Мировой океан Дослідження габітусу і шкіри тварин
Дослідження габітусу і шкіри тварин Магистры Тема 2
Магистры Тема 2 Магия в первобытной культуре. Виды, приемы, механизмы
Магия в первобытной культуре. Виды, приемы, механизмы Что такое почва
Что такое почва Организация работы прививочного кабинета
Организация работы прививочного кабинета Презентация АЧИИ
Презентация АЧИИ