Содержание
- 2. Ключевые слова CD – антигенные маркеры клеток иммунной системы МНС- главный комплекс гистосовместимости Адгезия - прикрепление
- 3. Факторы врожденного иммунитета Наследуются Действуют быстро Распознают опасность Память отсутствует Механизмы отличаются от адаптивного иммунитета
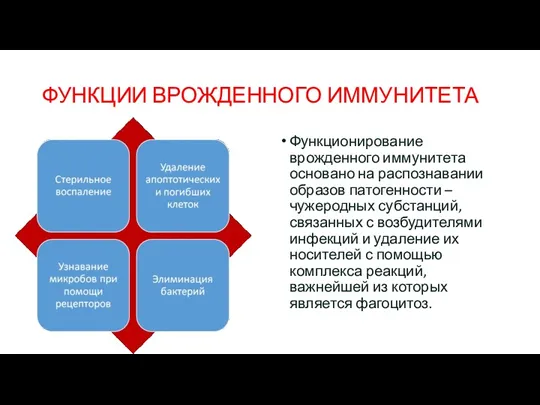
- 4. ФУНКЦИИ ВРОЖДЕННОГО ИММУНИТЕТА Функционирование врожденного иммунитета основано на распознавании образов патогенности – чужеродных субстанций, связанных с
- 5. Особенности врожденного иммунитета распознавание и элиминация патогенов в первые минуты или часы после их проникновения в
- 6. При попадании в организм чужеродного агента ему противостоят сразу все факторы врожденного иммунитета, что порой неадекватно
- 7. Первая линия защиты: Кожа и слизистые ( анатомический барьер - многослойный эпителий); Нормальная микрофлора (колонизационная резистентность);
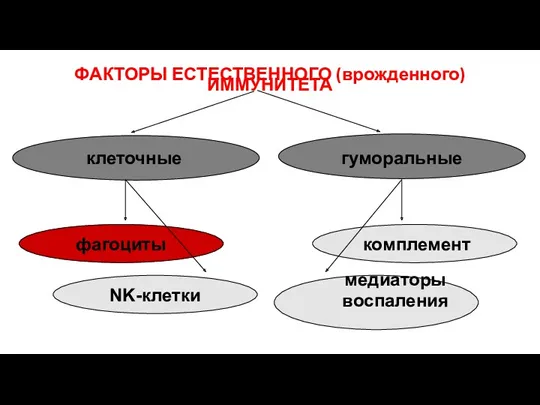
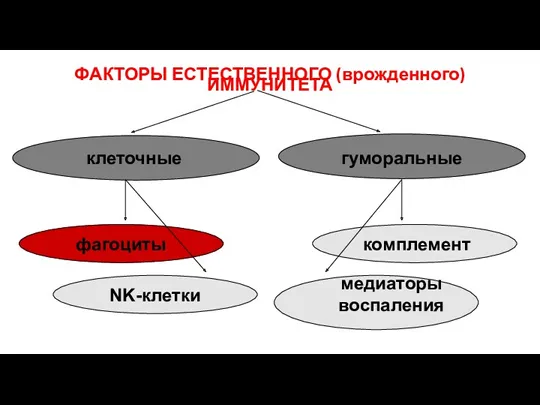
- 8. ФАКТОРЫ ЕСТЕСТВЕННОГО (врожденного) ИММУНИТЕТА клеточные гуморальные фагоциты NK-клетки комплемент медиаторы воспаления
- 9. Распознавание «ВРАГА» в иммунитете КАК ЭТО ПРОИСХОДИТ ?
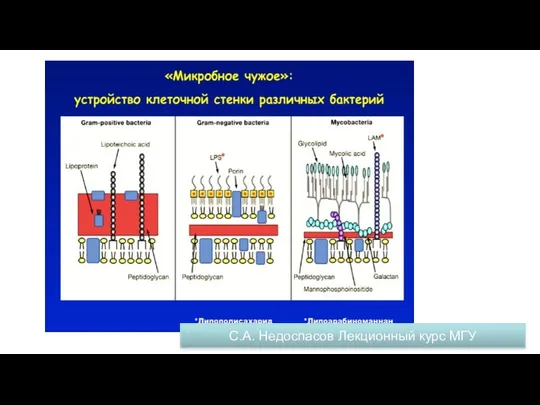
- 10. Принципы иммунологического распознавания 1. «Микробное чужое» (безусловное чужое) Основа врожденного иммунитета. В основе лежит распознавание специальными
- 11. С.А. Недоспасов Лекционный курс МГУ
- 12. Принципы иммунологического распознавания Основа врожденного иммунитета. 2. «Отсутствие своего» (молекулярный пароль) – для «естественных киллеров- NK
- 13. Принципы иммунологического распознавания (характерно для приобритенного/адаптивного имм-та) 3. Распознавание антигена рецепторами В-лимфоцитов или антителами –основа приобретенного
- 14. Принципы иммунологического распознавания (характерно для приобритенного/адаптивного имм-та) 4. «Чужое в контексте своего» - распознавание рецепторами Т
- 15. Врожденный иммунитет распознавание…..
- 16. Принципы иммунологического распознавания 1. «Микробное чужое» (безусловное чужое) - Основа врожденного иммунитета. В основе лежит распознавание
- 17. Образы патогенности PAMP (Pathogen-associated molecular patterns - патоген-ассоциированные молекулярные паттерны) - группы молекул, характерные для патогенов
- 18. РАСПОЗНАВАНИЕ ПАТОГЕНОВ РЕЦЕПТОРАМИ ВРОЖДЕННОГО ИММУНИТЕТА Патогены Патоген-ассоциированные молекулярные структуры или паттерны (РАМРs) Паттерн распознающие рецепторы (PRRs)
- 19. врожденный иммунитет (ВИ) Является первой линией защиты и сенсором одновремненно Обьекты распознавания это РАМР мкробов Из
- 20. МОЛЕКУЛЯРНЫЕ СТРУКТУРЫ ПАТОГЕНОВ И УЗНАЮЩИЕ ИХ РЕЦЕПТОРЫ (примеры) ЛПС – липополисахариды (грамотрицательные бактерии) ЛПБ – ЛПС-связывающий
- 21. Паттернраспознающие рецепторы (PRRs) - консервативные структуры микробов общие для разных патогенов, распознаваемые с помощью паттернраспознающих рецепторов
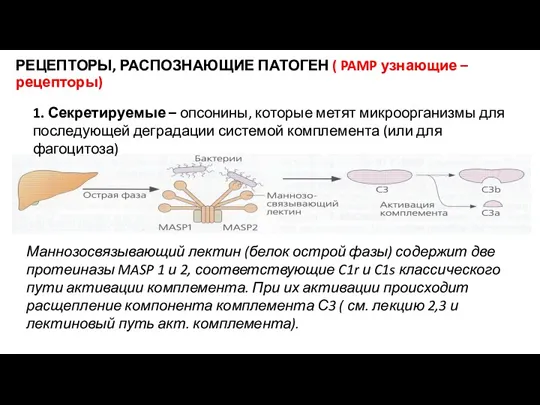
- 22. РЕЦЕПТОРЫ, РАСПОЗНАЮЩИЕ ПАТОГЕН ( PAMP узнающие – рецепторы) 1. Секретируемые – опсонины, которые метят микроорганизмы для
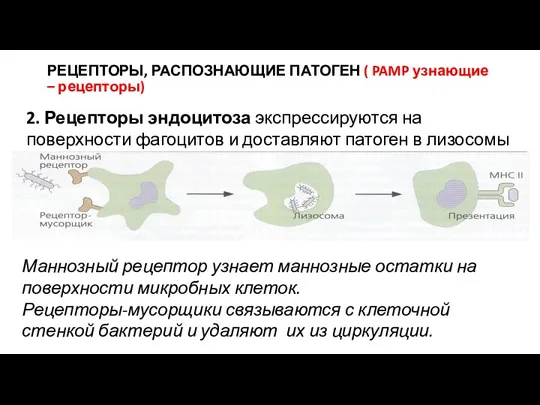
- 23. РЕЦЕПТОРЫ, РАСПОЗНАЮЩИЕ ПАТОГЕН ( PAMP узнающие – рецепторы) 2. Рецепторы эндоцитоза экспрессируются на поверхности фагоцитов и
- 24. Рецепторы врожденного иммунитета, распознающие патоген - ассоциированные структуры микроорганизмов
- 25. Патогенраспознающие рецепторы обладают сродством к образам патогенности (PAMP). Через них в клетку поступают сигналы, включающие «ГЕНЫ
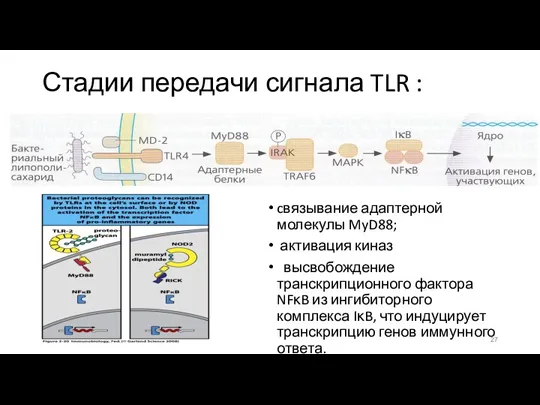
- 26. РЕЦЕПТОРЫ, РАСПОЗНАЮЩИЕ ПАТОГЕН 3. Сигнальные (Toll-подобные рецепторы – TLR) Патогенраспознающие рецепторы обладают сродством к образам патогенности
- 27. Стадии передачи сигнала TLR : cвязывание адаптерной молекулы MyD88; активация киназ высвобождение транскрипционного фактора NFκB из
- 28. ФАКТОРЫ ЕСТЕСТВЕННОГО (врожденного) ИММУНИТЕТА Клеточные факторы
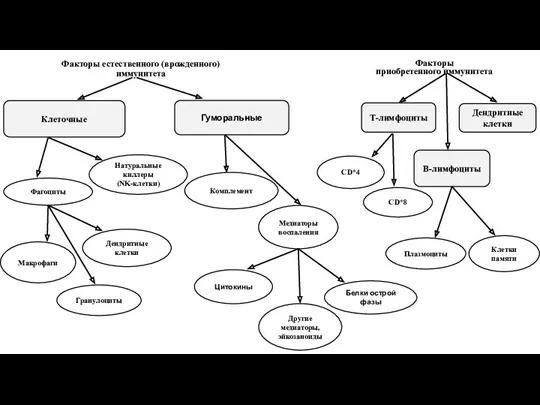
- 29. Факторы естественного (врожденного) иммунитета Цитокины Белки острой фазы Факторы приобретенного иммунитета Т-лимфоциты В-лимфоциты Дендритные клетки Плазмоциты
- 30. ФАКТОРЫ ЕСТЕСТВЕННОГО (врожденного) ИММУНИТЕТА клеточные гуморальные фагоциты NK-клетки комплемент медиаторы воспаления
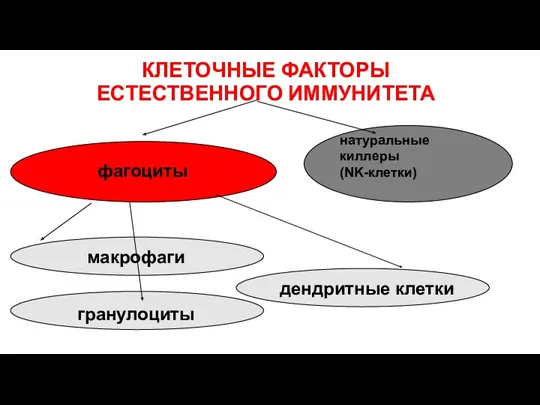
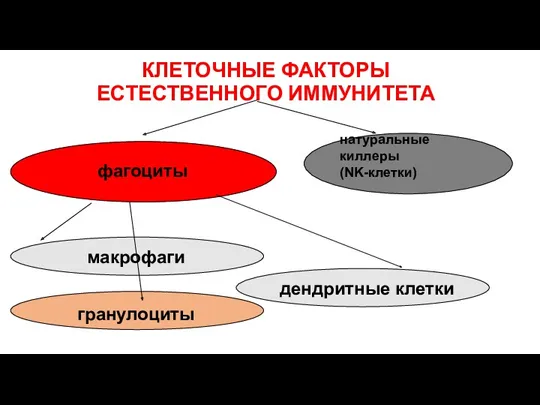
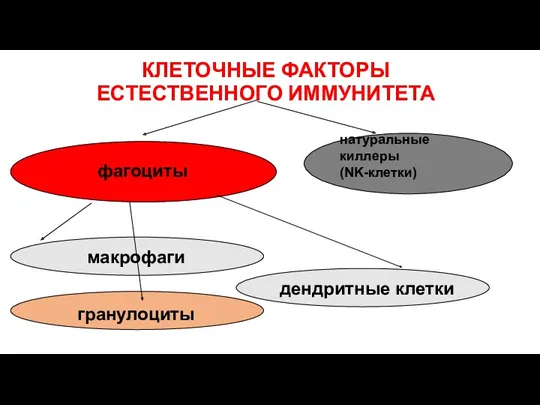
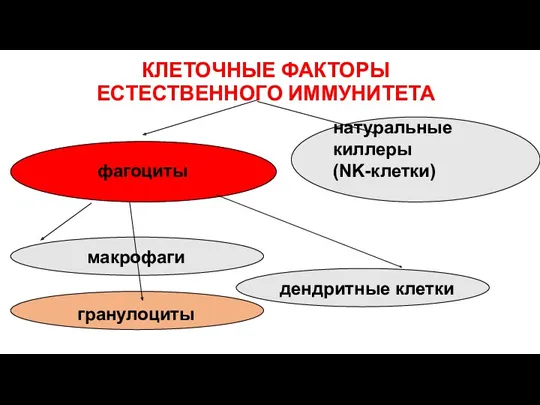
- 31. КЛЕТОЧНЫЕ ФАКТОРЫ ЕСТЕСТВЕННОГО ИММУНИТЕТА натуральные киллеры (NK-клетки) фагоциты макрофаги гранулоциты дендритные клетки
- 32. Из за значительных различий в свойствах Моноцитов(макрофагов), ДК и нейтрофилов роли у них разноплановые и не
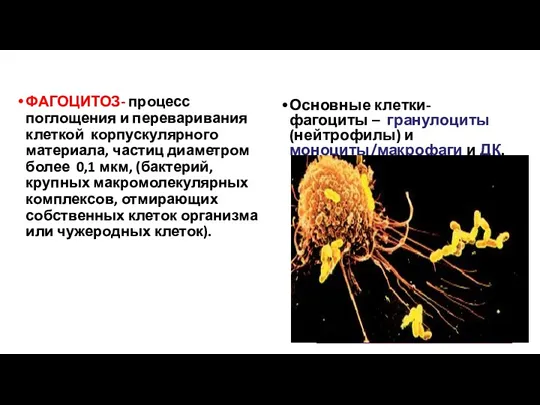
- 33. ФАГОЦИТОЗ- процесс поглощения и переваривания клеткой корпускулярного материала, частиц диаметром более 0,1 мкм, (бактерий, крупных макромолекулярных
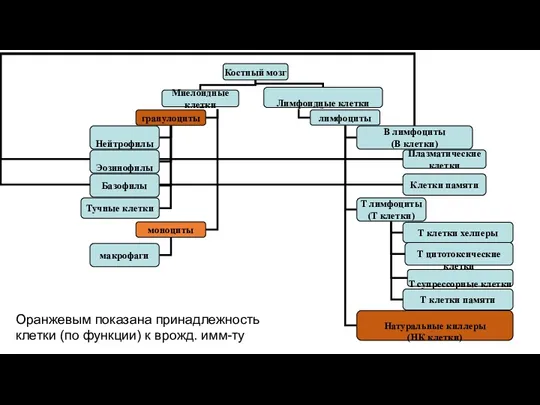
- 34. Оранжевым показана принадлежность клетки (по функции) к врожд. имм-ту
- 35. МОНОЦИТЫ и МАКРОФАГИ
- 36. ХАРАКТЕРИСТИКА МОН/МФ компактное ядро округлой формы размеры - 10-18 мкм содержат ряд ферментов (кислая гидролаза, пероксидаза,
- 37. Моноциты/МАКРОФАГИ виды и фенотип CD14+ рецептор для ЛПС/ЛПБелков что облегчает взаимодействие с TLR CD16+ низкоаффинный рецептор
- 38. ТКАНЕВЫЕ МАКРОФАГИ Печень: Купферовские клетки (мф синусов) Легкие: альвеолярные макрофаги (подвижные) Селезенка: макрофаги селезенки (свободные, подвижные
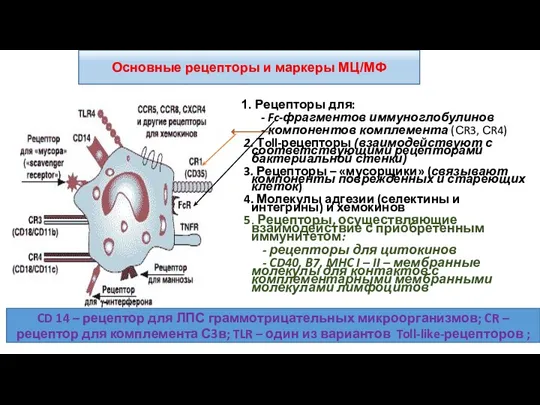
- 39. 1. Рецепторы для: - Fc-фрагментов иммуноглобулинов - компонентов комплемента (СR3, СR4) 2. Тoll-рецепторы (взаимодействуют с соответствующими
- 40. КЛЕТОЧНЫЕ ФАКТОРЫ ЕСТЕСТВЕННОГО ИММУНИТЕТА натуральные киллеры (NK-клетки) фагоциты макрофаги гранулоциты дендритные клетки
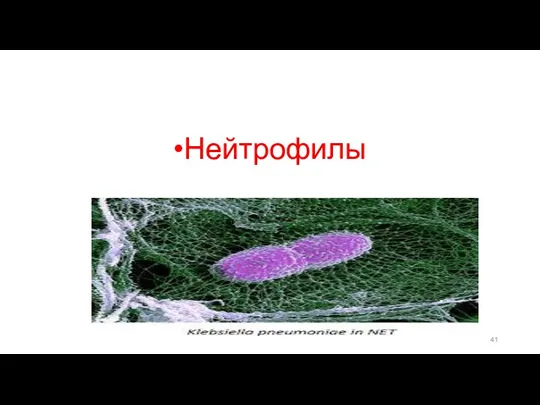
- 41. Нейтрофилы
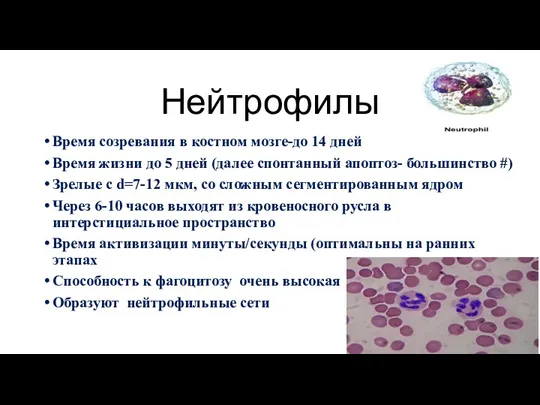
- 42. Нейтрофилы Время созревания в костном мозге-до 14 дней Время жизни до 5 дней (далее спонтанный апоптоз-
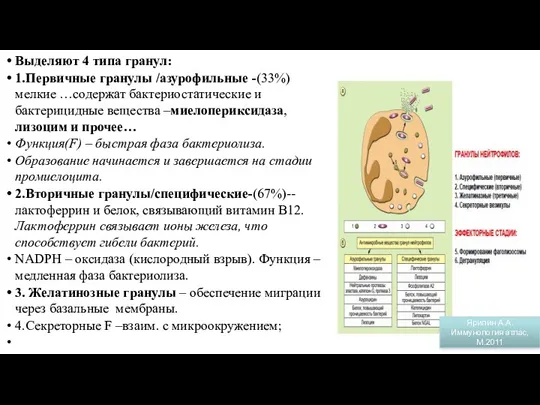
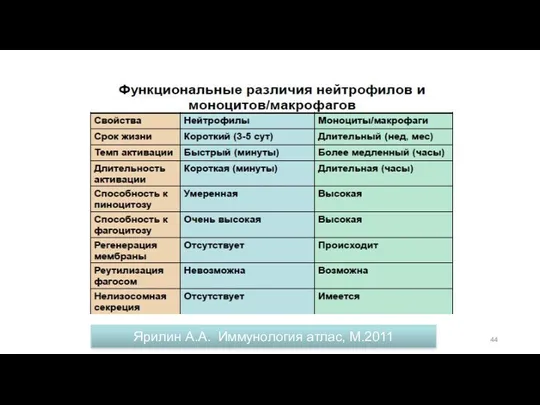
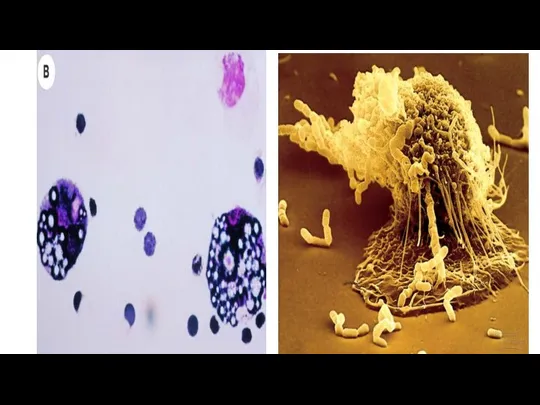
- 43. Гранулы нейтрофилов Выделяют 4 типа гранул: 1.Первичные гранулы /азурофильные -(33%) мелкие …содержат бактериостатические и бактерицидные вещества
- 44. Ярилин А.А. Иммунология атлас, М.2011
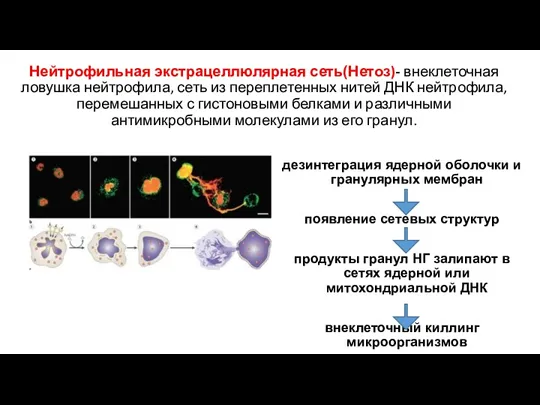
- 45. Нейтрофильная экстрацеллюлярная сеть(Нетоз)- внеклеточная ловушка нейтрофила, сеть из переплетенных нитей ДНК нейтрофила, перемешанных с гистоновыми белками
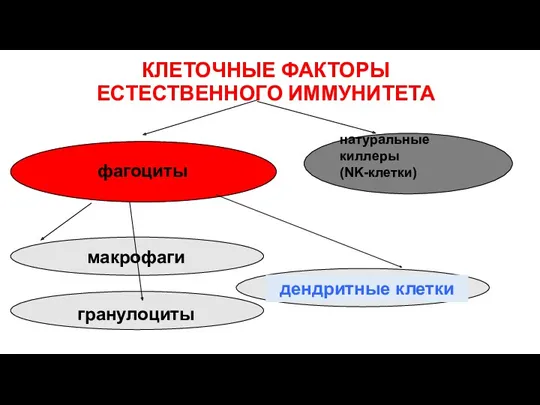
- 46. КЛЕТОЧНЫЕ ФАКТОРЫ ЕСТЕСТВЕННОГО ИММУНИТЕТА натуральные киллеры (NK-клетки) фагоциты макрофаги гранулоциты дендритные клетки
- 47. КЛЕТОЧНЫЕ ФАКТОРЫ ЕСТЕСТВЕННОГО ИММУНИТЕТА натуральные киллеры (NK-клетки) фагоциты макрофаги гранулоциты дендритные клетки
- 48. ДЕНДРИТНЫЕ КЛЕТКИ
- 49. Дендритные клетки миелоидные дендритные клетки ( mDC) — происходят от общего миелоидного предшественника. Локализованы в различных
- 50. Дендритные клетки-Дендритные клетки (англ. DC) — это гетерогенная популяция антигенпрезентирующих клеток КМ. Крупные клетки (15-20 мкм)
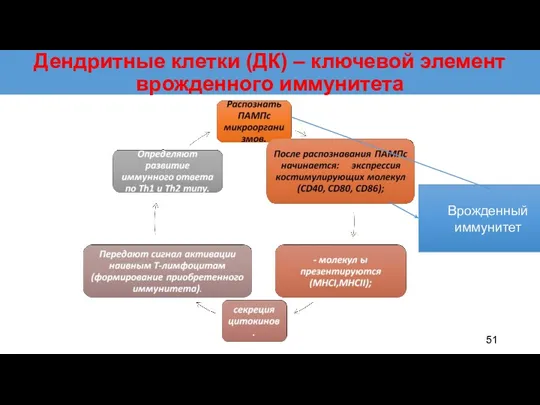
- 51. Дендритные клетки (ДК) – ключевой элемент врожденного иммунитета Врожденный иммунитет
- 52. Естественные (натуральные) киллеры
- 53. КЛЕТОЧНЫЕ ФАКТОРЫ ЕСТЕСТВЕННОГО ИММУНИТЕТА натуральные киллеры (NK-клетки) фагоциты макрофаги гранулоциты дендритные клетки
- 54. Естественные киллеры клетки NK – “natural killers”распознают через активирующие рецепторы и уничтожают на основе распознавания клетки-мишени,
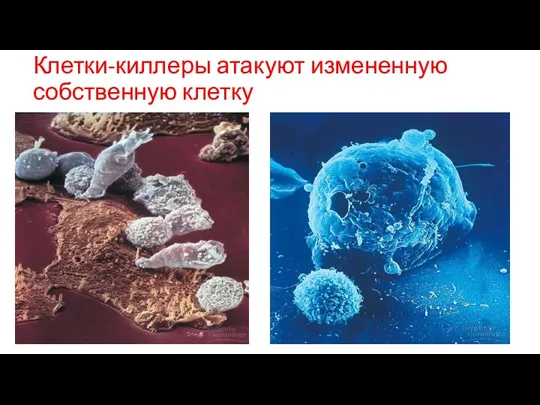
- 55. Клетки-киллеры атакуют измененную собственную клетку
- 56. Мы это разбирали на первой части лекции Принципы иммунологического распознавания 3. «Отсутствие своего» (молекулярный пароль) –
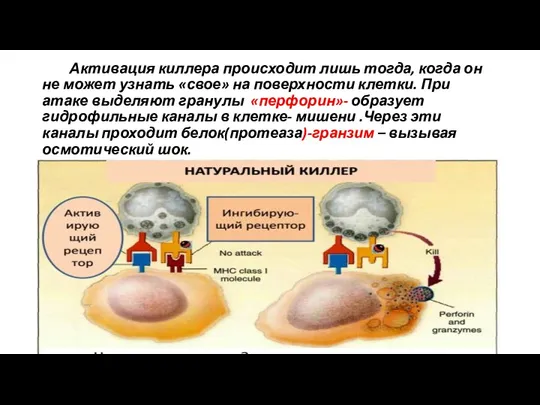
- 57. Активация киллера происходит лишь тогда, когда он не может узнать «свое» на поверхности клетки. При атаке
- 58. Принцип действия NK - клетки. Если естественные киллеры не находят на клетках рецептора МНС I класса,
- 59. ФАГОЦИТОЗ
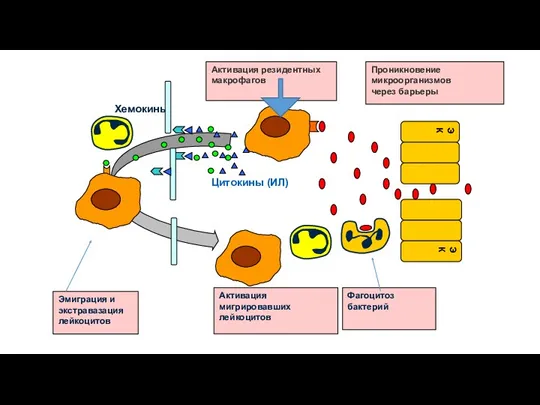
- 60. РАСПОЗНАВАНИЕ ЧУЖЕРОДНЫХ МИКРООРГАНИЗМОВ (НЕПОСРЕДСТВЕННО ИЛИ ЧЕРЕЗ ОПСОНИЗАЦИЮ) и ФАГОЦИТОЗ ГЕНЕРАЦИЯ МЕДИАТОРОВ ВОСПАЛЕНИЯ ( метаболиты арахидоновой кислоты,
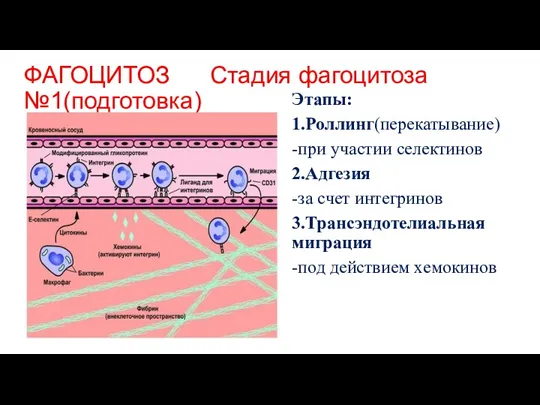
- 63. ФАГОЦИТОЗ Стадия фагоцитоза №1(подготовка) в очаг воспаления Этапы: 1.Роллинг(перекатывание) -при участии селектинов 2.Адгезия -за счет интегринов
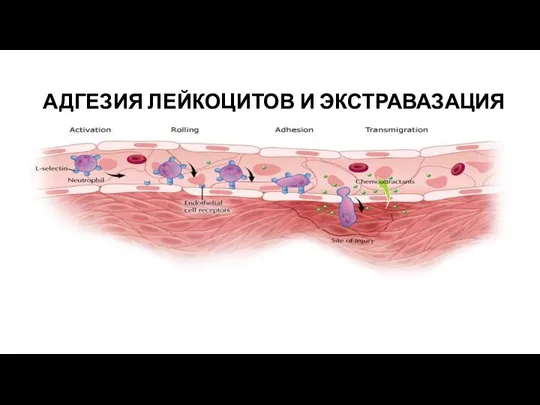
- 64. АДГЕЗИЯ ЛЕЙКОЦИТОВ И ЭКСТРАВАЗАЦИЯ
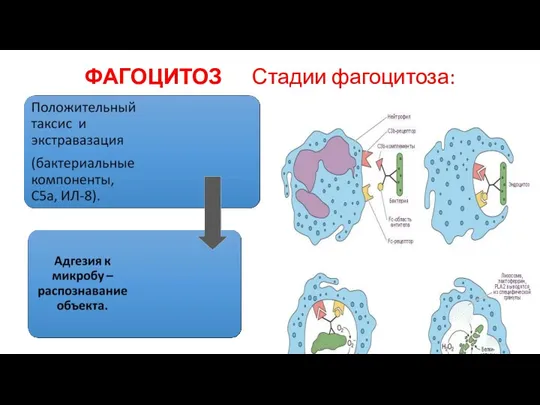
- 65. ФАГОЦИТОЗ Стадии фагоцитоза:
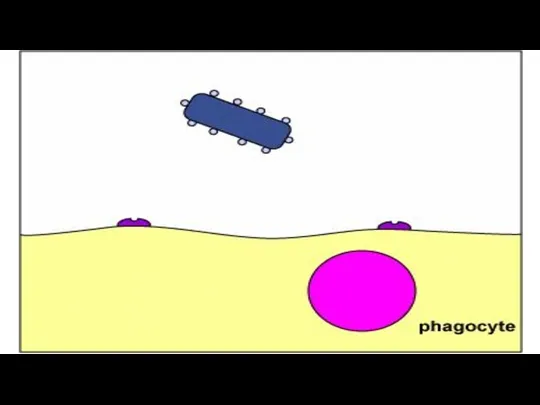
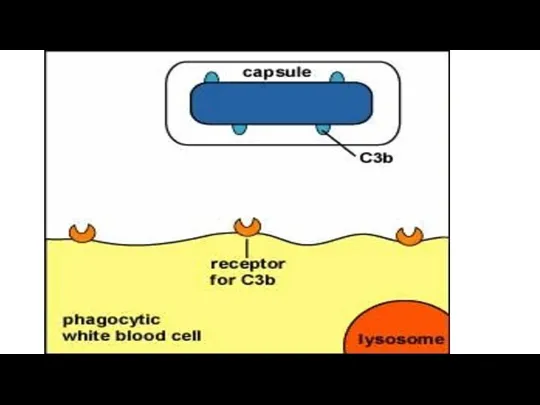
- 66. Опсонины Процесс фагоцитоза усиливают опсонины – белки, обволакивающие микробы, корпускулярные антигены и усиливающие их фагоцитоз. Роль
- 67. Процесс фагоцитоза усиливают опсонины ( на слайде показано , что отличное качество фагоцитоза возможно лишь при
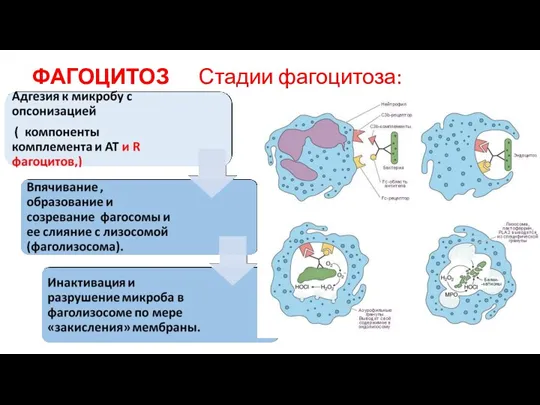
- 68. ФАГОЦИТОЗ Стадии фагоцитоза:
- 69. Механизмы фагоцитоза завершенный и не завершенный фагоцитоз
- 70. Киллинг ОСУЩЕСТВЛЯЕТСЯ в фагоците 1. кислородозависимые механизмы: - метаболиты кислорода - метаболиты азота 2. кислородонезависимые механизмы
- 71. КИСЛОРОДЗАВИСИМЫЙ (ОКСИДАЗОТНЫЙ) МЕХАНИЗМ Молекулярный кислород поэтапно превращается в супеpоксидный анион-радикал (∙О2-) и пеpоксид водоpода (Н2О2) и
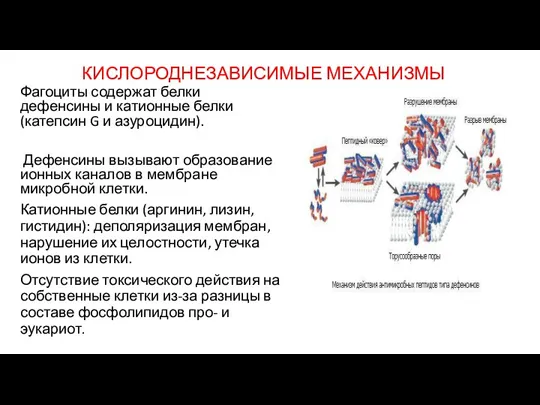
- 72. КИСЛОРОДНЕЗАВИСИМЫЕ МЕХАНИЗМЫ Фагоциты содержат белки дефенсины и катионные белки (катепсин G и азуроцидин). Дефенсины вызывают образование
- 73. Фагоцитоз (анимация)
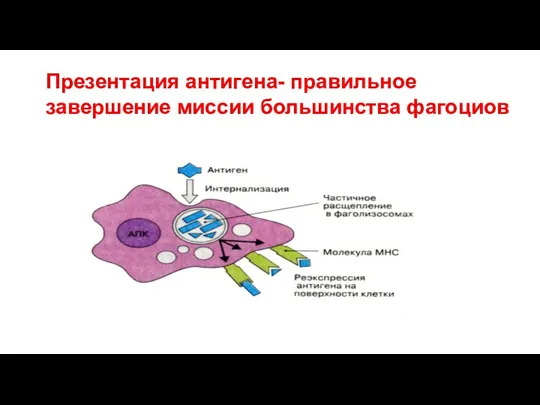
- 76. Презентация антигена- правильное завершение миссии большинства фагоциов
- 77. ЭТАПЫ ФАГОЦИТОЗА (РЕЗЮМЕ) Активация фагоцита (распознавание хемотаксических сигналов) Хемотаксис - направленная миграция в сторону увеличения хемотаксических
- 78. Незавершенный фагоцитоз В процессе захвата бактерий фагоциты образуют фагосому, которая постепенно созревает, формируя условия для киллинга
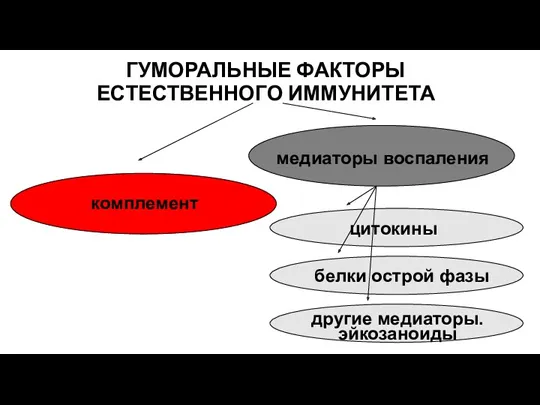
- 79. ГУМОРАЛЬНЫЕ ФАКТОРЫ ЕСТЕСТВЕННОГО ИММУНИТЕТА
- 80. ГУМОРАЛЬНЫЕ ФАКТОРЫ ЕСТЕСТВЕННОГО ИММУНИТЕТА комплемент медиаторы воспаления цитокины белки острой фазы другие медиаторы. эйкозаноиды
- 81. Комплемент Система комплемента – комплекс гликопротеидов сыворотки крови, участвующих в воспалении, опсонизации (обволакивании) антигенов для фагоцитоза,
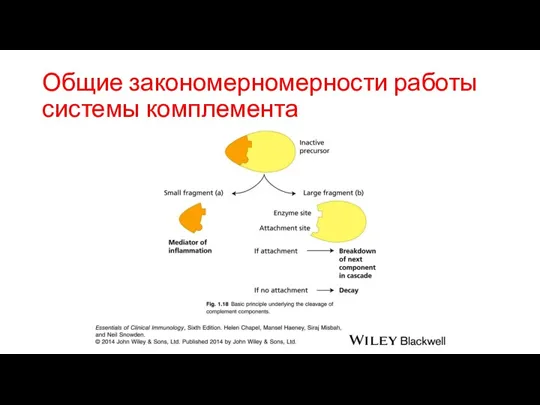
- 82. Общие закономерномерности работы системы комплемента
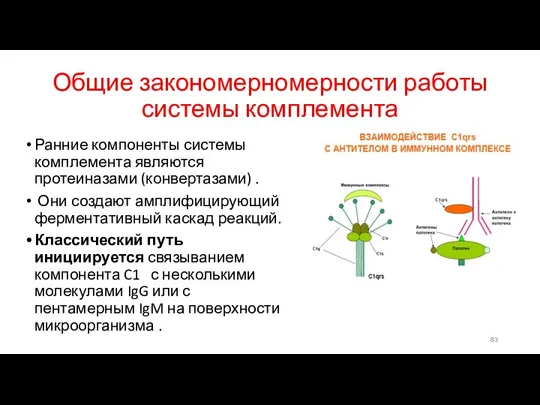
- 83. Общие закономерномерности работы системы комплемента Ранние компоненты системы комплемента являются протеиназами (конвертазами) . Они создают амплифицирующий
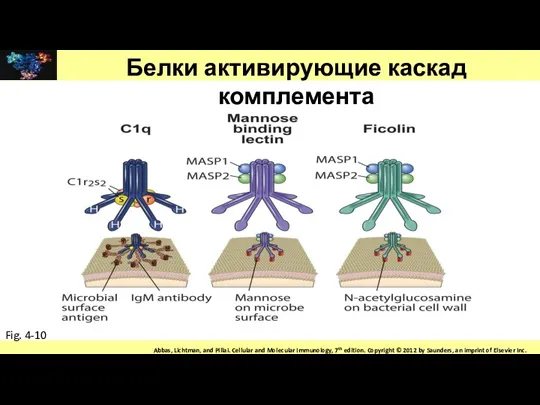
- 84. Белки активирующие каскад комплемента Fig. 4-10
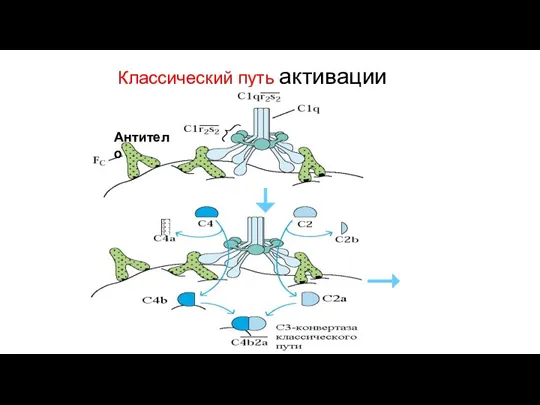
- 85. Классический путь
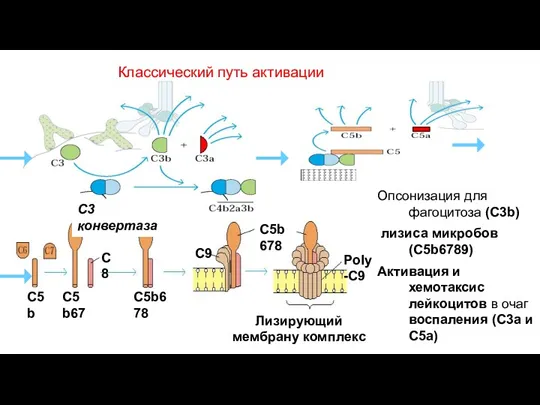
- 86. Классический путь активации
- 87. Классический путь активации Опсонизация для фагоцитоза (C3b) лизиса микробов (С5b6789) Активация и хемотаксис лейкоцитов в очаг
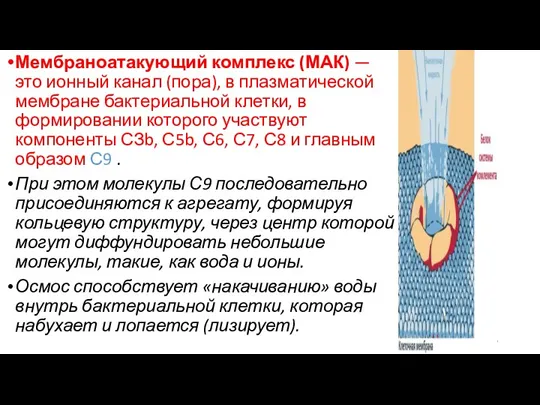
- 88. Мембраноатакующий комплекс (МАК) — это ионный канал (пора), в плазматической мембране бактериальной клетки, в формировании которого
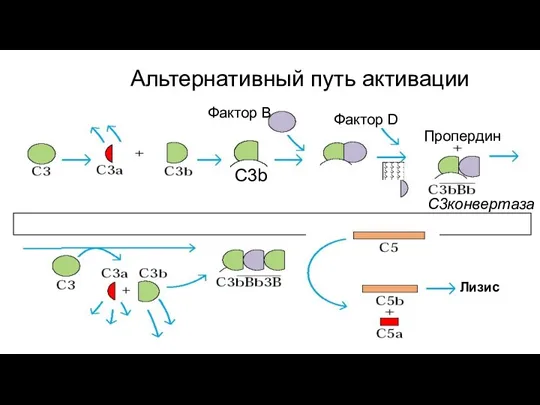
- 90. Альтернативный путь
- 91. Альтернативный путь инициируется связыванием фактора В, например, с бактериальным липополисахаридом (эндотоксином) или спонтанная диссоциация С3. И
- 92. Альтернативный путь активации
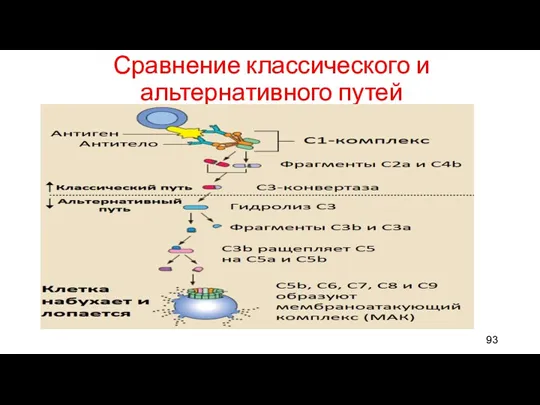
- 93. Сравнение классического и альтернативного путей
- 94. Лектиновый путь активации
- 95. Лектиновый путь активации Сывороточный маннозосвязывающий МС рецептор, связываясь с концевыми маннозными группами на поверхности бактерий, взаимодействует
- 96. Ярилин А.А. Иммунология атлас, М.2011
- 97. Система комплемента может действовать тремя различными способами: • через хемотаксис: различные компоненты (факторы) комплемента могут привлекать
- 98. Выводы:
- 99. Цитокины врожденного иммунитета и белки острой фазы
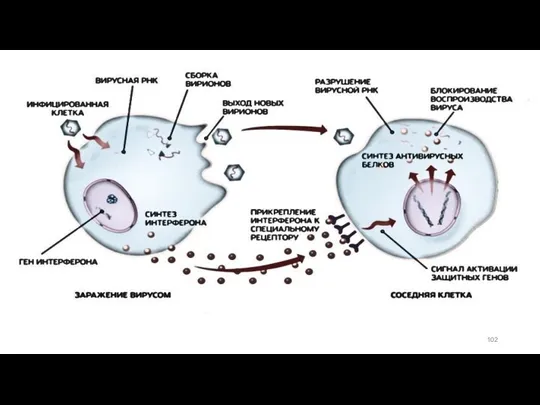
- 100. Интерфероны Интерфероны - гликопротеины, вырабатываемые клетками в ответ на вирусную инфекцию и другие стимулы. Блокируют репликацию
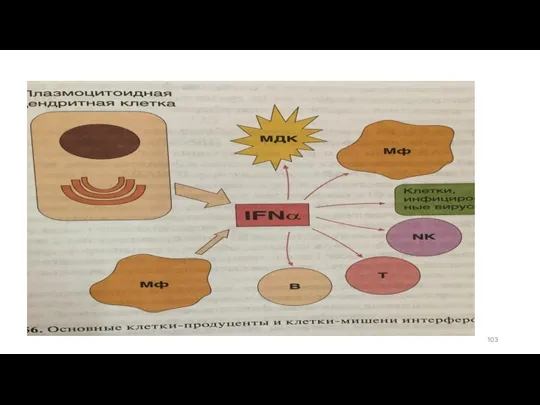
- 101. Интерфероны(ИФН) I типа Источник ИФН: плазмоцитоидные ДК Индуктор : двуспиральная Рнк у млекопитающих нет такой молекулы
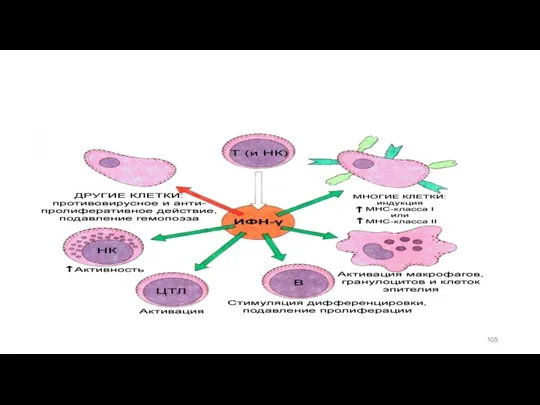
- 104. Интерфероны II типа ИФН-γ ("иммунный ИФН") продуцируется Т-лимфоцитами и NK. Стимулирует активность Т- и В-лимфоцитов, моноцитов/макрофагов
- 106. Растворимые рецепторы для патогенов. Пентраксины и Белки острой фазы: • С-реактивный белок – связывается с С-полисахаридом
- 107. Пентраксины и Белки острой фазы: Пропердин – гамма-глобулин нормальной сыворотки. Активация комплемента по альтернативному пути Фибронектин
- 108. Антимикробные пептиды 1. Лизоцим – фермент муромидаза синтезируется макрофагами и нейтрофилами и вызывает гидролиз муреина (пептидокликана)
- 110. Скачать презентацию




























































 Правовая система в Португалии
Правовая система в Португалии презентация Наркотики-дорога в никуда
презентация Наркотики-дорога в никуда Разложение многочлена на множители различными способами
Разложение многочлена на множители различными способами ПРИМЕНЕНИЕ АЛГОРИТМОВ В ЛИЧНОСТНО-ОРИЕНТИРОВАННОМ ОБУЧЕНИИ НА УРОКАХ МАТЕМАТИКИ
ПРИМЕНЕНИЕ АЛГОРИТМОВ В ЛИЧНОСТНО-ОРИЕНТИРОВАННОМ ОБУЧЕНИИ НА УРОКАХ МАТЕМАТИКИ Памятка - рекомендации для педагогов по составлению статьи
Памятка - рекомендации для педагогов по составлению статьи Сети фиксированной телефонной связи
Сети фиксированной телефонной связи Городской конкурс проектов Мы любим свой город
Городской конкурс проектов Мы любим свой город Русский футуризм. Поэзия
Русский футуризм. Поэзия Элементы принципиальной электрической схемы
Элементы принципиальной электрической схемы Микропроцессоры. Логические основы ЭВМ, элементы и узлы
Микропроцессоры. Логические основы ЭВМ, элементы и узлы Ломыга И.В._Психологическая безопасность как фактор корпоративной культуры
Ломыга И.В._Психологическая безопасность как фактор корпоративной культуры Техническое обслуживание и ремонт электрооборудования специально токарного станка ИЖ-250
Техническое обслуживание и ремонт электрооборудования специально токарного станка ИЖ-250 wepik-gruziia-istoriia-kultura-i-priroda-20240206154241hfGr
wepik-gruziia-istoriia-kultura-i-priroda-20240206154241hfGr Тірі организмдердегі металдардың рөлі
Тірі организмдердегі металдардың рөлі Интеллектуальный марафон - 2 (2 класс)
Интеллектуальный марафон - 2 (2 класс) Нарушение кровообращения и лимфообращения. Лекция № 4
Нарушение кровообращения и лимфообращения. Лекция № 4 Осциллографы
Осциллографы Водопады- уникальные природные памятники
Водопады- уникальные природные памятники Социокультурное пространство города
Социокультурное пространство города Огонь - наш друг и враг
Огонь - наш друг и враг Економічні аспекти глобальних проблем
Економічні аспекти глобальних проблем Презентация по теме Мировой океан 6 класс
Презентация по теме Мировой океан 6 класс Примерная структура планирования воспитательно-образовательной работы на 1 день
Примерная структура планирования воспитательно-образовательной работы на 1 день Полимеры. Каучуки. Резина
Полимеры. Каучуки. Резина Наклонно направленные скважины
Наклонно направленные скважины 20230209_prez.ovz_1
20230209_prez.ovz_1 Захист прав українських туристів за межами України
Захист прав українських туристів за межами України Электроснабжение ремонтно-механического цеха
Электроснабжение ремонтно-механического цеха