Мемлекеттік тіркеу, қайта тіркеу және тіркеу мәліметтеріне өзгерістерді енгізу кезінде жүзеге асырылатын ДЗ тиімділігін презентация
Содержание
- 2. Жоспар Кіріспе ДЗ тіркеу: жалпы ережелер Біртұтас Экономикалық Кеңістікке (БЭК) қатысушы мемлекеттерде дәрілік заттарды тіркеу ерекшеліктері
- 3. Кіріспе Қазіргі таңда, ДЗ мемлекеттік тіркеу жұмыстарын Денсаулық Сақтау Министрлігінің (ДСМ) ведомствосы – Фармация Комитеті РМК
- 4. ДЗ тіркеу: жалпы ережелер ДЗ тіркеу бұл — белгілі бір мемлекет аясында ДЗ тауарайналымға (қолданысқа) түсуіне
- 5. Мемлекеттік тіркелуге тиісті дәрілік заттар Мемлекеттік тіркеу және қайта тіркеуге Қазақстан Республикасында өндірілген, сонымен қатар осы
- 6. 4) Қазақстан Республикасында бұрын тіркелген бірақ басқа өндіруші мекемемен басқа дәрілік түрде жаңа мөлшерімен, жаңа түптелуімен,
- 7. Мемлекеттік тіркелуге тиісті емес дәрілік заттар Дәріханаларда дайындалған дәрілік препараттар Тиісті өндірістік тәжірибе жағдайларында жасалған дәрілік
- 8. Дәрілік заттарды тіркеуге керекті негізгі құжаттар Қазақстан Республикасында дәрілік заттарды мемлекеттік тіркеуге, қайта тіркеуге өтініш немесе
- 9. Қазақстан Республикасында дәрілік заттарды мемлекеттік тіркеу, қайта тіркеу кезінде ұсынылатын тіркеу деректерінің тізбесі I бөлім Жалпы
- 10. Жалпы техникалық құжат форматында (тиісті өндірістік практика жағдайында өндірілген дәрілік заттар үшін) Қазақстан Республикасында дәрілік заттарды
- 11. Біртұтас Экономикалық Кеңістікке (БЭК) қатысушы мемлекеттерде дәрілік заттарды тіркеу ерекшеліктері Сарапшылардың болжамдары бойынша осы альянс мемлекеттерінің
- 12. Ресей Федерациясының үлесіне 91%, ал Қазақстан мен Беларусь үлестеріне - 5 және 4% сәйкесінше тиесілі. Сонымен
- 13. Қарастырылып жатқан мемлекеттерде ДЗ-ды тіркеу процедураларында ұқсастық пен айырмашылықтар да бар. Бұл үрдіс жергілікті заңннамалар негізінде
- 14. Ресейде — РФ Денсаулық Сақтау және Әлеуметтік Даму Министрлігі (Минздравсоцразвития), Беларусияда — БР Денсаулық Сақтау Министрлігі
- 15. Кесте 1. БЭК-ке қатысушы мемлекеттерде ДЗ-ды тіркеуге уәкілетті сараптама мекемелері
- 16. Жалпы ДЗ-ды тіркеу процедурасын айтарлықтай ашық деп атауға болады. Қарастырылып жатқан мемлекеттер қолданысында бар негізгі заңнама
- 17. Кесте 2. БЭК мемлекеттерінде ДЗ-ты тіркеу кезінде қолданылатын негізгі заңнама актілері
- 18. Дегенмен, тіркеу регламенті көрсетілген заңнама актілерімен шектелмейді. Сонымен бірге тіркеу процедураларын регламенттейтін жергілікті бұйрықтар, қаулылар мен
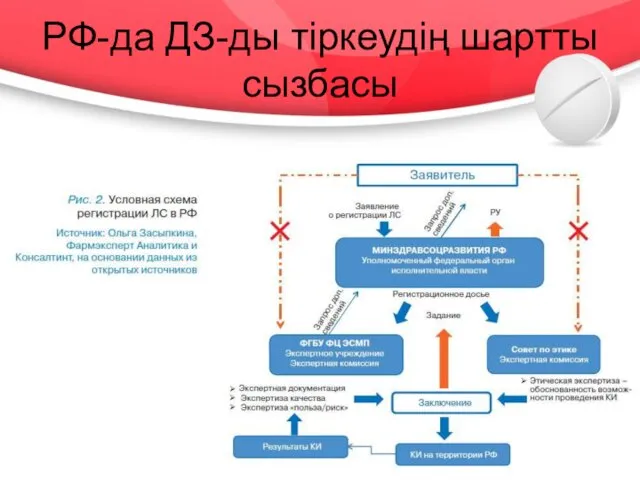
- 19. РФ-да ДЗ-ды тіркеудің шартты сызбасы
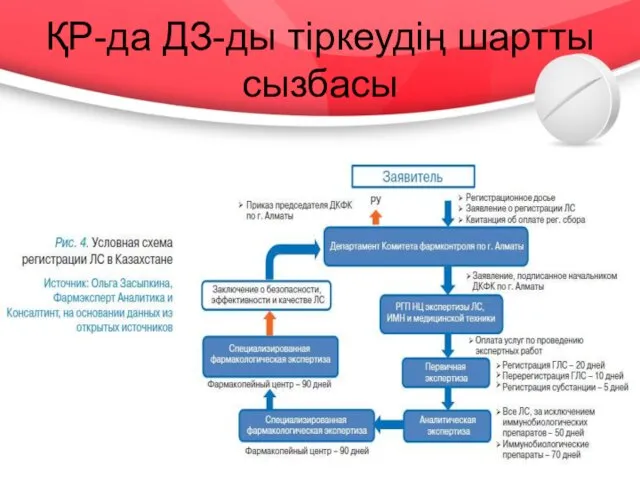
- 20. ҚР-да ДЗ-ды тіркеудің шартты сызбасы
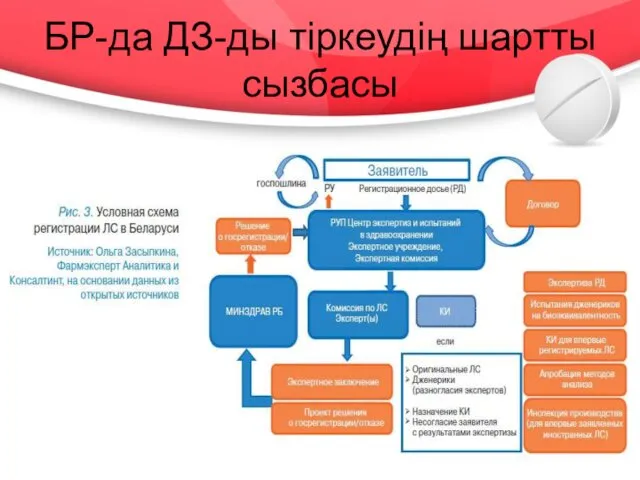
- 21. БР-да ДЗ-ды тіркеудің шартты сызбасы
- 22. ДЗ-тың сапасын стандартизациялау ДЗ-тың сапасын бақылау тіркеу процедурасында міндетті кезеңдерінің бірі болып табылады. Әрбір қарастырылатын мемлекеттерде
- 23. ҚР территориясында көптеген халықаралық Фармакопеялар танылған. Қазақстанның Мемлекеттік Фармакопеясындағы редакцияларға түсірілген материалдары Европалық Фармакопеямен жақындастырады, бірақ
- 24. Тіркеу мерзімдері БЭК-ке қатысушы мемлекеттердің әрқайсысында ДЗ-ты тіркеу мерзімі, сонымен қатар осы процедураның құны, ең алдымен,
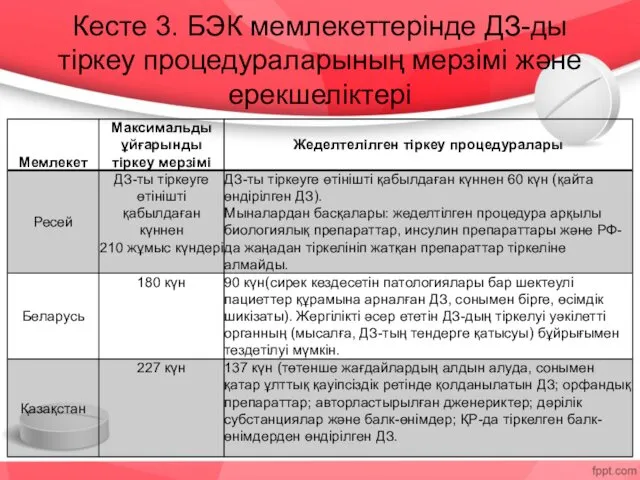
- 25. Кесте 3. БЭК мемлекеттерінде ДЗ-ды тіркеу процедураларының мерзімі және ерекшеліктері
- 26. Барлық қарастырылған мемлекеттерде тіркеу мерзіміне клиникалық зерттеулер (КЗ) жүргізу мерзімі есептелінбеген. Егер Сараптама Комиссиясымен қосымша клиникалық
- 27. Клиникалық зерттеулер/сынақтар ДЗ-ды тіркеуді регламенттейтін негізгі құжаттарда табылатын ең бірінші ерекшелік– «клиникалық зерттеулер» (РФ) және «клиникалық
- 28. РФ-да ФЗ-61 сәйкес КЗ немесе КЗ-дің бөлігі Ресей территориясында жүргізілуі тиіс (барлық ДЗ; тек тауарайналым периоды
- 29. Қорытынды БЭК-ке қатысушы-мемлекеттерінде ДЗ-ды тіркеу процедуралары, сонымен бірге олардың құны мен мерзімі бір-бірінен айтарлықтай ерекшелінеді. Бірақ
- 31. Скачать презентацию
























 Качество товаров
Качество товаров Презентация к сказке Колосок
Презентация к сказке Колосок Westfälische Wilhelms-Universität Münster
Westfälische Wilhelms-Universität Münster Экономический кризис 1998 года
Экономический кризис 1998 года Морские волны, возникающие при подводных и прибрежных землетрясениях - цунами
Морские волны, возникающие при подводных и прибрежных землетрясениях - цунами Студенческая футбольная лига
Студенческая футбольная лига Бассүйек-ми жарақаты
Бассүйек-ми жарақаты Признаки делимости натуральных чисел от 2 до 25 и на 50
Признаки делимости натуральных чисел от 2 до 25 и на 50 Замена пролетных строений консольными кранами
Замена пролетных строений консольными кранами Автоматическая установка умягчения воды непрерывного действия Passion for Progress © BMA
Автоматическая установка умягчения воды непрерывного действия Passion for Progress © BMA Новый Год шагает по планете. Викторина
Новый Год шагает по планете. Викторина Презентация Школьная библиотека
Презентация Школьная библиотека Профессии, связанные с созданием изделий из древесины и древесных материалов
Профессии, связанные с созданием изделий из древесины и древесных материалов Слюна и ротовая жидкость
Слюна и ротовая жидкость Информационные технологии как система. Лекция 1
Информационные технологии как система. Лекция 1 Ароматические углеводороды
Ароматические углеводороды Знакомьтесь. Геометрия
Знакомьтесь. Геометрия 20230612_algebra_9_klass_presentatsia_generalnai_sovokupnost_i_viborka
20230612_algebra_9_klass_presentatsia_generalnai_sovokupnost_i_viborka Проект Скоро в школу!
Проект Скоро в школу! Полномочия прокурора возбужденным по делам в виду новых или вновь открывшихся обстоятельств
Полномочия прокурора возбужденным по делам в виду новых или вновь открывшихся обстоятельств Введение в Delphi. (Лекция 2)
Введение в Delphi. (Лекция 2) ФЗ О бухгалтерском учете
ФЗ О бухгалтерском учете Шарик улетел.
Шарик улетел. Бактериофагия, бактериофаги
Бактериофагия, бактериофаги Шкільна форма
Шкільна форма Ярославская область. Основные социально-экономические показатели
Ярославская область. Основные социально-экономические показатели творчество В.М. Васнецова Наши сказки
творчество В.М. Васнецова Наши сказки Звук Ль Диск Диск Диск
Звук Ль Диск Диск Диск