Содержание
- 2. Литература
- 3. Отбор, транспортировка и хранение проб для химического анализа
- 4. Главные принципы отбора проб Проба природного объекта должна отражать условия и место взятия. Отбор пробы, транспортировка,
- 5. ТЕХНИКА ОТБОРА ПРОБ Выбор места для отбора проб зависит от целей анализа. Виды отбора проб бывают:
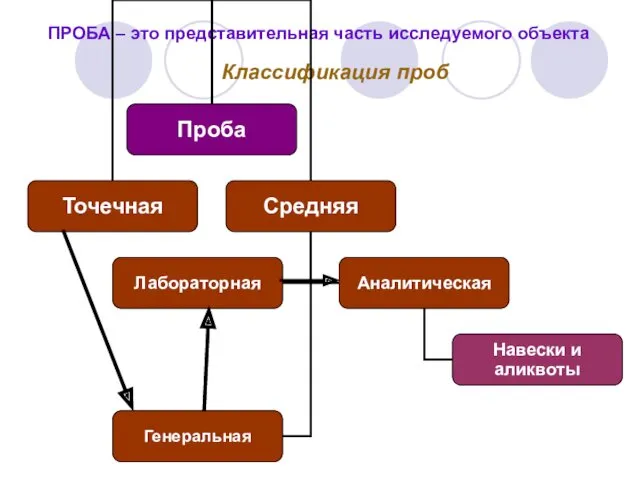
- 6. Классификация проб ПРОБА – это представительная часть исследуемого объекта
- 7. Для каждого рода материала существуют специальные правила пробоотбора, регламентирующие порядок проведения отдельных операций (прописаны ГОСТ). ПРОБЫ
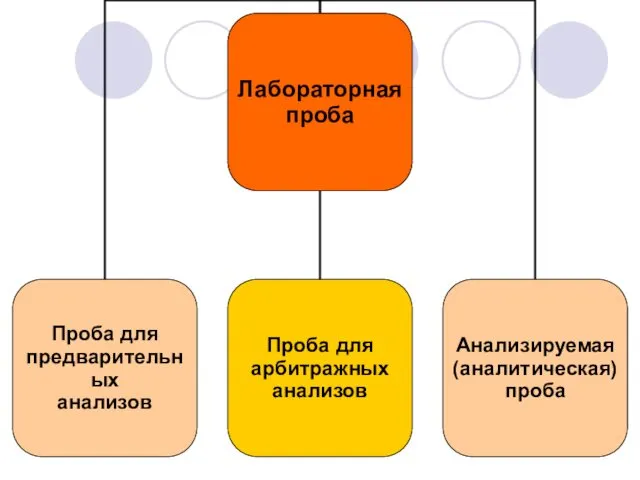
- 9. Лабораторная проба – конечная промежуточная проба, полученная при сокращении генеральной пробы и поступившая в лабораторию для
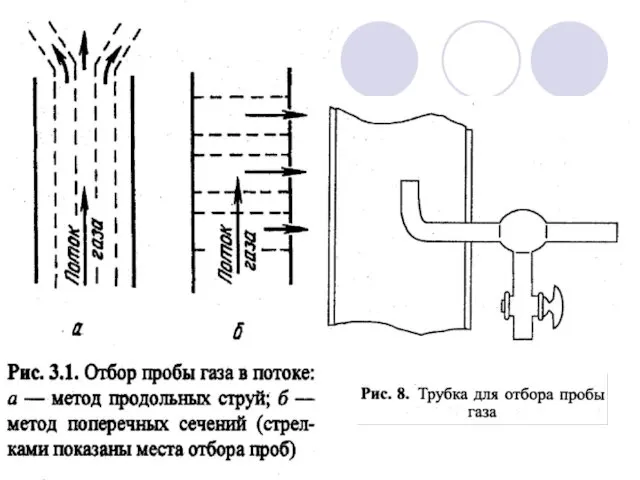
- 11. Отбор проб конкретных природных объектов. ГАЗЫ. ВОЗДУХ Основные требования к пробоотбору: Предохранять пробы от потери в
- 12. Методы пробоотбора газов и воздуха (атмосферного, рабочей зоны) Вакуумные (без концентрирования) основаны на заборе небольших объемов
- 13. Вакуумные методы Аспирационные методы
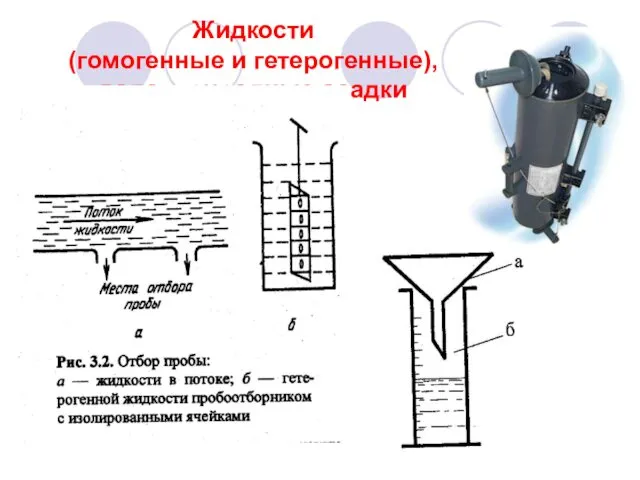
- 15. Жидкости (гомогенные и гетерогенные), вода, природные осадки
- 16. Батометр Автоматические пробоотборники Пробоотборный сосуд Пробоотборники воды
- 17. Требования к пробоотборным устройствам Они не должны: Являться причиной загрязнения пробы. Абсорбировать или адсорбировать определяемые компоненты.
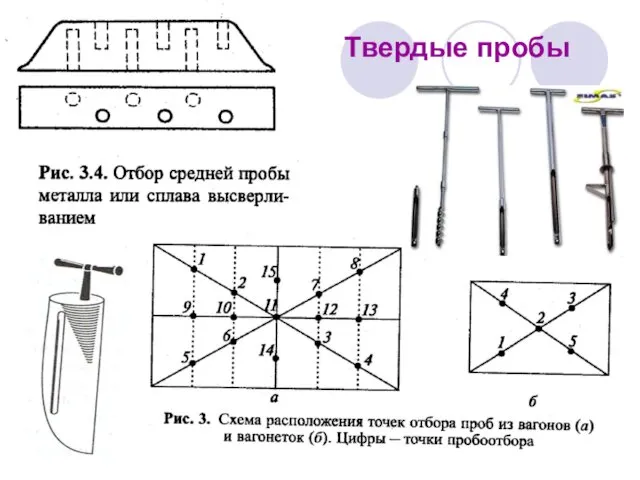
- 18. Твердые пробы
- 19. Донные отложения, почва, грунты
- 20. ПЕРВИЧНАЯ ПРОБОПОДГОТОВКА Стабилизация и хранение проб
- 21. Способы стабилизации проб Применение максимально инертной посуды. «Захолаживание» пробы. Затемнение пробы. Продувка пробы инертными газами. «Тренировка»
- 22. Правила консервации Используемые для консервации реагенты-стабилизаторы должны быть высочайшей чистоты (ОСЧ, ХЧ,ЧДА). Материалы, из которых изготовлены
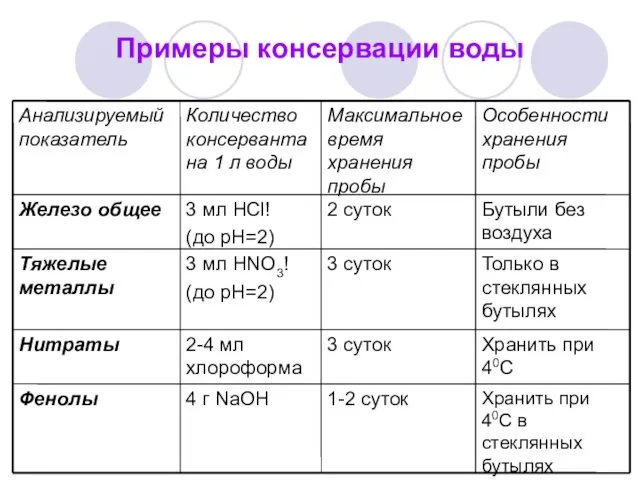
- 23. Примеры консервации воды
- 24. Транспортировка проб Должна быть: быстрой; в соответствующей таре, гарантирующей сохранность пробы. Для транспортировки проб часто используются
- 25. Особенности хранения различных проб ВОЗДУХ Пробы воздуха в контейнерах практически не хранятся. Могут храниться пробы взятые
- 26. ВОДА Без стабилизации вода не хранится (способы стабилизации см. ранее). Перед хранением вода обязательно консервируется. Применяемые
- 27. ПОЧВА Способ хранения пробы и ее упаковка зависят от целей анализа: Высушивают до воздушно-сухого состояния. Воздушно-сухие
- 28. РАСТЕНИЯ Способ хранения пробы и ее упаковка зависят от целей анализа: Высушивают до воздушно-сухого состояния. Воздушно-сухие
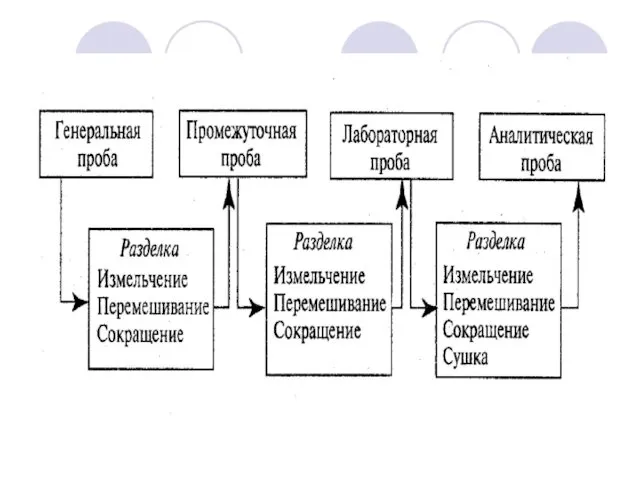
- 29. ОБРАБОТКА ГЕНЕРАЛЬНОЙ ПРОБЫ (ТВЕРДОЙ) Гомогенизация – получение однородного материала. Состоит из двух чередующихся операций: Дробление; Просеивание.
- 30. ДРОБЛЕНИЕ ПРОСЕИВАНИЕ ГОМОГЕНИЗАЦИЯ
- 31. Гомогенизация пробы ДРОБЛЕНИЕ Измельчители (мельницы, блендер) Фарфоровая ступка Механическая ступка
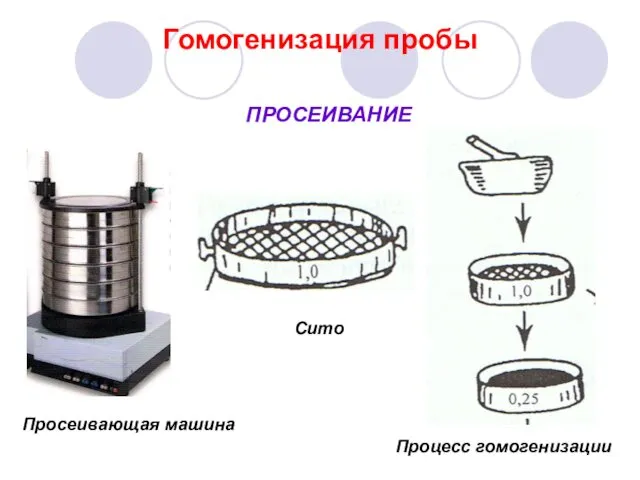
- 32. Гомогенизация пробы Процесс гомогенизации ПРОСЕИВАНИЕ Сито Просеивающая машина
- 33. УСРЕДНЕНИЕ ПЕРЕМЕШИВАНИЕ СОКРАЩЕНИЕ
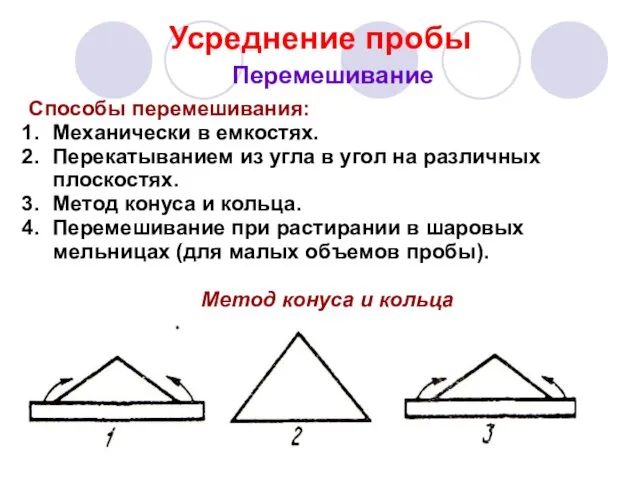
- 34. Усреднение пробы Перемешивание Способы перемешивания: Механически в емкостях. Перекатыванием из угла в угол на различных плоскостях.
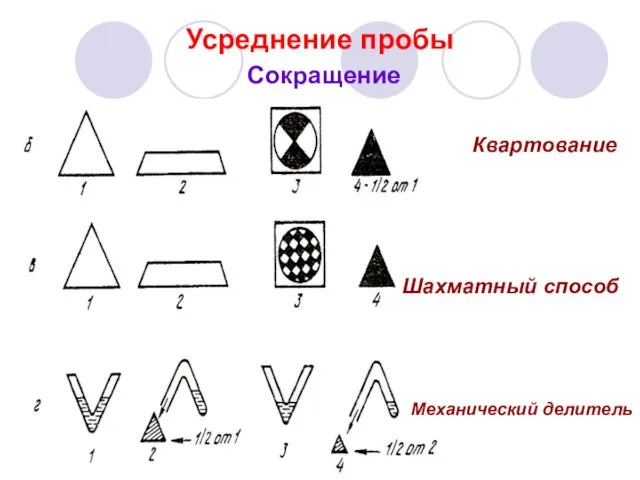
- 35. Усреднение пробы Сокращение Квартование Механический делитель Шахматный способ
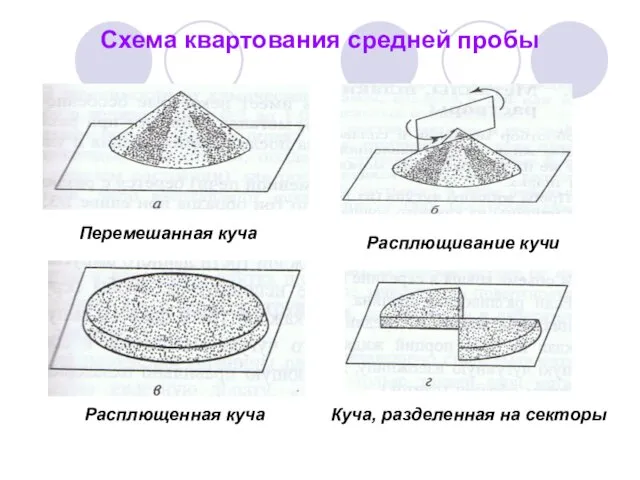
- 36. Схема квартования средней пробы Перемешанная куча Расплющивание кучи Расплющенная куча Куча, разделенная на секторы
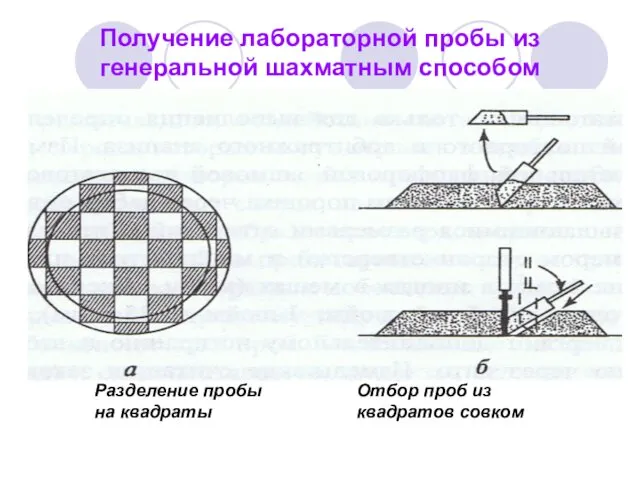
- 37. Получение лабораторной пробы из генеральной шахматным способом Разделение пробы на квадраты Отбор проб из квадратов совком
- 38. ВТОРИЧНАЯ ПРОБОПОДГОТОВКА Подготовка пробы к химическому анализу
- 39. Задачи вторичной пробоподготовки Высушивание пробы (удаление воды). Вскрытие (разложение пробы) и перевод ее в раствор. Обогащение
- 40. Вода в пробах Химически несвязанная вода (как загрязнение пробы): Адсорбированная на поверхности пробы твердого вещества. Сорбированная
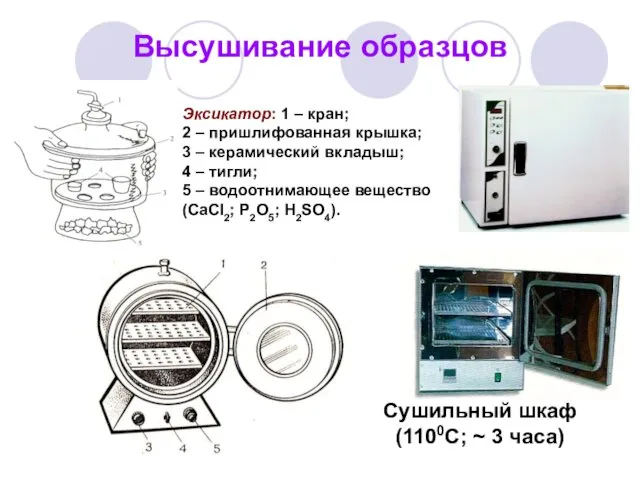
- 41. Высушивание образцов Сушильный шкаф (1100С; ~ 3 часа) Эксикатор: 1 – кран; 2 – пришлифованная крышка;
- 42. Разложение или вскрытие пробы Методы вскрытия проб: «Сухие» методы разложения (требуют дальнейшего растворения полученного остатка) –
- 43. «Сухие» методы. Термическое разложение Это разложение пробы при нагревании, сопровождающееся образованием одного или нескольких компонентов газообразной
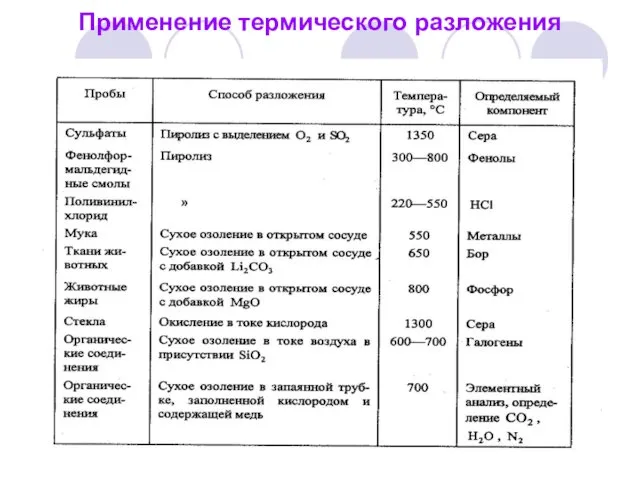
- 44. Применение термического разложения
- 45. «Сухие» методы. Сплавление и спекание Сплавление – измельченную пробу смешивают с 8 –10-кратным избытком реагента (плавня)
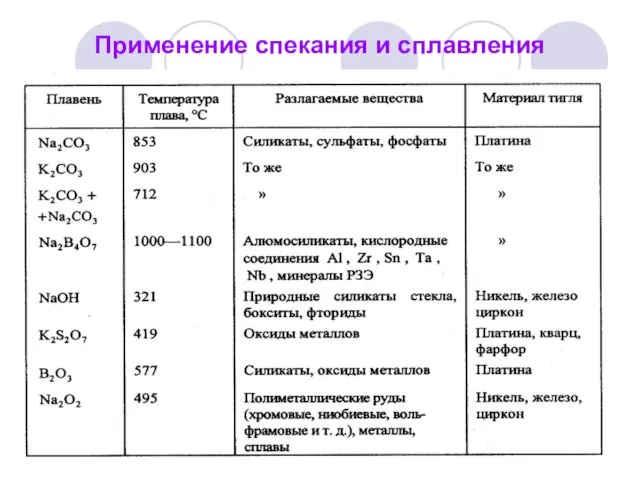
- 46. Классификация реагентов для сплавления и спекания Плавни: Щелочные (карбонаты, гидроксиды, бораты щелочных металлов и их смеси).
- 47. Применение спекания и сплавления
- 48. Оборудование для «сухих» методов разложения Муфельная печь Микроволновая печь Нагревательная камера
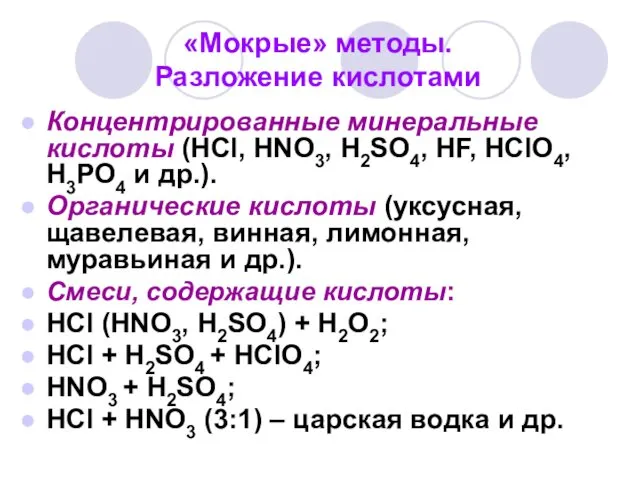
- 49. «Мокрые» методы. Разложение кислотами Концентрированные минеральные кислоты (HCl, HNO3, H2SO4, HF, HClO4, H3PO4 и др.). Органические
- 51. «Мокрые» методы. Другие способы Водные растворы солей и оснований: Гидроксиды (NaOH, KOH); Карбонаты щелочных металлов (Na2CO3,
- 52. Оборудование для «мокрых» методов разложения Автоклав для разложения проб кислотами Микроволновая установка для мокрой минерализации проб
- 53. «МИНОТАВР» Прибор для «мокрой» минерализации проб
- 54. Растворение пробы Основные растворители: Вода. Органические растворители. Водные смеси (с кислотами; органическими растворителями). Водные растворы кислот,
- 55. Специфические способы подготовки к анализу ООС Почвы: Вытяжки (водные, солевые, кислотные, буферные). Растения: Сок. Вытяжки и
- 56. Оборудование для приготовления почвенных вытяжек
- 57. Перемешивающие устройства
- 58. Концентрирование Концентрирование – это операция, в результате которой повышается отношение концентрации или количества микрокомпонентов к концентрации
- 60. Скачать презентацию





































 Обследование звукослоговой структуры слов с использованием ИКТ
Обследование звукослоговой структуры слов с использованием ИКТ Кіномистецтво
Кіномистецтво Проект на тему Человек, которым я горжусь. Владимир Иванович Даль 1801-1872
Проект на тему Человек, которым я горжусь. Владимир Иванович Даль 1801-1872 Иконопись. Русская икона
Иконопись. Русская икона День недели…
День недели… Эстетикалық стоматология үшін оптикалық жүйенің маңызы
Эстетикалық стоматология үшін оптикалық жүйенің маңызы Презентация Интегративный подход в организации экспериментальной деятельности младших дошкольников
Презентация Интегративный подход в организации экспериментальной деятельности младших дошкольников Автомобильные грузовые транспортные средства
Автомобильные грузовые транспортные средства Военно-мостовая подготовка. Итоговый тест
Военно-мостовая подготовка. Итоговый тест ЧПУ станоктары
ЧПУ станоктары Материнская плата
Материнская плата Презентация к классному часу Наши права и обязанности
Презентация к классному часу Наши права и обязанности Межзвёздная среда: Газ и пыль
Межзвёздная среда: Газ и пыль мультик
мультик класс
класс русский 08.02
русский 08.02 Случаи вычитания 16-
Случаи вычитания 16- Клятвы на новый год
Клятвы на новый год Контроль качества строительно-монтажных работ
Контроль качества строительно-монтажных работ Проблематика романа М. Булгакова Белая гвардия
Проблематика романа М. Булгакова Белая гвардия Разработка урока Планеты Солнечной системы.
Разработка урока Планеты Солнечной системы. Сотворение человека. Православная антропология
Сотворение человека. Православная антропология The degrees of comparison of adjectives
The degrees of comparison of adjectives Проектная деятельность обучающихся. Проект по теме Сколько весит здоровье ученика?
Проектная деятельность обучающихся. Проект по теме Сколько весит здоровье ученика? 20191208_kraevedcheskoe_kazino_loyma_i_eyo_okrestnosti
20191208_kraevedcheskoe_kazino_loyma_i_eyo_okrestnosti Советский Союз в 1950--1991 годах
Советский Союз в 1950--1991 годах Испытание № 6. Бутерброд NETWORKING
Испытание № 6. Бутерброд NETWORKING Загадки про игрушки (ранний возраст)
Загадки про игрушки (ранний возраст)