Слайд 2

Многоатомные спирты – это органические соединения, в молекулах которых содержатся две
или более гидроксильных групп, соединенных с углеводородным радикалом.
Слайд 3
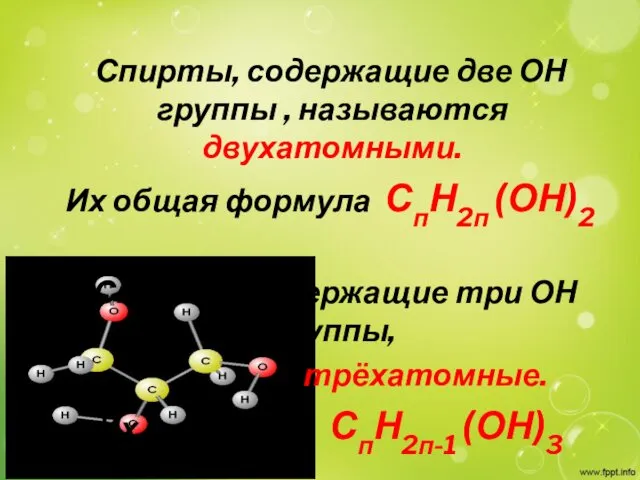
Спирты, содержащие две ОН группы , называются двухатомными.
Их общая
формула СпН2п (ОН)2
Спирты, содержащие три ОН группы,
трёхатомные.
Их СпН2п-1 (ОН)3
Слайд 4

Название гликоли- объясняется сладким вкусом первого представителя ряда- гликоля (от греч.
"гликос"- сладкий). По номенклатуре ИЮПАК эти спирты называются алкандиолы.
Простейшим представителем алкандиолов является спирт состава HO-CH2CH2-OH, так называемый этиленгликоль или этандиол.
Простейшим трехатомным спиртом является глицерин или пропантриол.
Слайд 5
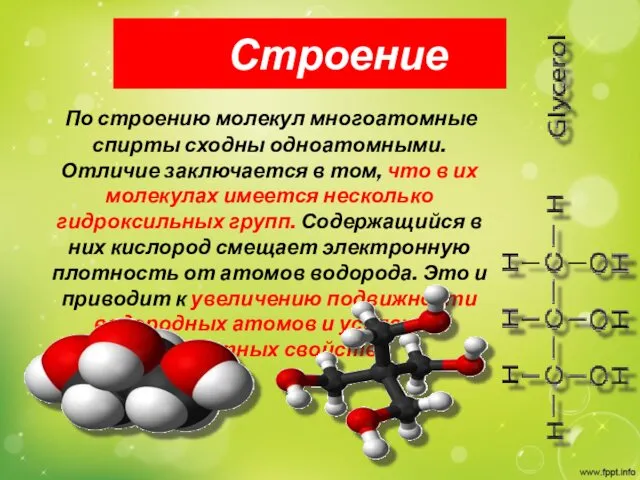
Строение
По строению молекул многоатомные спирты сходны одноатомными. Отличие заключается
в том, что в их молекулах имеется несколько гидроксильных групп. Содержащийся в них кислород смещает электронную плотность от атомов водорода. Это и приводит к увеличению подвижности водородных атомов и усилению кислотных свойств.
Слайд 6

Физические свойства
Этиленгликоль-представитель двухатомных спиртов-гликолей.
Сиропообразная жидкость сладковатого вкуса, без запаха, ядовит.
Хорошо смешивается
с водой и спиртом, гигроскопичен.
Глицерин-представитель трехатомных спиртов-глицеринов.
Бесцветная, вязкая, гигроскопическая жидкость, сладкая на вкус.
Смешивается с водой в любых отношениях.
Слайд 7

Получение
Гликоли получают окислением алкенов в водной среде. Например, при действии перманганата
калия или кислорода воздуха в присутствии серебряного катализатора алкены превращаются в двухатомные спирты:
Слайд 8

Другой способ получения многоатомных спиртов – гидролиз галогенпроизводных углеводородов:
Получение
Слайд 9
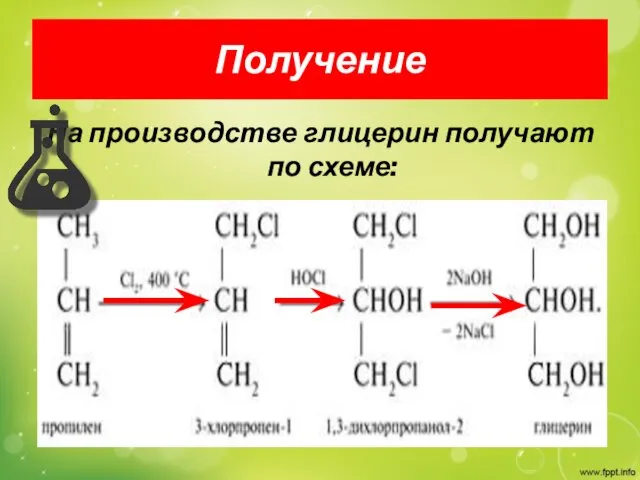
Получение
На производстве глицерин получают по схеме:
Слайд 10

Химические свойства
Замещение водорода гидроксогруппы:
с щелочными металлами
С растворами щелочей
Слайд 11

образование сложных эфиров.
с азотной кислотой
Химические свойства
Слайд 12

Химические свойства
Замещение всей гидроксогруппы
Слайд 13

Химические свойства
Качественная реакция многоатомных спиртов, позволяющая отличить соединения этого класса, –
взаимодействие со свежеприготовленным гидроксидом меди(II). В щелочной среде при достаточной концентрации глицерина голубой осадок Cu(OH)2 растворяется с образованием раствора ярко-синего цвета – гликолята меди(II)
Слайд 14

Применение этиленгликоля
Важным свойством этиленгликоля является способность понижать температуру замерзания воды, от
чего вещество нашло широкое применения как компонент автомобильных антифризов и незамерзающих жидкостей.
Он применяется для получения лавсана (ценного синтетического волокна).













 Патология гемостаза
Патология гемостаза Человек познает мир
Человек познает мир Развитие конфликтной компетентности подростков
Развитие конфликтной компетентности подростков Европа в XIX веке
Европа в XIX веке Утверждение авторитарных и тоталитарных режимов в Италии и Испании
Утверждение авторитарных и тоталитарных режимов в Италии и Испании Доноведение 4 класс Мой крайпрезентация
Доноведение 4 класс Мой крайпрезентация Grammar A2+articles
Grammar A2+articles Электрические станции и подстанции. Главные схемы распределительных устройств электростанций и подстанций. (Лекция 3)
Электрические станции и подстанции. Главные схемы распределительных устройств электростанций и подстанций. (Лекция 3) Самый умный. Игра
Самый умный. Игра Что означают английские надписи на одежде
Что означают английские надписи на одежде Урок труда Волшебные нитки, иголки и пуговицы
Урок труда Волшебные нитки, иголки и пуговицы 01 .НТД. ГФ
01 .НТД. ГФ Фотоальбом. Для Алексея
Фотоальбом. Для Алексея Деление с остатком
Деление с остатком Производство окиси этилена окислением этилена кислородом
Производство окиси этилена окислением этилена кислородом Охранно - пожарная сигнализация. Виды сигнализаций
Охранно - пожарная сигнализация. Виды сигнализаций Создание программы
Создание программы Аудирование как средство совершенствования лексического навыка
Аудирование как средство совершенствования лексического навыка Тренажёр Табличное умножение
Тренажёр Табличное умножение Мой любимый детский сад. Экскурсия в медицинский кабинет
Мой любимый детский сад. Экскурсия в медицинский кабинет Состав языка C#. Тема 2
Состав языка C#. Тема 2 Христианин в труде. 4 класс
Христианин в труде. 4 класс Михаил Юрьевич Лермонтов
Михаил Юрьевич Лермонтов Организация процесса приготовления и разработка ассортимента изделий из пряничного теста
Организация процесса приготовления и разработка ассортимента изделий из пряничного теста OECD_RU
OECD_RU Новогодний праздник Святки для 3-4 классов
Новогодний праздник Святки для 3-4 классов Светлая Пасха. История и традиции
Светлая Пасха. История и традиции Энергосбережение – умное потребление
Энергосбережение – умное потребление