Содержание
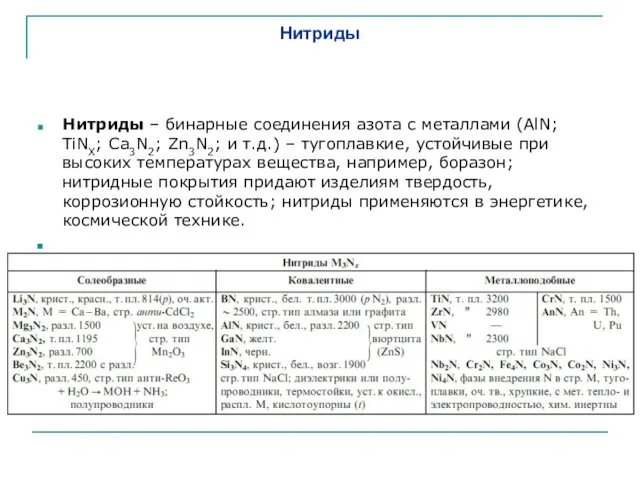
- 2. Нитриды Нитриды – бинарные соединения азота с металлами (AlN; TiNX; Ca3N2; Zn3N2; и т.д.) – тугоплавкие,
- 3. Нитриды Ионные нитриды. Связь в этих соединениях предполагает переход электронов от металла к азоту с образованием
- 4. Нитриды Ковалентные нитриды. Когда электроны азота участвуют в образовании связи совместно с электронами другого элемента без
- 5. Нитриды Нитрид алюминия AlN был впервые синтезирован в 1877, но только в середине 1980-ых, его потенциал
- 6. Нитриды Выше этой температуры происходит объёмное окисление материала. Нитрид алюминия устойчив в атмосферах водорода и углекислого
- 7. Нитриды Нитрид титана – соединение титана и азота состава TiNX (x = 0,58÷1,00), представляет собой фазу
- 8. Нитриды Нитрид титана
- 9. Нитриды Нитрид кремния Si3N4, желтоватые кристаллы; цвет поликристаллического нитрида кремния изменяется от белого до серого. Не
- 10. Нитриды Компактные изделия из Si3N4 получают спеканием, горячим прессованием, пиролизом соединений Si. Высокопрочные изделия производят спеканием
- 11. Нитриды Нитрид кремния Si3N4
- 12. Нитриды Нитрид бора BN. При обычных условиях устойчива графитоподобная α-модификация: белое кристаллическое вещество, т. пл. ~3000°С
- 13. Нитриды Модификация β-BN образуется из α-BN выше 1350°С и давлениях выше 5 ГПа в присутствии щелочных
- 14. Нитриды Нитрид бора BN Эрозионностойкие композиционные материалы на основе нитрида бора Заточные круги из нитрида бора
- 15. Нитриды Нитрид галлия GaN Ковалентный нитрид. Для объемного нитрида галлия термодинамически стабильной структурой является структура вюрцита,
- 16. Нитриды По мнению экспертов, промышленное использование GaN открывает большие перспективы для микроэлектроники – чипы на его
- 18. Скачать презентацию














 Осложнения и аварии в бурении
Осложнения и аварии в бурении Бумажная аппликация
Бумажная аппликация Синтез систем автоматического управления
Синтез систем автоматического управления Чувашская легенда
Чувашская легенда Самарская региональная общественная еврейская благотворительная организация. Курсы иврита
Самарская региональная общественная еврейская благотворительная организация. Курсы иврита Презентация по теме Работа по развитию мелкой моторики в системе здоровьесберегающих технологий
Презентация по теме Работа по развитию мелкой моторики в системе здоровьесберегающих технологий Лекарственные поражения печени
Лекарственные поражения печени Слайды
Слайды PartnerPlusBenefit - специальная бонусная программа для малых и средних предприятий
PartnerPlusBenefit - специальная бонусная программа для малых и средних предприятий Словосочетание
Словосочетание О мерах противодействия распространения ВИЧ-инфекции на территории города Вологды
О мерах противодействия распространения ВИЧ-инфекции на территории города Вологды Компьютерные игры. Советы для родителей.
Компьютерные игры. Советы для родителей. Новый год и Рождество в разных странах
Новый год и Рождество в разных странах Учение с увлечением!
Учение с увлечением! Религия в современном мире. Религиозные объединения и организации в Российской Федерации
Религия в современном мире. Религиозные объединения и организации в Российской Федерации Музыка в стиле джаз
Музыка в стиле джаз Упражнения для закрепления правильного употребления в речи предлогов.
Упражнения для закрепления правильного употребления в речи предлогов. Францияның еңбек туралы заңы
Францияның еңбек туралы заңы Презентация Какие растения самые важные
Презентация Какие растения самые важные Евреи (иудеи)
Евреи (иудеи) Инструктаж по поведению на льду
Инструктаж по поведению на льду Зачарована Десна (1956) - автобіографічна повість, спогади Олександра Довженка
Зачарована Десна (1956) - автобіографічна повість, спогади Олександра Довженка МИНИ МУЗЕЙ В ГРУППЕ РАННЕГО ВОЗРАСТА ТЕМА № 2 В ГОСТЯХ У СКАЗКИ Диск Диск
МИНИ МУЗЕЙ В ГРУППЕ РАННЕГО ВОЗРАСТА ТЕМА № 2 В ГОСТЯХ У СКАЗКИ Диск Диск Правила оформления презентации
Правила оформления презентации Борис Пастернак (1890-1960)
Борис Пастернак (1890-1960) Посвящается выпускникам 2020 года …
Посвящается выпускникам 2020 года … Телевизоры. Ключевые характеристики
Телевизоры. Ключевые характеристики Сибирская язва
Сибирская язва