Слайд 2
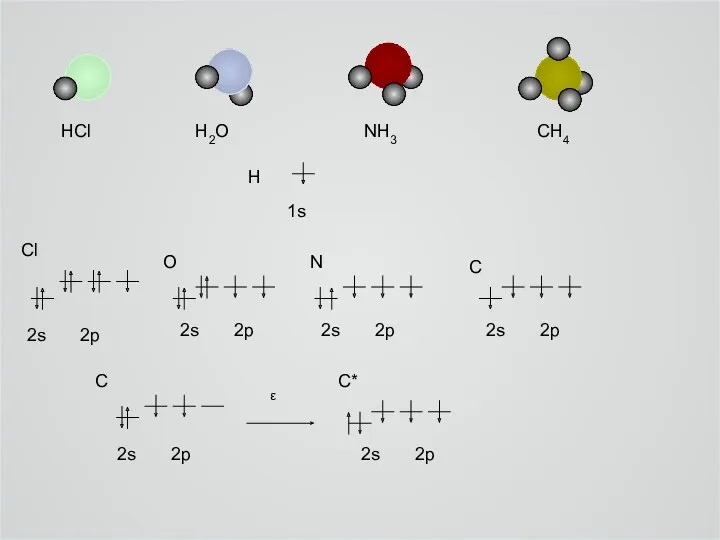
HCl H2O NH3 CH4
Cl
O
N
C
C
C*
2s 2p
2s 2p
2s 2p
2s 2p
2s 2p
2s 2p
H
1s
ε
Слайд 3
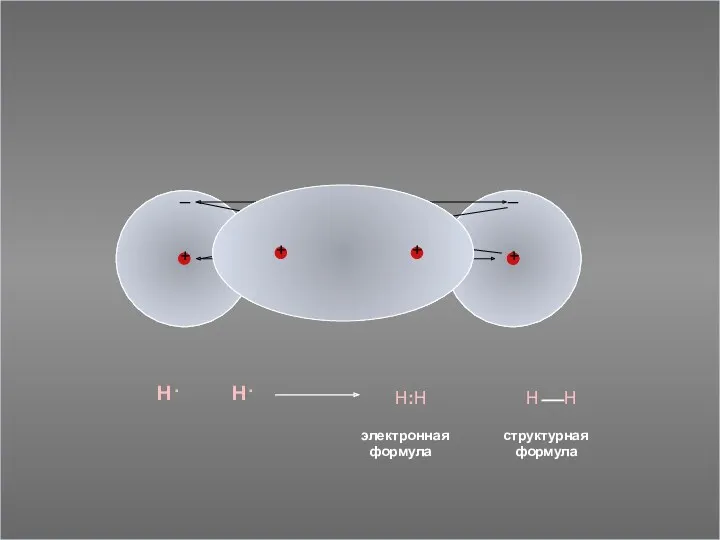
_
_
H:H
электронная
формула
структурная
формула
Слайд 4

На следующем слайде покажем график изменения энергии системы двух атомов при
их сближении.
Слайд 5
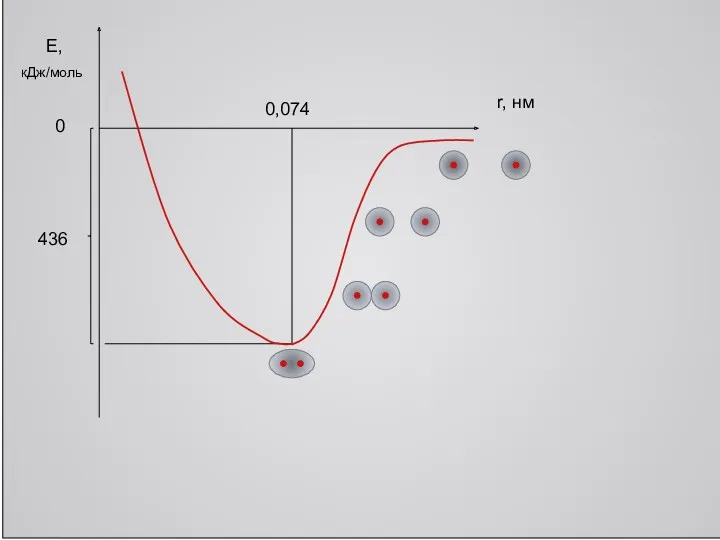
Слайд 6
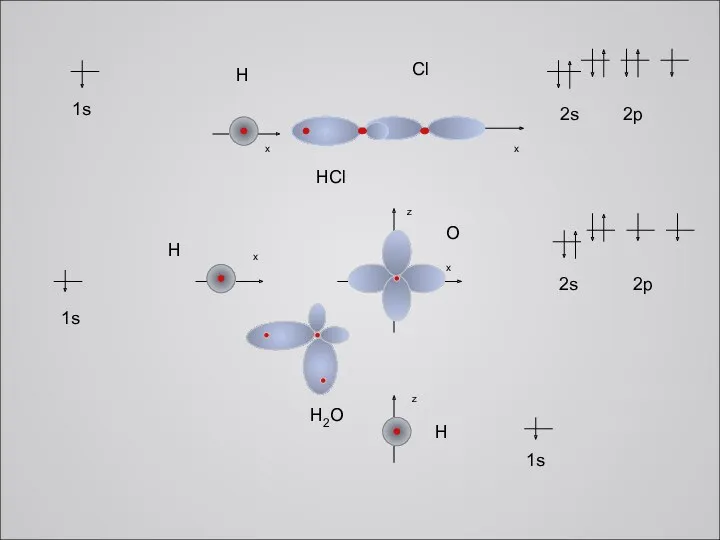
x
x
x
z
H
Cl
z
O
H
H
HCl
H2O
1s
2s 2p
2s 2p
1s
1s
x
Слайд 7
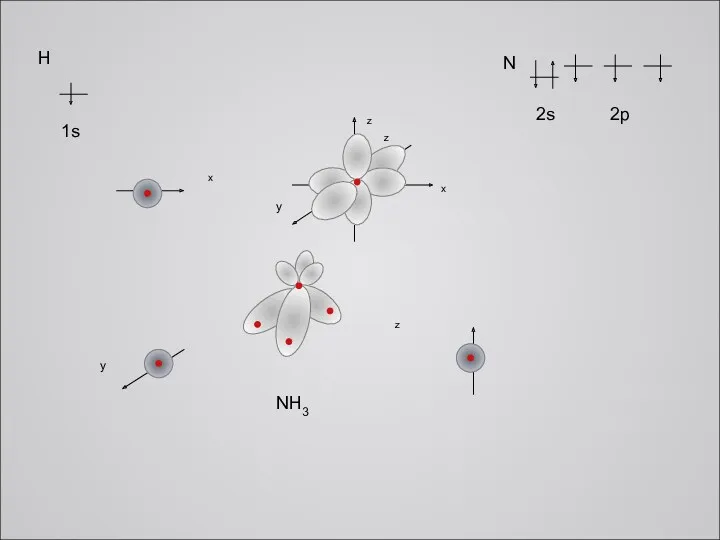
Слайд 8

Теперь решим проблему неспаренных электронов в атоме углерода и образование ковалентных
связей в молекуле метана. Сначала вернёмся к первому слайду и рассмотрим валентную оболочку атома углерода. Затем покажем следующий слайд с моделированием образования ковалентных связей в молекуле СН4.
Слайд 9
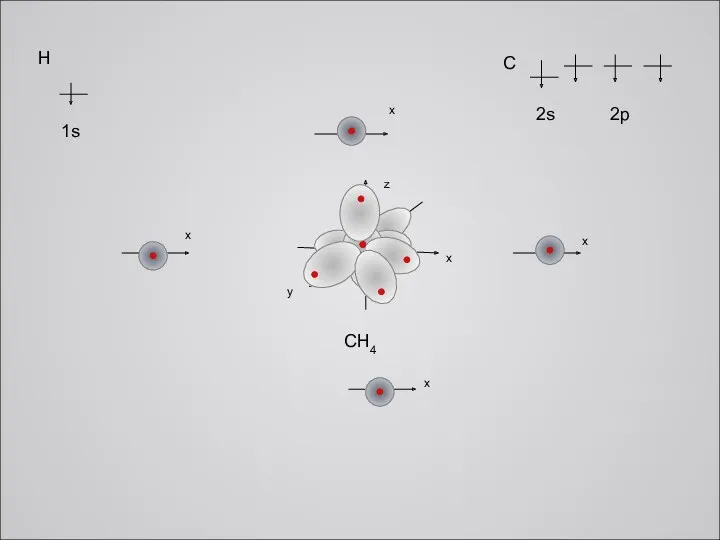
Слайд 10

Поскольку учащиеся в 8 классе не только знакомились, но и пользовались
структурными представлениями на атомно-молекулярном уровне, необходимо их познакомить со структурой молекул на электронном уровне. Применим модель отталкивания электронных пар. Сначала продемонстрируем разнообразие геометрических форм молекул на следующем слайде. Далее рассмотрим электронное представление о геометрии молекул.
Слайд 11
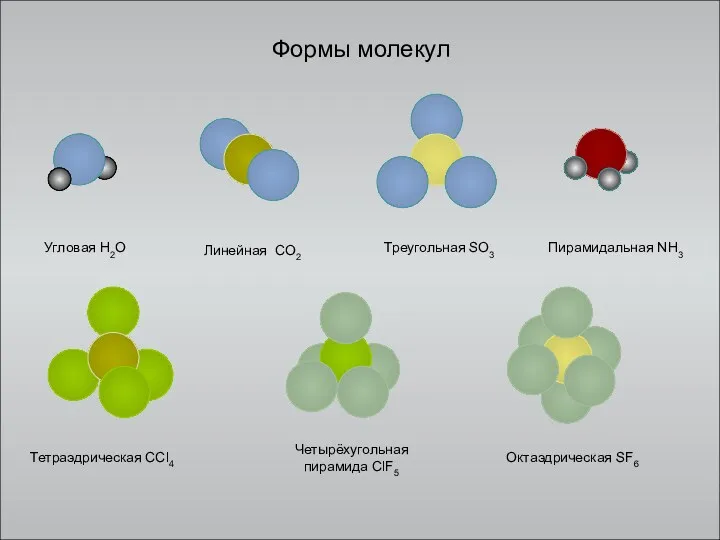
Формы молекул
Угловая H2O
Линейная CO2
Треугольная SO3
Тетраэдрическая CCl4
Четырёхугольная пирамида ClF5
Октаэдрическая SF6
Пирамидальная NH3
Слайд 12
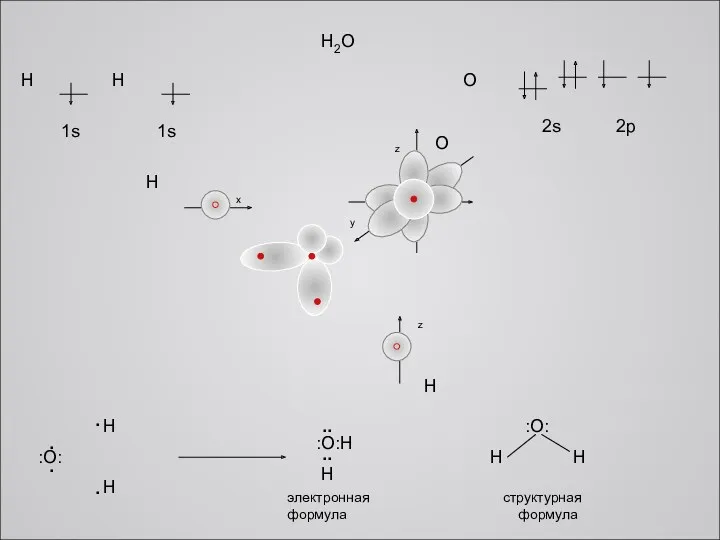
x
x
z
z
O
H
H
H2O
2s 2p
1s
1s
O
H
H
электронная формула
структурная
формула
y
Слайд 13
x
x
z
N
H
2s 2p
1s
y
y
z
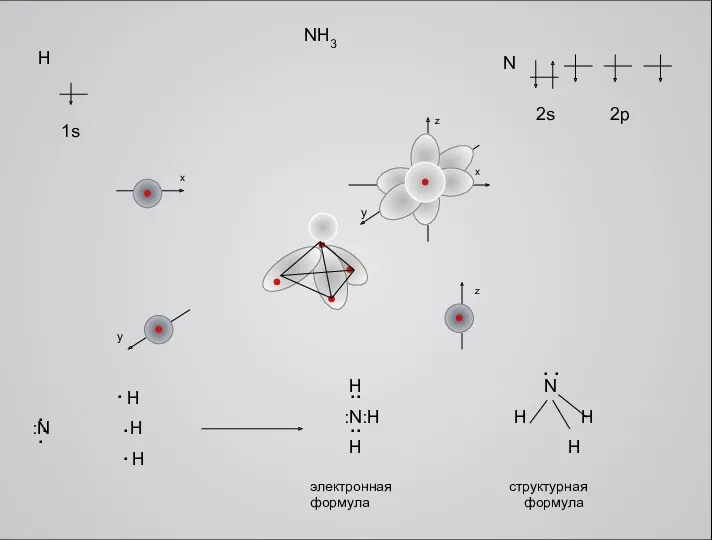
NH3
электронная формула
структурная
формула
Слайд 14
.
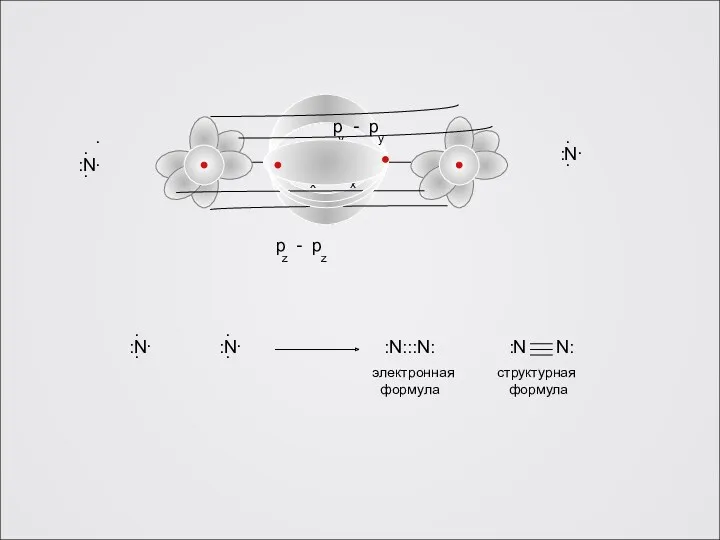
:N:::N:
:N N:
электронная
формула
структурная
формула
Слайд 15
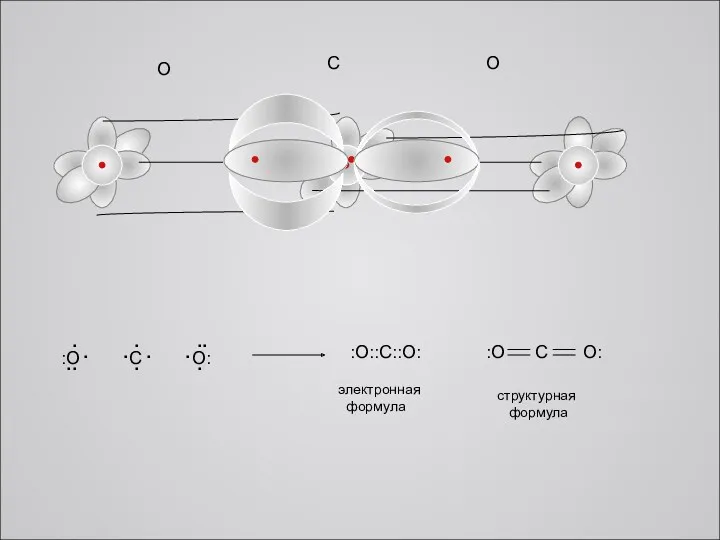
O
C
O
:O::C::O:
электронная
формула
структурная
формула














 Платонов Андрей Платонович (1899 — 1951)
Платонов Андрей Платонович (1899 — 1951) Эксплуатация выключателей
Эксплуатация выключателей Влияние мультфильмов на развитие детей
Влияние мультфильмов на развитие детей Логические основы работы ЭВМ. Лекция 5. Часть 2
Логические основы работы ЭВМ. Лекция 5. Часть 2 20231026_mediaproekt_biografiya_ivana_susanina
20231026_mediaproekt_biografiya_ivana_susanina Рыбы Тульской области
Рыбы Тульской области Проект Эстамп – это здо́рово!
Проект Эстамп – это здо́рово! Ликвидация возможных аварийных ситуаций в резервуарном парке
Ликвидация возможных аварийных ситуаций в резервуарном парке Золотые ворота в Древнюю Русь
Золотые ворота в Древнюю Русь Защита малых рек
Защита малых рек Викторина Олимпийские игры
Викторина Олимпийские игры Организация питания
Организация питания Методика обучения чтению Николая Зайцева. Кубики Зайцева. Презентация для родителей и педагогов.
Методика обучения чтению Николая Зайцева. Кубики Зайцева. Презентация для родителей и педагогов. ПРавила дорожного движения для 1-х классов.
ПРавила дорожного движения для 1-х классов. Марк Твен
Марк Твен Мастер-класс Новогодняя гирлянда
Мастер-класс Новогодняя гирлянда Формирование экологической культуры у детей особой заботы старшего дошкольного возраста
Формирование экологической культуры у детей особой заботы старшего дошкольного возраста Презентация Урок правильного дыхания
Презентация Урок правильного дыхания Нахождение процентов от числа
Нахождение процентов от числа Электронное портфолио
Электронное портфолио Дары Осени
Дары Осени Целостный педагогический процесс
Целостный педагогический процесс Датчики давления
Датчики давления Questions
Questions Заттар алмасуына кіріспе. Заттардың алмасуын оқып үйренуінің тәсілдері. Изотопты тәсілдер
Заттар алмасуына кіріспе. Заттардың алмасуын оқып үйренуінің тәсілдері. Изотопты тәсілдер Цунами, его название. Объяснение этого явления
Цунами, его название. Объяснение этого явления Основное представление об игре баскетбол
Основное представление об игре баскетбол Законодательство Республики Казахстан в области стандартизации, сертификации и лицензирования
Законодательство Республики Казахстан в области стандартизации, сертификации и лицензирования