Содержание
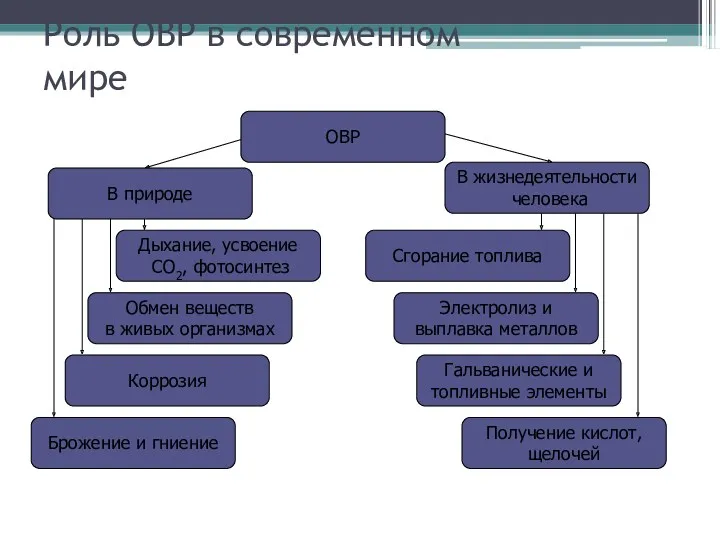
- 2. Роль ОВР в современном мире В природе ОВР В жизнедеятельности человека Дыхание, усвоение CO2, фотосинтез Сгорание
- 3. Расчет степени окисления Следует запомнить: 1. Степени окисления атомов в простых веществах равны нулю: Na0; H20
- 4. Окислительно-восстановительные реакции Реакции, протекающие с изменением степени окисления, называются окислительно-восстановительными реакциями. 0 +2 0 +2 Cu
- 5. Степень окисления (СО) Степень окисления – это условный заряд атома в соединении, вычисленный исходя из предположения,
- 6. Окислитель -Частица (атом, ион), которая в ходе окислительно-восстановительного процесса принимает электроны называется окислителем -Простые вещества -
- 7. Восстановитель Частица (атом, ион), которая в ходе окислительно-восстановительного процесса отдает электроны, называется восстановителем Типичные восстановители
- 8. Окисление-восстановление окисление Окислением называется процесс отдачи атомом, молекулой или ионом электронов. Степень окисления при этом повышается
- 9. Окисление-процесс отдачи электронов 0 +2 Cu – 2 e- = Cu При окислении степень окисления элемента
- 10. +2 0 Hg + 2 e- = Hg При восстановлении степень окисления элемента понижается, а элемент
- 11. Алгоритм расстановки коэффициентов в ОВР методом электронного баланса Запишите схему реакции: C + HNO3 → CO2
- 13. Скачать презентацию









 Наша армия родная
Наша армия родная Computers in our lives
Computers in our lives Идентификация по клавиатурному почерку
Идентификация по клавиатурному почерку Правила техники безопасности во время каникул
Правила техники безопасности во время каникул Общественные финансы. (Тема 6)
Общественные финансы. (Тема 6) Циркуляционные окислительные каналы
Циркуляционные окислительные каналы Дизайн штор.
Дизайн штор. Кризис трех лет
Кризис трех лет Развитие связной речи у детей дошкольного возраста
Развитие связной речи у детей дошкольного возраста Мягкая игрушка. Диванный зайчик
Мягкая игрушка. Диванный зайчик Василий Иванович Белов
Василий Иванович Белов Студенческие работы.
Студенческие работы. исИстория органов внутренних дел Российской Федерации.тория
исИстория органов внутренних дел Российской Федерации.тория Потребности вузов москвы в модернизации в целях повышения доступности высшего образования для лиц с ОВЗ
Потребности вузов москвы в модернизации в целях повышения доступности высшего образования для лиц с ОВЗ Презентация для обобщающего урока- игры по теме Африка 7 класс
Презентация для обобщающего урока- игры по теме Африка 7 класс презентация к уроку по химии Классы неорганических веществ
презентация к уроку по химии Классы неорганических веществ Автоматически реализуемое свойство
Автоматически реализуемое свойство Методика организации детских утренников с использованием элементов казахской народной педагогики
Методика организации детских утренников с использованием элементов казахской народной педагогики 9 мая – День Победы
9 мая – День Победы Торговые весы
Торговые весы Из чего состоит радиоуправляемая автомодель
Из чего состоит радиоуправляемая автомодель Многообразие класса Пресмыкающихся
Многообразие класса Пресмыкающихся Ершалаимские главы в романе Мастер и Маргарита. Понтий Пилат и Иешуа Га-Ноцри. Диалог о добре и зле
Ершалаимские главы в романе Мастер и Маргарита. Понтий Пилат и Иешуа Га-Ноцри. Диалог о добре и зле Адам и Ева и сотворение ангелов
Адам и Ева и сотворение ангелов Занимательная артикуляционная гимнастика Диск
Занимательная артикуляционная гимнастика Диск Портфолио к аттестации
Портфолио к аттестации Презентация Неизвестные герои .
Презентация Неизвестные герои . Следователь. Судмедэксперт
Следователь. Судмедэксперт