Оксиды. Классификация, химические и физические свойства. Определение групп оксидов. Получение оксидов презентация
Содержание
- 2. Что такое оксиды? Оксиды – это сложные вещества, состоящие из двух химических элементов, один из которых
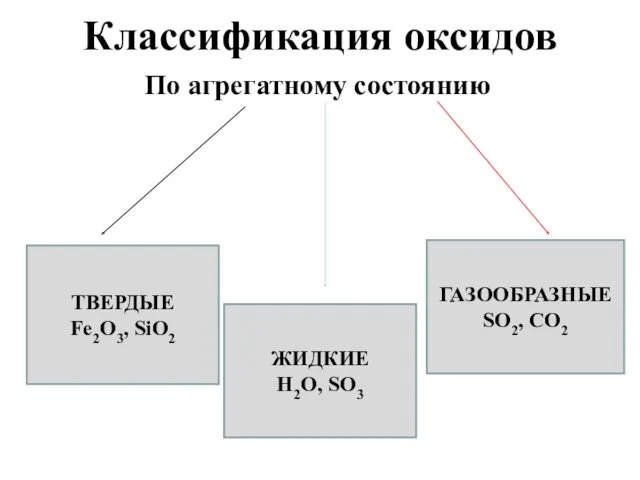
- 3. Классификация оксидов По агрегатному состоянию ТВЕРДЫЕ Fe2O3, SiO2 ЖИДКИЕ Н2О, SO3 ГАЗООБРАЗНЫЕ SO2, CO2
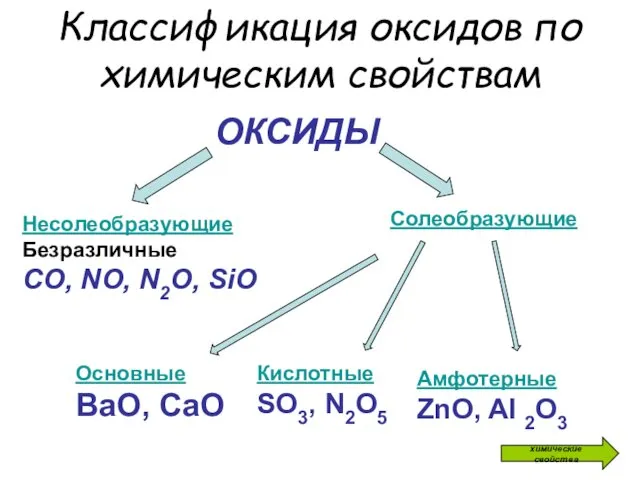
- 4. Классификация оксидов по химическим свойствам ОКСИДЫ Несолеобразующие Безразличные СО, NO, N2O, SiO Солеобразующие Основные ВаО, СаО
- 5. Классификация оксидов Несолеобразующие оксиды – такие оксиды, которые не взаимодействуют ни с кислотами, ни с щелочами
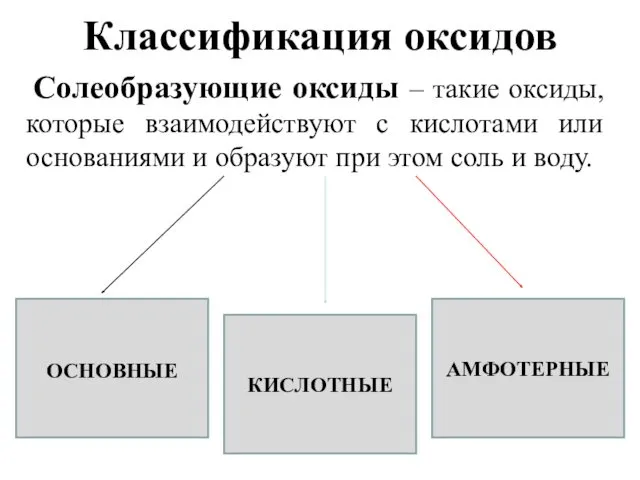
- 6. Классификация оксидов Солеобразующие оксиды – такие оксиды, которые взаимодействуют с кислотами или основаниями и образуют при
- 7. ОПРЕДЕЛЕНИЕ ГРУПП ОКСИДОВ Основными называются оксиды, которые образуют соли при взаимодействии с кислотами или кислотными оксидами.
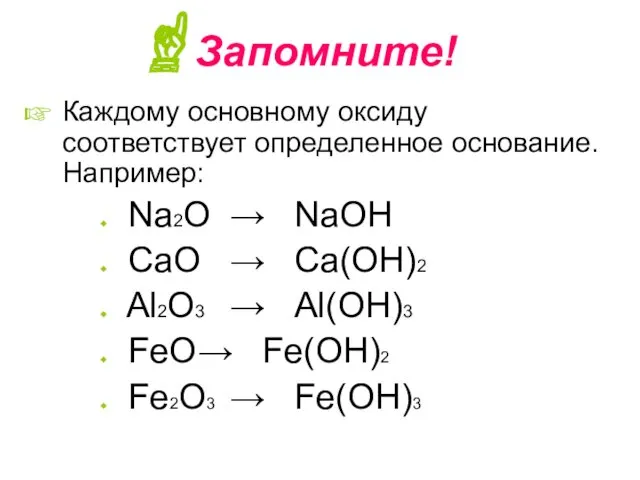
- 8. Запомните! Каждому основному оксиду соответствует определенное основание. Например: Na2O → NaOH CaO → Ca(OH)2 Al2O3 →
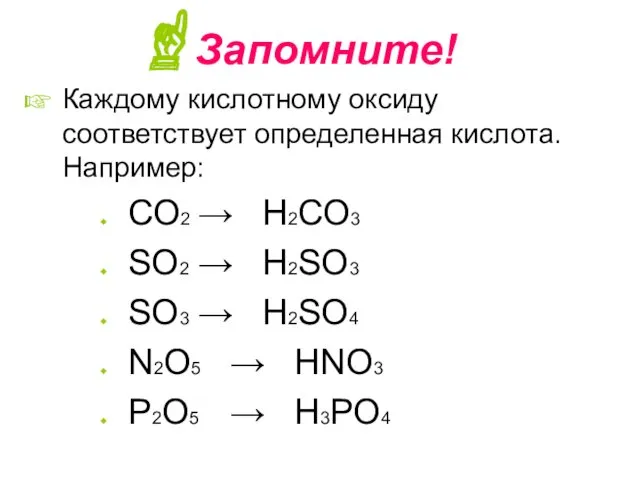
- 9. Запомните! Каждому кислотному оксиду соответствует определенная кислота. Например: СО2 → Н2СО3 SО2 → H2SО3 SО3 →
- 10. Типичные реакции основных оксидов 1) Основной оксид + кислота = соль + вода 2) Основной оксид
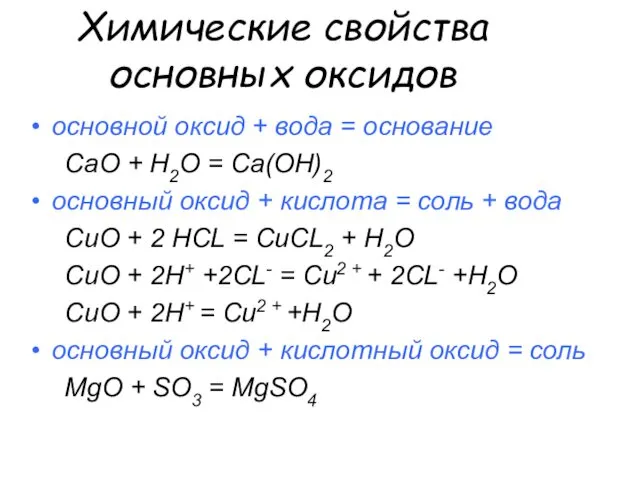
- 11. Химические свойства основных оксидов основной оксид + вода = основание СаO + H2O = Са(OН)2 основный
- 12. Типичные реакции кислотных оксидов 1) Кислотный оксид + основание = соль + вода 2) Кислотный оксид
- 13. Химические свойства кислотных оксидов кислотный оксид + вода = кислота Р2O5 + 3H2O = 2H3РO4 кислотный
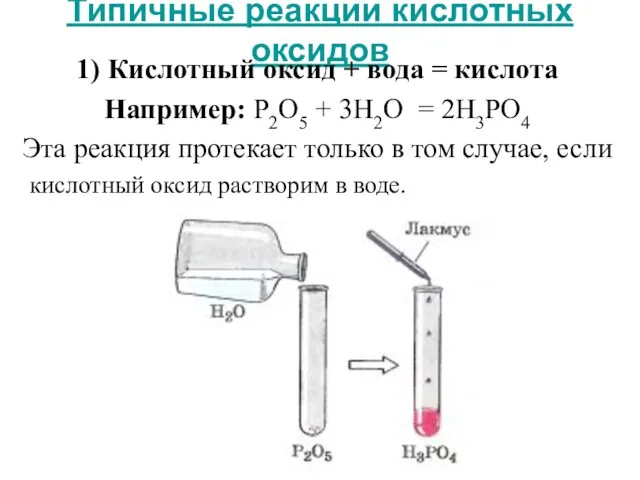
- 14. Типичные реакции кислотных оксидов 1) Кислотный оксид + вода = кислота Например: P2O5 + 3H2O =
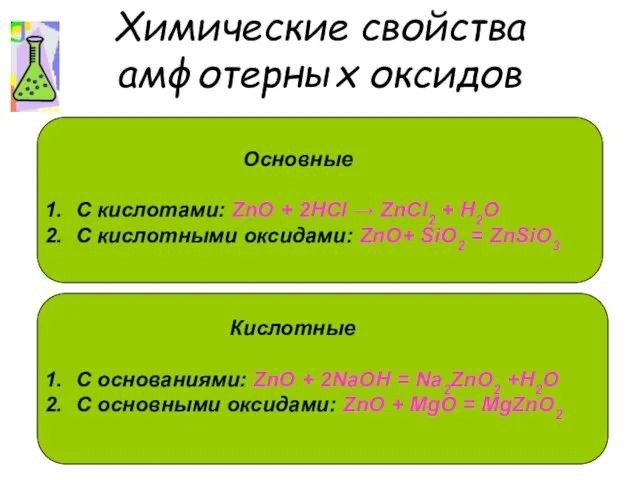
- 15. Химические свойства амфотерных оксидов Основные С кислотами: ZnO + 2НСl → ZnСl2 + Н2О С кислотными
- 16. Получение оксидов
- 17. 1 способ: окисление металлов где CuO – оксид меди (II) Способы получения оксидов
- 18. 2 способ: окисление неметаллов где CO2 – оксид углерода (IV) Способы получения оксидов
- 19. 3 способ: разложение кислот где - сернистая кислота, SO2 – оксид серы (IV) Способы получения оксидов
- 20. 4 способ: разложение солей где - карбонат кальция CаO – оксид кальция (II) Способы получения оксидов
- 21. 5 способ: разложение нерастворимых оснований где - гидроксид железа (II), FeO – оксид железа (II) Способы
- 22. 6 способ: вытеснение из солей другими оксидами где - карбонат натрия, SiO2 – оксид кремния (IV),
- 23. 7 способ: горение сложных веществ где - этанол (этиловый спирт), СO2 – оксид углерода (IV) Способы
- 24. Обобщение темы: Тест: «Правильный ответ» 1) Какой из оксидов несолеобразующий: а) а) P2O5 б) б) NO
- 25. Наша лаборатория получила заказ на получение оксидов из следующих веществ: а) серыа) серы; б) фосфораа) серы;
- 26. Был найден листок, но записи на нем частично исчезли, необходимо восстановить их. C + ? =
- 27. В нашу лабораторию пришло ещё одно письмо: Здравствуйте, здравствуйте! Не могли бы вы мне ответить на
- 28. Самостоятельная работа Напишите уравнения реакций химических свойств следующих оксидов:
- 30. Скачать презентацию



















 Нации и межнациональные отношения
Нации и межнациональные отношения ФГТ
ФГТ Формирование народов
Формирование народов Методика повышения технической подготовленности футболистов старшего школьного возраста
Методика повышения технической подготовленности футболистов старшего школьного возраста 20231112_prezentatsiya_srednevekovaya_arhitektura_bolgarii_1_1
20231112_prezentatsiya_srednevekovaya_arhitektura_bolgarii_1_1 Мастер-класс Формирование действия моделирования через решение текстовых задач
Мастер-класс Формирование действия моделирования через решение текстовых задач Восстание декабристов
Восстание декабристов БД_22_Лекция12
БД_22_Лекция12 ВИКТОРИНА ДЛЯ НАСТОЯЩИХ И БУДУЩИХ УЧИТЕЛЕЙ
ВИКТОРИНА ДЛЯ НАСТОЯЩИХ И БУДУЩИХ УЧИТЕЛЕЙ Урок химии в 10 кл.Генетическая связь УВ и кислородсодержащих орг. соединений
Урок химии в 10 кл.Генетическая связь УВ и кислородсодержащих орг. соединений Педпагогиканың класссгі К.Д. Ушинскийдің мұраларындағы халықтық тәрбие мәселелері
Педпагогиканың класссгі К.Д. Ушинскийдің мұраларындағы халықтық тәрбие мәселелері Типология современного урока
Типология современного урока Загрузка изображений
Загрузка изображений Зависть
Зависть Дім моєї мрії
Дім моєї мрії Стихи со звуками
Стихи со звуками Обработка нижнего среза сорочки швом вподгибку с закрытым срезом
Обработка нижнего среза сорочки швом вподгибку с закрытым срезом Книга Памяти учащихся 3 - а класса Диск
Книга Памяти учащихся 3 - а класса Диск Разрезы. Особые случаи разрезов
Разрезы. Особые случаи разрезов Презентация к занятию по театрализованной деятельности в старшей группе ДОУ Эмоции и мимика
Презентация к занятию по театрализованной деятельности в старшей группе ДОУ Эмоции и мимика Emotions
Emotions Презентация:Использования ИКТ для формирования открытого информационного пространства ДОУ
Презентация:Использования ИКТ для формирования открытого информационного пространства ДОУ В кругу семьи.
В кругу семьи. Аппаратные средства вычислительной техники. (Лекция 1)
Аппаратные средства вычислительной техники. (Лекция 1) Определение времени возведения ограждающей крепи котлована выполненной способом Стена в грунте
Определение времени возведения ограждающей крепи котлована выполненной способом Стена в грунте Иудаизм. Монотеистическая национальная религия евреев
Иудаизм. Монотеистическая национальная религия евреев Эссе на тему: Моё педагогическое кредо: смыслы, ценности, приоритеты
Эссе на тему: Моё педагогическое кредо: смыслы, ценности, приоритеты Обмен белков-4
Обмен белков-4