Определение массовой концентрации общего железа с сульфосалициловой кислотой. (Лабораторная работа 2) презентация
Содержание
- 2. Гаврилова Таисия Германовна Цицилина Дарья Михайловна 8:30 – 11:35 11:20 уборка рабочего места Сдача долгов: 18
- 3. Содержание 1. Цель работы 2. Характеристика объектов исследования 3. Приборы (оборудование) и материалы 4. Порядок выполнения
- 4. 1 Цель работы 1.1 Ознакомиться с ГОСТом 4011-72 «Измерение массовой концентрации общего железа с сульфосалициловой кислотой».
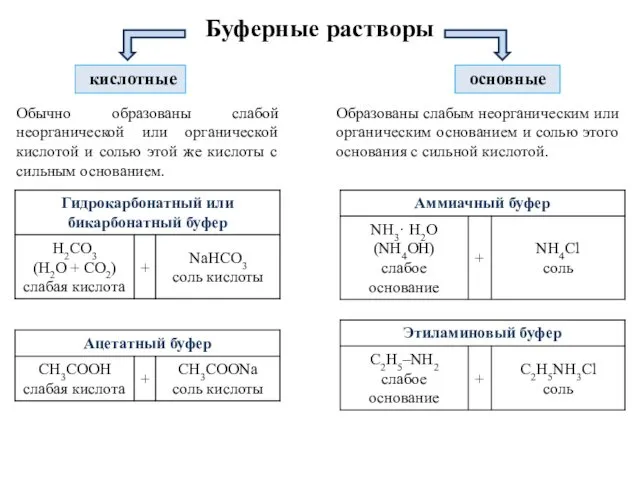
- 5. Буферные растворы Многие реакции в растворе протекают в нужном направлении только при определенной концентрации ионов Н+.
- 6. основные Буферные растворы кислотные Обычно образованы слабой неорганической или органической кислотой и солью этой же кислоты
- 7. Сущность метода Метод основан на взаимодействии ионов железа в щелочной среде с сульфосалициловой кислотой с образованием
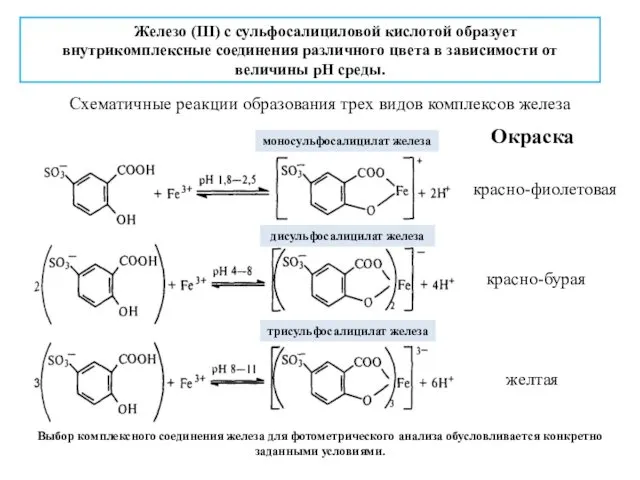
- 8. Железо (III) с сульфосалициловой кислотой образует внутрикомплексные соединения различного цвета в зависимости от величины рН среды.
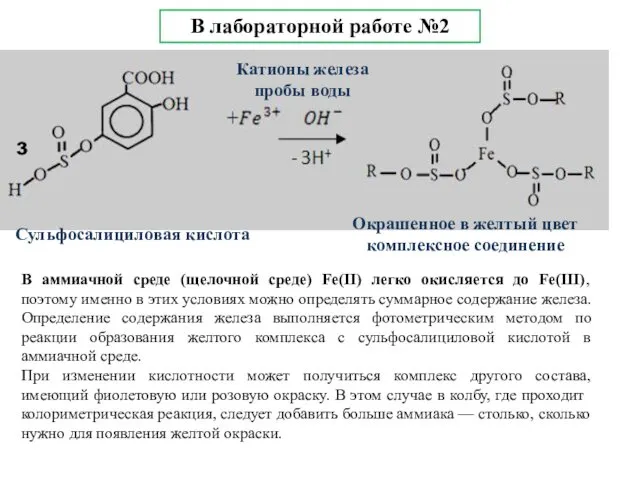
- 9. В аммиачной среде (щелочной среде) Fe(II) легко окисляется до Fe(III), поэтому именно в этих условиях можно
- 10. Измерение оптической плотности окрашенных растворов (D) проводится на спектрофотометре ЮНИКО 1201, при длине волны (λ) равной
- 11. 2 Характеристика объектов исследования Объектом исследования в данной работе являются пробы воды, отобранной …
- 12. 3 Оборудование и материалы - спектрофотометр ЮНИКО 1201; - кюветы толщиной оптического слоя 3 см; -
- 13. 4 Порядок выполнения работы Приготовьте две параллельные пробы воды, используя следующую методику: При массовой концентрации железа
- 14. 4.2 Пробу воды нагреть до кипения и упарить до объема 35-40 мл. Раствор охлаждать до комнатной
- 15. 4.4 4.5 По индикаторной бумаге определить значение рН раствора, которое должно быть ≥ 9. Если рН
- 16. 4.6 4.7 4.8 Измерить оптическую плотность окрашенных растворов, использую фиолетовый светофильтр (λ = 400 нм) и
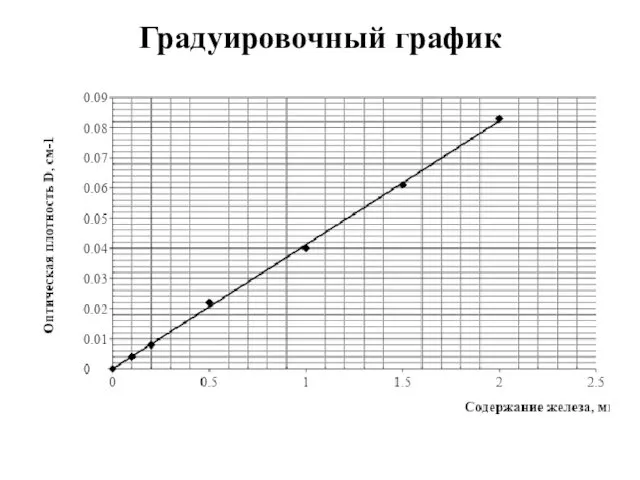
- 17. Градуировочный график
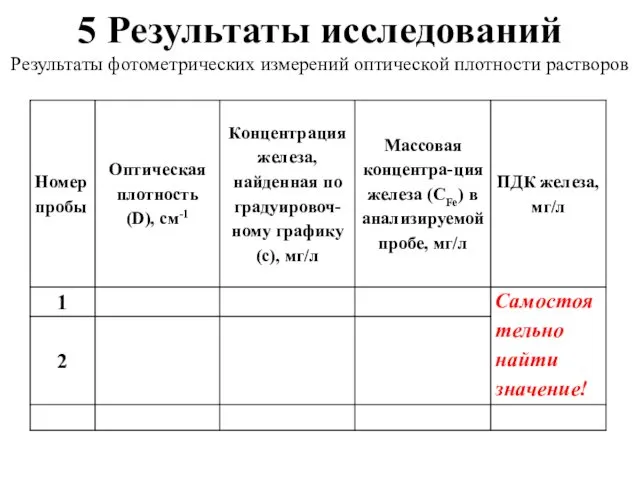
- 18. 5 Результаты исследований Результаты фотометрических измерений оптической плотности растворов
- 19. Расчеты 1. Массовую концентрацию железа (СFe, мг/л) в анализируемой пробе вычислить по формуле: c - концентрация
- 20. 2. Оценить сходимость результатов анализа (А) в процентах по формуле: Р1 – больший результат из двух
- 21. За окончательный результат анализа принимают среднее арифметическое результатов двух параллельных измерений, допустимое расхождение между которыми не
- 22. Выводы 1. Освоен оптический метод определения общего железа в воде с сульфасалициловой кислотой. 2. Концентрация общего
- 23. 1. Как наличие железа влияет на качество воды? Способы устранение содержания железа. 2. Уравнения реакций, протекающих
- 24. План характеристики элемента 1. Положение в периодической системе химических элементов (порядковый номер, атомная масса, период, группа,
- 26. Скачать презентацию


















 Психология развития
Психология развития Диверсификация производств и интеграция строительных организаций
Диверсификация производств и интеграция строительных организаций Стоп-кадр
Стоп-кадр Устройство компьютера. Системный блок
Устройство компьютера. Системный блок Устройство рулевого управления
Устройство рулевого управления Презентация к уроку Роль гидросферы в жизни Земли часть1 7 класс
Презентация к уроку Роль гидросферы в жизни Земли часть1 7 класс Шаблоны презентаций Тетрадь на спирали. Часть 1
Шаблоны презентаций Тетрадь на спирали. Часть 1 координатная прямая
координатная прямая геодистант 6 класс Мир карт
геодистант 6 класс Мир карт Мир информатики. Ответы, решения, разъяснения к заданиям. (Часть 1)
Мир информатики. Ответы, решения, разъяснения к заданиям. (Часть 1) Успехи в освоении технологии за 6 класс
Успехи в освоении технологии за 6 класс Основы латинского языка с медицинской терминологией. Названия растений
Основы латинского языка с медицинской терминологией. Названия растений Конкурс инновационных проектов
Конкурс инновационных проектов День знаний
День знаний Шаблон для презентации 1 октября - День добра и уважения
Шаблон для презентации 1 октября - День добра и уважения Несеп-жыныс жүйесінiң туберкулезі
Несеп-жыныс жүйесінiң туберкулезі Город мастеров кисти и резца часть 1 Диск
Город мастеров кисти и резца часть 1 Диск Правила создания презентации к дипломным и курсовым работам
Правила создания презентации к дипломным и курсовым работам Решение задач. Параллелограмм (8кл)
Решение задач. Параллелограмм (8кл) Декор учебно-опытного участка как средство формирования экологических представлений дошкольников
Декор учебно-опытного участка как средство формирования экологических представлений дошкольников Как помочь заикающимся школьникам
Как помочь заикающимся школьникам Презентация Дорога жизни.
Презентация Дорога жизни. Родительское собрание Права и обязанности
Родительское собрание Права и обязанности Отчет о выполнении работ по благоустройству общественной территории. Вельский район деревня Никифорово
Отчет о выполнении работ по благоустройству общественной территории. Вельский район деревня Никифорово Империя Наполеона. Урок 9
Империя Наполеона. Урок 9 Процессоры
Процессоры Экологические основы природопользования. Лимитирующий фактор. Закон минимума. Бочка Либиха. Факторы влияющие на организм
Экологические основы природопользования. Лимитирующий фактор. Закон минимума. Бочка Либиха. Факторы влияющие на организм технологии муз. воспитания
технологии муз. воспитания