Содержание
- 2. Определение «Опухоль – патологическая и избыточная масса ткани, рост которой нескоординирован, превышает таковой в нормальных тканях
- 3. Этиология опухолей (бластомогенные факторы) Химические канцерогены (асбест, табак) – вызывают 75% всех злокачественных опухолей Физические канцерогены
- 4. Условия возникновения Наследственные факторы Низкая активность механизмов противоопухолевой активности Географические факторы Пол Возраст Хронические заболевания
- 6. Структура опухоли Паренхима (опухолевые клетки) Строма (соединительная ткань + сосуды + клетки воспалительного инфильтрата организма-хозяина) Паренхиматозные
- 7. Характерные морфологические изменения опухолевых клеток: Полиморфизм опухолевых клеток и их ядер – характерна выраженная вариабельность по
- 8. 3) Митозы – отмечается большое количество митозов, что связано с высокой пролиферативной активностью клеток. Характерно обнаружение
- 10. Номенклатура опухолей I. Паренхима представлена одним типом клеток (опухоли мезенхимального происхождения, производные эндотелиальных и связанных с
- 11. В клинической практике используется классификация злокачественных опухолей по системе TNM T (tumor) – характеризует распространение первичной
- 12. Доброкачественная опухоль Локализованная Не распространяется на другие участки Поддается местному хирургическому удалению Не приводит к смерти
- 14. Злокачественная опухоль (раковая, рак, лат. cancer – рак, краб) Способна инфильтрировать любые ткани (врастать в них)
- 15. Сравнительная характеристика доброкачественных и злокачественных опухолей
- 16. Темп роста опухоли Исходная трансформированная клетка (диаметр =10 мкм) и ее производные должны пройти путь по
- 17. Хроническое воспаление и опухоли
- 18. Предопухолевые состояния Хронический атрофический гастрит, солнечный кератоз кожи, хронический язвенный колит, а также лейкоплакия полости рта,
- 19. Молекулярные основы канцерогенеза
- 20. Основные принципы канцерогенеза нелетальное повреждение генома клетки является ключевым событием канцерогенеза; опухоль формируется из одной клетки-предшественника,
- 23. Основные изменения в физиологии опухолевой клетки: 1) автономность роста. Опухоль обладает свойством пролиферировать без внешних стимулов,
- 24. Основные изменения в физиологии опухолевой клетки: 4) безграничный потенциал репликации. Опухолевые клетки имеют способность к неограниченной
- 25. Основные изменения в физиологии опухолевой клетки: 6) способность к инвазии и метастазированию. Метастазирование опухолей — основная
- 26. Проявления атипизма опухолевых клеток Атипизм размножения — бесконтрольное деление опухолевых клеток. н е р е г
- 27. Проявления атипизма опухолевых клеток Атипизм дифференцировки заключается в частичном или полном ингибировании процесса созревания клеток. Он
- 28. Проявления атипизма опухолевых клеток Метаболический и энергетический атипизмы и н т е н с и в
- 29. Проявления атипизма опухолевых клеток Физико-химический атипизм проявляется увеличением содержания в опухолевых клетках воды, ионов калия и
- 30. Проявления атипизма опухолевых клеток Функциональный атипизм а) снижение, например, секреции желудочного сока при раке желудка, образования
- 31. Проявления атипизма опухолевых клеток Антигенный атипизм состоит в разнонаправленных изменениях антигенного состава опухолевых клеток — антигенном
- 32. Проявления атипизма опухолевых клеток Морфологический атипизм: тканевый и клеточный. Т к а н е в ы
- 33. Проявления атипизма опухолевых клеток Атипизм взаимодействия клеток опухоли с организмом заключается в том, что в отличие
- 34. Пути метастазирования • Лимфогенный - наиболее частый путь метастазирования опухолей, особенно карцином. • Гематогенный путь наиболее
- 35. Стадии метастазирования и н в а з и и — миграция опухолевых клеток в просвет сосудов.
- 37. Рецидивирование (от лат. recidivas — возврат; повторное развитие болезни). Причинами рецидивов являются: а) неполное удаление опухолевых
- 39. Онкогены Гены, обеспечивающие автономный рост опухолевых клеток, называют онкогенами, а их клеточные предшественники — протоонкогенами. Продукты
- 40. Протооногены: биологическая роль Деятельность протоонкогенов регулируется генами-онкосупрессорами. При мутациях и нарушениях регуляции в этих генах происходит
- 41. Продукты онкогенов: биохимические функции
- 42. p53 – страж генома Около 80% точечных мутаций, обнаруженных в злокачественных опухолях человека, располагаются в домене
- 43. Онкоген RAS RAS – семейство генов, кодирующих маленькие мембраносвязанные G-белки, функции которых - передача сигнала, регулирование
- 44. Онкоген RAS
- 45. Изменения нерецепторных тирозинкиназ Тирозинкиназы функционируют в сигнальных путях, регулируют рост клеток. При их чрезмерном синтезе происходит
- 46. Ядерные онкогены В семейство ядерных онкогенов входят гены jun, fos, myc, myb и erb А. Онкопротеины,
- 47. Циклины и циклин-зависимые киназы
- 48. Химический канцерогенез Проканцерогены сами по себе не вызывают опухоль. Но трансформируются в организме в истинные (конечные)
- 49. Инициаторы – высокореактивные электрофильные вещества, их мишени ДНК, РНК и белки. Вызывают нелетальные повреждения ДНК, поэтому
- 50. Химические канцерогены Генотоксические: прямые и непрямые. Негенотоксические обычно выступают промоторами (пестициды, гормоны). Способны вызвать оксидативный стресс,
- 51. Генотоксические химические канцерогены Прямые канцерогены – химические агенты, которым для реализации канцерогенного эффекта не нужно метаболическое
- 52. Молекулярные мишени химических канцерогенов Основная мишень – ДНК Обычно мутации происходят в онкогенах и генах-супрессорах опухолей
- 53. Вирусный канцерогенез ДНК-вирусы (внедряются в ДНК клетки) Вирус Эпштейна-Барр (лимфомы) Вирусы гепатита B, C (гепатокарциномы) Вирус
- 54. Этапы вирусного канцерогенеза Проникновение онкогенного вируса в клетку Включение вирусного онкогена в геном клетки Экспрессия онкогена
- 55. H.pylori Причина развития аденокарцином и лимфом желудка (3% инфицированных) H.pylori на фоне хронического воспаления усиливает пролиферацию
- 56. Радиационный канцерогенез УФ лучи Ионизирующее излучение
- 57. Ультрафиолетовые лучи Степень риска зависит от типа УФ-лучей, интенсивности и длительности экспозиции, от количества меланина. Три
- 58. Ионизирующая радиация Все виды электромагнитного излучения оказывают канцерогенное действие. Наиболее часто развиваются: Острая и хроническая миелоидная
- 59. Антибластомная резистентность организма Наличие причины опухолей и даже включение механизмов канцерогенеза сами по себе еще недостаточны
- 60. Антибластомная резистентность организма Механизмы антибластомной резистентности: А н т и к а н ц е р
- 61. Антиканцерогенные механизмы Против химических канцерогенов: 1) реакции инактивации канцерогенов (окислительно-восстановительные и конъюгационные) 2) элиминация экзо- и
- 62. Антиканцерогенные механизмы Против биологических этиологических факторов: 1) ингибирование онкогенных вирусов интерферонами; 2) нейтрализация онкогенных вирусов специфическими
- 63. Антиканцерогенные механизмы Против физических канцерогенных факторов: реакции торможения образования и инактивации свободных радикалов (антирадикальные реакции) и
- 64. Антитрансформационные механизмы 1) антимутационные механизмы, являющиеся функцией клеточных ферментных систем репарации ДНК, устраняющих повреждения, ошибки ДНК
- 65. Антицеллюлярные механизмы Эти механизмы включаются с момента образования первых бластомных клеток. Они направлены на ингибирование и
- 66. Противоопухолевая защита организма и почему она бывает неэффективной Две линии противоопухолевой защиты. Первая линия защиты направлена
- 67. Противоопухолевый иммунитет Теория иммунного надзора подразумевает, что нормальная функция иммунной системы заключается в распознавании и разрушении
- 68. Противоопухолевые эффекторные механизмы Клеточный иммунитет — доминирующий механизм противоопухолевой защиты в естественных условиях. Эффекторные клетки иммунной
- 70. ПРОТИВООПУХОЛЕВАЯ ИММУННАЯ ЗАЩИТА Противоопухолевая иммунная защита основана на том что, на поверхности раковых клеток содержатся специфические
- 71. 1. TSA-специфичные антитела могут ограничивать опухолевый рост Зависимая от антител клеточно-опосредуемая цитотоксичность (antibody-dependent cell-mediated cytotoxicity, ADCC)
- 72. Уклонение раковых клеток от иммунобиологического надзора
- 74. Клинические проявления патогенного действия опухоли на организм Патогенное действие опухоли проявляется в следующих клинических симптомах и
- 75. СИНДРОМ КАХЕКСИИ Изменение белкового, липидного, углеводного обмена Астения (значительная слабость) Анорексия (потеря аппетита) Плохая работоспособность Ранние
- 76. Кахексия (от греч. kakos — плохой, дурной + hexis — состояние) — синдром истощения и общей
- 77. Паранеопластические синдромы У 10% пациентов со злокачественными опухолями наблюдаются симптомокомплексы, развитие которых невозможно объяснить локальным или
- 78. Паранеопластические синдромы важно диагностировать по следующим причинам: - могут быть ранней манифестацией бессимптомной опухоли; - обусловливают
- 80. Скачать презентацию
 Полуавтоматическая сварка в среде защитного газа
Полуавтоматическая сварка в среде защитного газа Иммунология на службе здоровья человека. Вакцина и сыворотка
Иммунология на службе здоровья человека. Вакцина и сыворотка Вижу, слышу, ощущаю... (индивидуальные особенности детей и их учёт при организации работы с дошкольниками)
Вижу, слышу, ощущаю... (индивидуальные особенности детей и их учёт при организации работы с дошкольниками) Бароко
Бароко Хирургическая анатомия пж и желчных протоков
Хирургическая анатомия пж и желчных протоков Ярмарка
Ярмарка Объектно-ориентированное программирование. IT-школа
Объектно-ориентированное программирование. IT-школа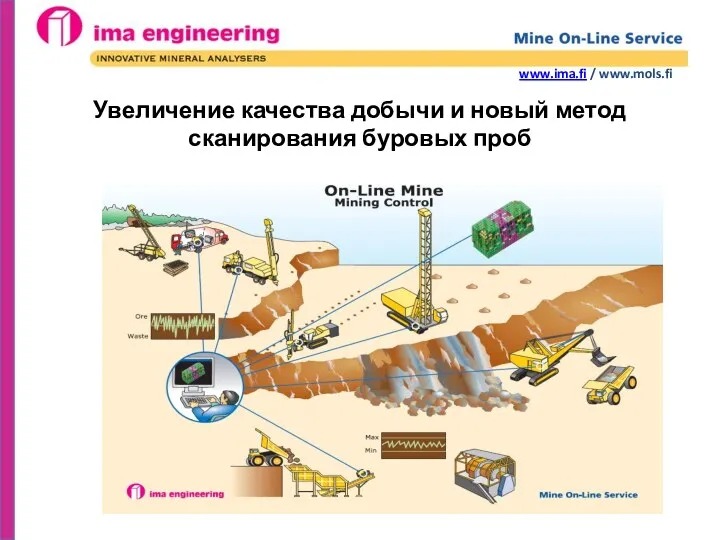 IMA Engineering. Увеличение качества добычи руды и новый метод сканирования буровых проб
IMA Engineering. Увеличение качества добычи руды и новый метод сканирования буровых проб Правильные многогранники
Правильные многогранники Шустрый Зайчик
Шустрый Зайчик Аккумулятор мобильного телефона
Аккумулятор мобильного телефона Банки и банковская система Республики Беларусь
Банки и банковская система Республики Беларусь Звездный час
Звездный час Соединенные Штаты Америки
Соединенные Штаты Америки Виды рабочей одежды. Снятие мерок
Виды рабочей одежды. Снятие мерок Эмоционально-волевая сфера слепых и слабовидящих
Эмоционально-волевая сфера слепых и слабовидящих Ведение буровзрывных работ на горизонте Южной залежи
Ведение буровзрывных работ на горизонте Южной залежи Ақуызды алғаш (клейковина тәрізді) 1728 ж. итальяндық ғалым Якопо Бартоломео Беккари (1682-1766) бидай ұнынан бөліп алған
Ақуызды алғаш (клейковина тәрізді) 1728 ж. итальяндық ғалым Якопо Бартоломео Беккари (1682-1766) бидай ұнынан бөліп алған Между надо и хочу
Между надо и хочу команда г. Железногорск Алгоритм квест-игры
команда г. Железногорск Алгоритм квест-игры Пологові травми спинного мозку та плечового сплетіння
Пологові травми спинного мозку та плечового сплетіння Автоматизация звука Ж в играх
Автоматизация звука Ж в играх КОМПЬЮТЕРНАЯ ПРЕЗЕНТАЦИЯ ПО ГЕОГРАФИИ Лесной комплекс Россииии 9 КЛАСС
КОМПЬЮТЕРНАЯ ПРЕЗЕНТАЦИЯ ПО ГЕОГРАФИИ Лесной комплекс Россииии 9 КЛАСС Біблія. Все про Біблію
Біблія. Все про Біблію Программирование линейных алгоритмов. Начала программирования
Программирование линейных алгоритмов. Начала программирования Краски Преображения в Лете Господнем
Краски Преображения в Лете Господнем презентация Давайте учиться друг у друга!
презентация Давайте учиться друг у друга! Презентация: Анализ содержания КИМ для проведения пробного экзамена по химии в 2013 году.
Презентация: Анализ содержания КИМ для проведения пробного экзамена по химии в 2013 году.