Содержание
- 2. Скорость ферментативной реакции Скорость ферментативной реакции определяется изменением количества молекул субстрата или продукта за единицу времени.
- 3. Скорость ферментативной реакции На начальном этапе [0 - t0] скорость реакции прямо пропорциональна времени и имеет
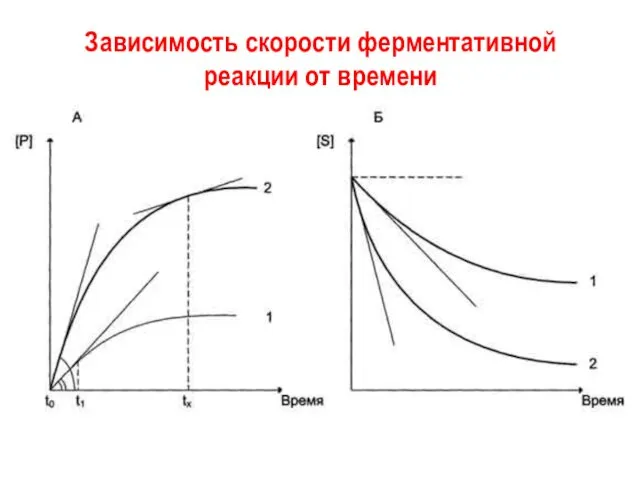
- 4. Зависимость скорости ферментативной реакции от времени
- 5. Скорость ферментативной реакции Скорость ферментативной реакции зависит от ряда факторов, таких как: количество и активность ферментов,
- 6. Зависимость скорости ферментативной реакции от концентрации фермента При проведении ферментативной реакции в условиях избытка субстрата скорость
- 7. Зависимость скорости ферментативной реакции от концентрации фермента Однако количество фермента часто невозможно определить в абсолютных величинах,
- 8. Зависимость скорости ферментативной реакции от концентрации фермента В 1973 г. была принята новая единица активности ферментов:
- 9. Зависимость скорости ферментативной реакции от температуры Повышение температуры до определённых пределов увеличивает скорость ферментативной: С повышением
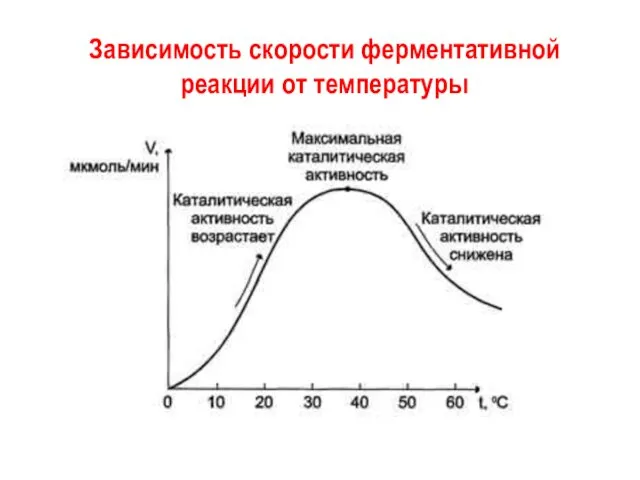
- 10. Зависимость скорости ферментативной реакции от температуры Зависимость скорости ферментативной реакции от температуры
- 11. Зависимость скорости ферментативной реакции от рН Для каждого фермента существует значение рН, при котором наблюдается его
- 12. Зависимость скорости ферментативной реакции от рН При закислении среды происходит протонирование свободных аминогрупп (NH3+), а при
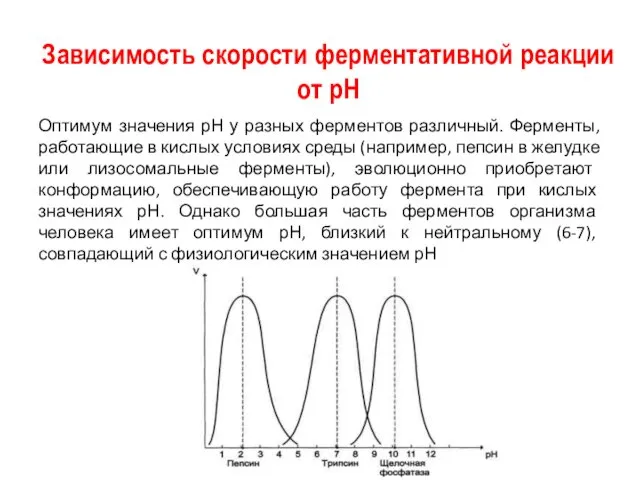
- 13. Зависимость скорости ферментативной реакции от рН Оптимум значения рН у разных ферментов различный. Ферменты, работающие в
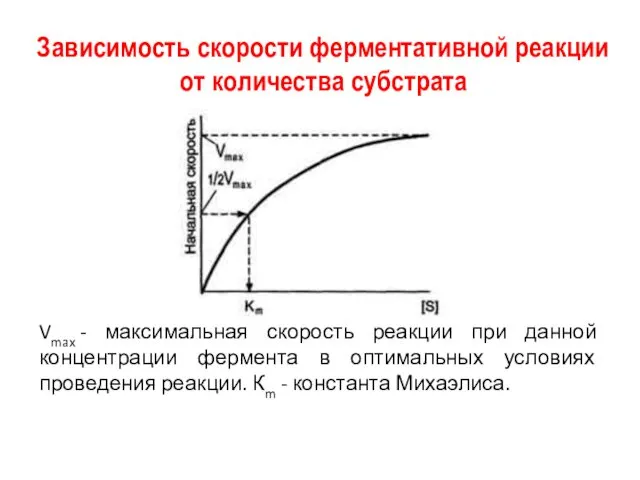
- 14. Зависимость скорости ферментативной реакции от количества субстрата Если концентрацию ферментов оставить постоянной, изменяя только количество субстрата,
- 15. Зависимость скорости ферментативной реакции от количества субстрата Vmax - максимальная скорость реакции при данной концентрации фермента
- 16. Уравнение Михаэлиса-Ментен Ферментативный процесс можно выразить следующим уравнением: где k1 - константа скорости образования фермент-субстратного комплекса;
- 17. Уравнение Михаэлиса-Ментен Наибольшая скорость реакции (Umax)наблюдается в том случае, когда все молекулы фермента находятся в комплексе
- 18. Порядок ферментативной реакции по субстрату Если концентрация субстрата значительно больше Km (S >> Km), то сумму
- 19. Km и Umax Vmax дает характеристику каталитической активности фермента и имеет размерность скорости ферментативной реакции моль/л,
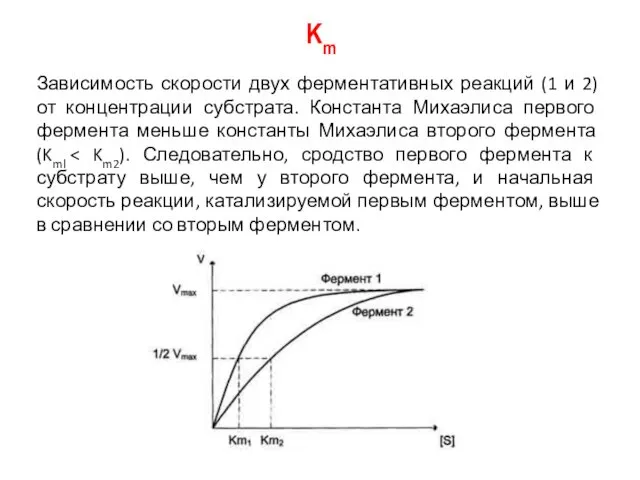
- 20. Km Зависимость скорости двух ферментативных реакций (1 и 2) от концентрации субстрата. Константа Михаэлиса первого фермента
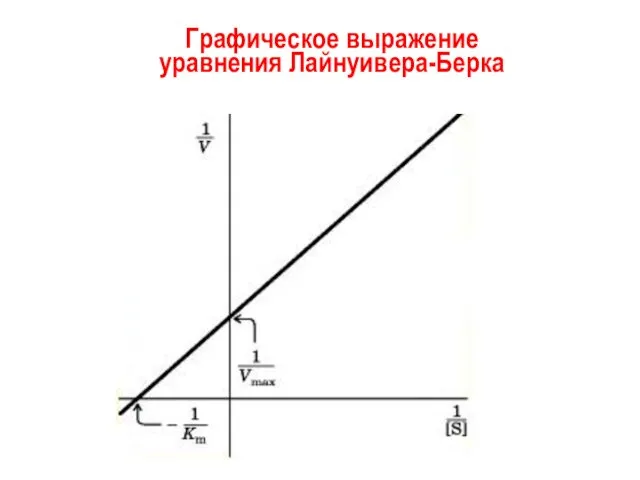
- 21. Анализ кинетики ферментов методом Лайнуивера-Берка Г. Лайнуивер и Д. Берк преобразовали уравнение Михаэлиса-Ментен, выразив обе части
- 22. Графическое выражение уравнения Лайнуивера-Берка
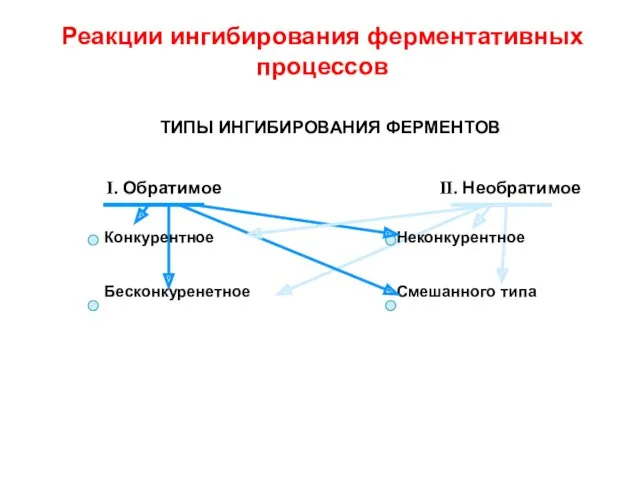
- 23. Реакции ингибирования ферментативных процессов ТИПЫ ИНГИБИРОВАНИЯ ФЕРМЕНТОВ I. Обратимое II. Необратимое Конкурентное Неконкурентное Бесконкуренетное Смешанного типа
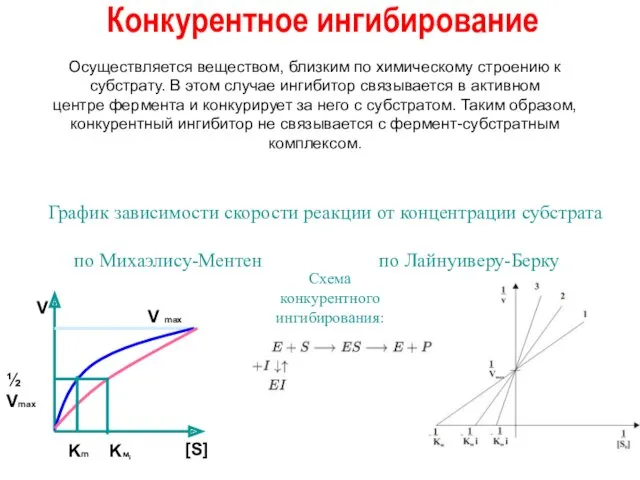
- 24. Конкурентное ингибирование Осуществляется веществом, близким по химическому строению к субстрату. В этом случае ингибитор связывается в
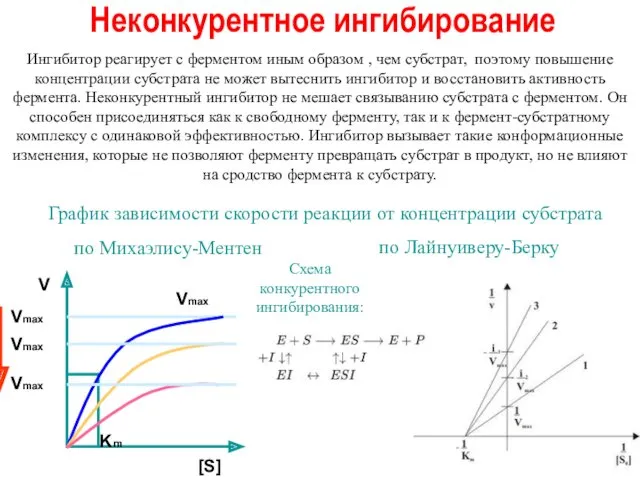
- 25. Неконкурентное ингибирование Ингибитор реагирует с ферментом иным образом , чем субстрат, поэтому повышение концентрации субстрата не
- 26. Бесконкурентное ингибирование При бесконкурентном ингибировании ингибитор связывается только с фермент-субстратным комплексом, но не со свободным ферментом.
- 27. Смешанное ингибирование Ингибитор связывается как в активном центре, так и вне его, а комплекс ЕI сохраняет
- 28. Сравнение типов ингибирования ферментов
- 29. Классификация ферментов.
- 30. Тривиальная классификация ферментов Название ферментов строится по принципу: Субстрат + реакция катализируемая ферментом + аза Например:
- 31. Международная классификация ферментов Шифр ферментов: 1.1.1.27 - ЛДГ В каждом шифре 4 цифры: 1 - класс
- 32. Классификация ферментов 1. Оксидоредуктазы - катализируют окислительно-восстановительные реакции 2. Трансферазы - катализируют реакции межмолекулярного переноса 3.
- 33. Дегидрогеназы - аэробные (малатдегидрогеназа, сукцинатдегидрогеназа) - анаэробные Оксигеназы - монооксигеназы - диоксигеназы Редуктазы Оксидоредуктазы Коферменты: НАД,
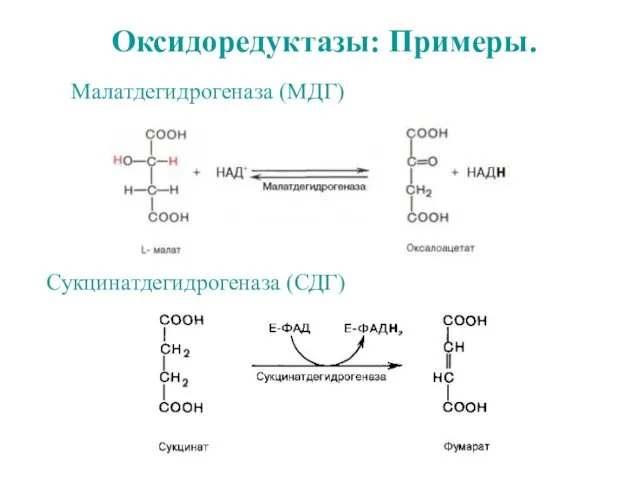
- 34. Оксидоредуктазы: Примеры. Малатдегидрогеназа (МДГ) Сукцинатдегидрогеназа (СДГ)
- 35. Трансферазы Ферменты: Аминотрансферазы Фосфотрансферазы Гликозилтрансферазы Коферменты: АТФ, ГТФ, УДФ, ЦДФ, тетрогидрофолиевая кислота, фосфопиридоксаль, SH-Коэнзим А, ФАФС.
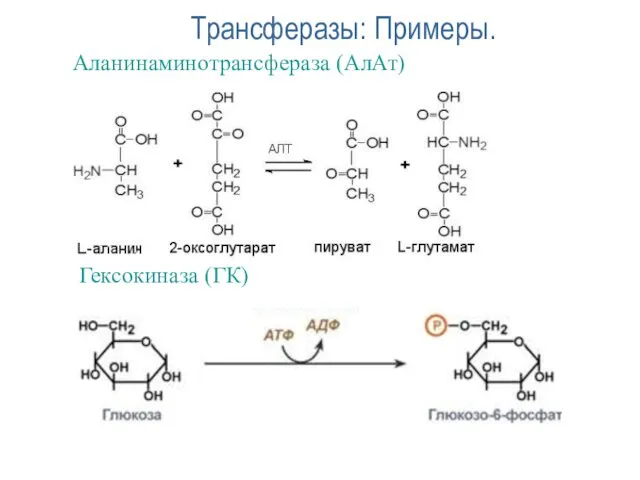
- 36. Трансферазы: Примеры. Аланинаминотрансфераза (АлАт) Гексокиназа (ГК)
- 37. Гидролазы Ферменты: Пептидгидролазы: - аминопептидазы - карбоксипептидаза - дипептидазы - пепсин - трипсин - химотрипсин Гликозидазы
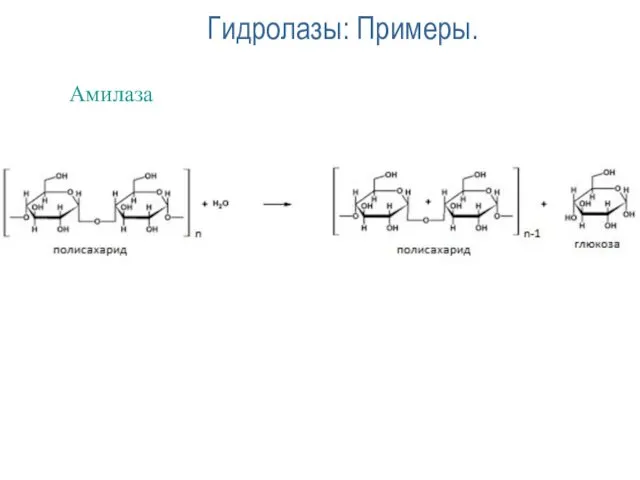
- 38. Гидролазы: Примеры. Амилаза
- 39. Лиазы Коферменты: - Фосфопиридоксаль - Тиаминпирофосфат Варианты разрывов связи: С-С С-О С-N С-S
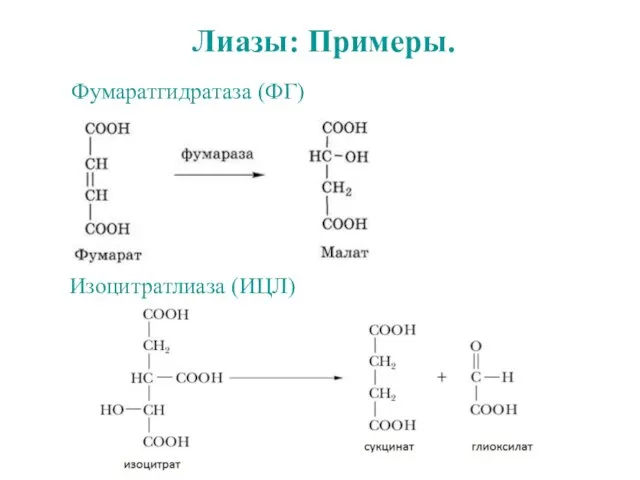
- 40. Лиазы: Примеры. Фумаратгидратаза (ФГ) Изоцитратлиаза (ИЦЛ)
- 41. Изомеразы Коферменты: кобамидные коферменты (витамин B12) Цис-трансизомеразы Внутримолекулярные
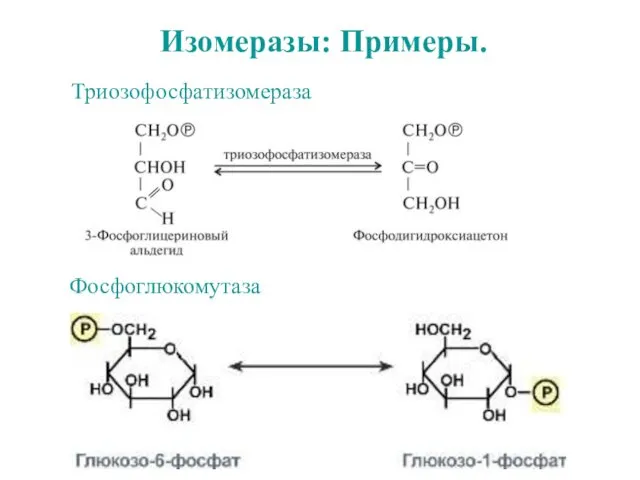
- 42. Изомеразы: Примеры. Триозофосфатизомераза Фосфоглюкомутаза
- 43. Лигазы Коферменты: - биотин - HS-КоА Ферменты: Глутаминсинтетаза Пируваткарбоксилаза Обязательный участник АТФ
- 45. Скачать презентацию

![Скорость ферментативной реакции На начальном этапе [0 - t0] скорость](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/80140/slide-2.jpg)


























 Искусство Испании XVII века
Искусство Испании XVII века Задержание в качестве подозреваемого
Задержание в качестве подозреваемого Производство серной кислоты H2SO4
Производство серной кислоты H2SO4 От всей души
От всей души Секреты осеннего леса (интегрированный урок)
Секреты осеннего леса (интегрированный урок) Г.Сабитов Ярсулы яз.
Г.Сабитов Ярсулы яз. Специальная обработка
Специальная обработка Пезентация на тему Моя любимая работа
Пезентация на тему Моя любимая работа Черные дыры
Черные дыры Презентация для 7 класса Саванны
Презентация для 7 класса Саванны Режим работы водителя. Соглашение AETR
Режим работы водителя. Соглашение AETR Беҙҙә ҡышлаусы ҡоштар
Беҙҙә ҡышлаусы ҡоштар Тула веками оружие ковала...Часть2
Тула веками оружие ковала...Часть2 Материал для родительского собрания Нравственные законы семьи – законы жизни (родительский всеобуч от 30 .01.2015 года) К воспитанию детей следовало бы относиться как к самой важной из земных профессий.
Материал для родительского собрания Нравственные законы семьи – законы жизни (родительский всеобуч от 30 .01.2015 года) К воспитанию детей следовало бы относиться как к самой важной из земных профессий. Monitorizarea calitatii. Energiei electrice
Monitorizarea calitatii. Energiei electrice Дифференциальные уравнения. Линейные дифференциальные уравнения высшего порядка
Дифференциальные уравнения. Линейные дифференциальные уравнения высшего порядка Минувшее в настоящем. Ценить прошлое и настоящее
Минувшее в настоящем. Ценить прошлое и настоящее Презентация МИНИ -МУЗЕЙ ПУГОВКА
Презентация МИНИ -МУЗЕЙ ПУГОВКА Горячий цех на предприятиях общественного питания
Горячий цех на предприятиях общественного питания Проблема бездомных животных
Проблема бездомных животных Естественный отбор, его формы
Естественный отбор, его формы Сравнение углов наложением
Сравнение углов наложением What is shrove tuesday
What is shrove tuesday Презентация к уроку в 7 классе по ОЗОЖ.
Презентация к уроку в 7 классе по ОЗОЖ. Органы чувств. 3 класс
Органы чувств. 3 класс Радіоелектроніка. Робота напівпровідникових випрямлячів
Радіоелектроніка. Робота напівпровідникових випрямлячів Инновационные технологии в строительстве
Инновационные технологии в строительстве Культура Казахстана в XVIII-XIX веках
Культура Казахстана в XVIII-XIX веках