Содержание
- 2. Почему ПСХЭ названа - ПЕРИОДИЧЕСКОЙ? ПСХЭ – это графическая запись ПЕРИОДИЧЕСКОГО ЗАКОНА!
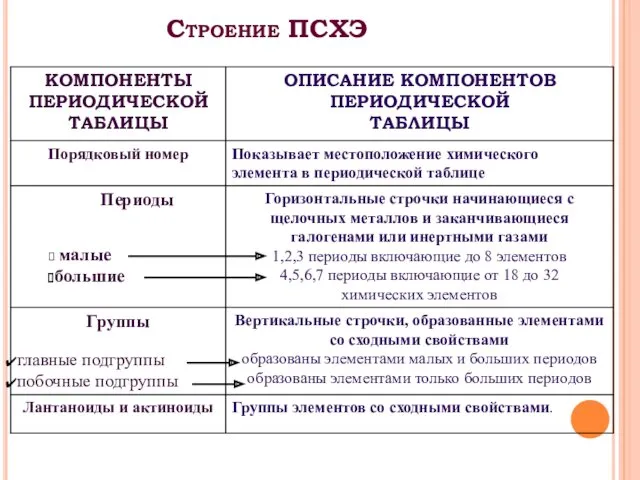
- 3. Строение ПСХЭ
- 4. Строение атома
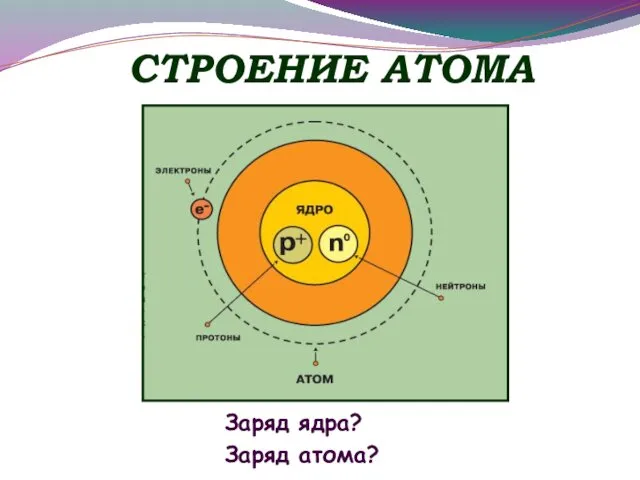
- 5. СТРОЕНИЕ АТОМА Заряд ядра? Заряд атома?
- 6. АТОМ p и n - нуклоны, из их массы слагается масса атома. Ядро атома ± p
- 7. Взаимосвязь положения элемента в ПСХЭ и строением его атома Порядковый номер элемента соответствует заряду ядра атома
- 8. Характеристика серы S Порядковый номер равен ?, следовательно заряд ядра + ?, общее количество электронов ?,
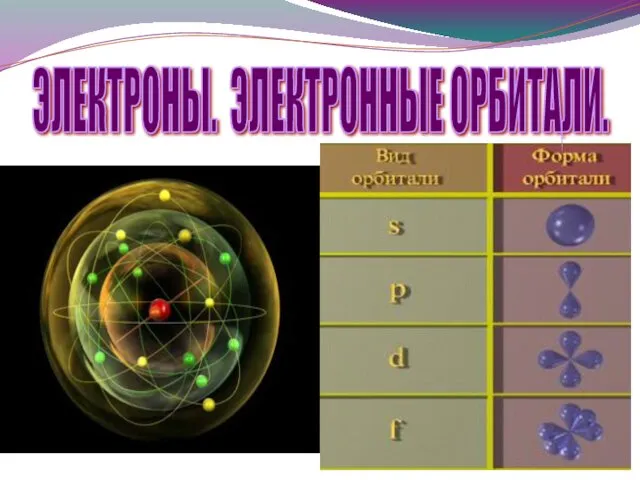
- 9. ЭЛЕКТРОНЫ. ЭЛЕКТРОННЫЕ ОРБИТАЛИ.
- 10. Электронные орбитали ↑↓ Электронная орбиталь вмещает два электрона отличающиеся своим спином
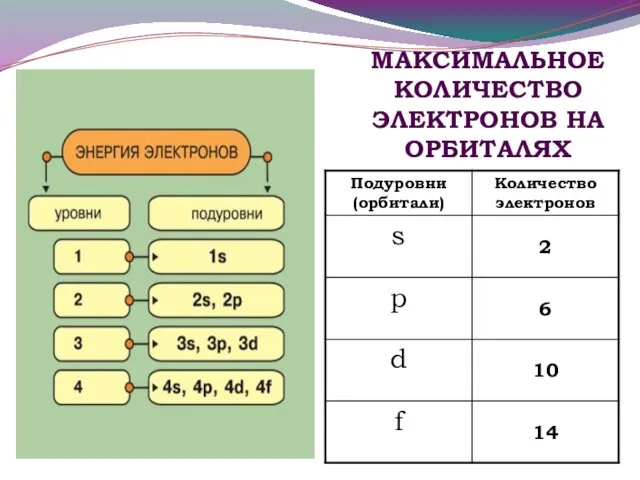
- 11. МАКСИМАЛЬНОЕ КОЛИЧЕСТВО ЭЛЕКТРОНОВ НА ОРБИТАЛЯХ
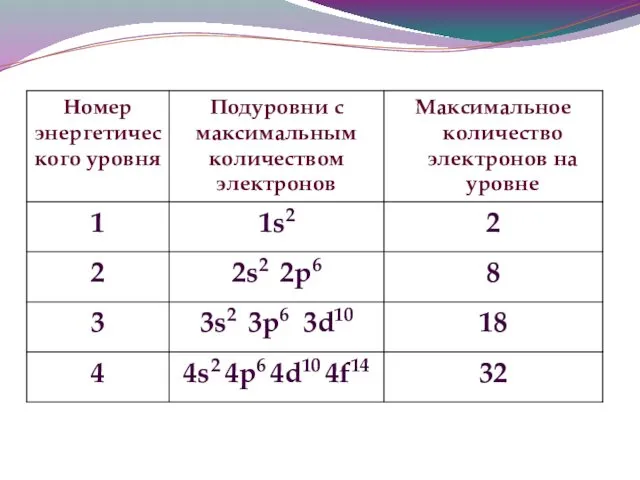
- 13. Строение энергетических уровней
- 14. ШКАЛА ЭНЕРГИИ 1s
- 15. Взаимосвязь положения элемента в ПСХЭ с электронным строением его атома 1. Порядковый номер элемента соответствует заряду
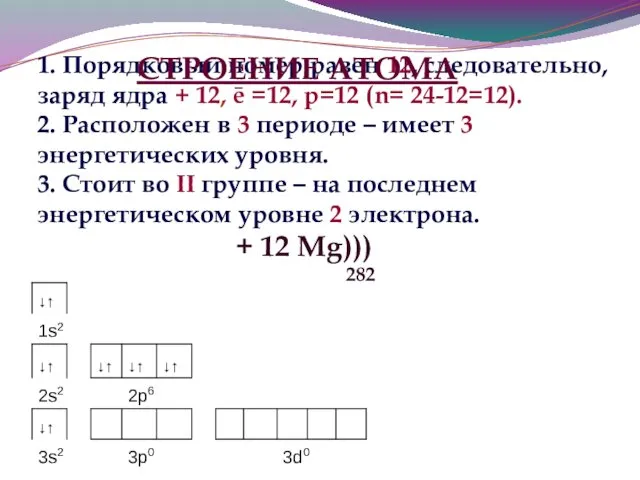
- 16. 1. Порядковый номер равен 12, следовательно, заряд ядра + 12, ē =12, р=12 (n= 24-12=12). 2.
- 17. Строение электронных оболочек атомов
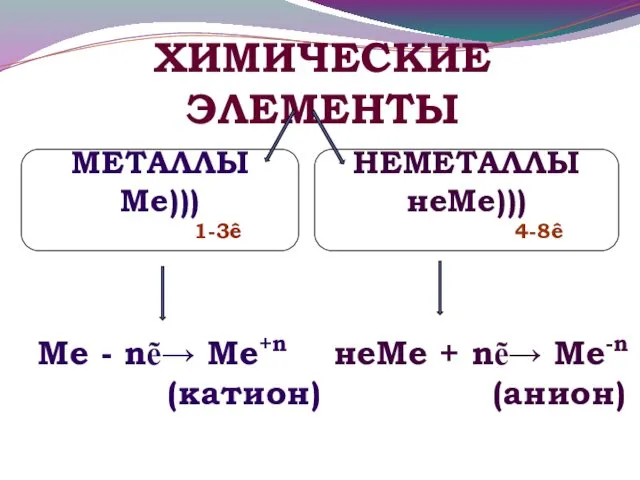
- 18. Ме - nẽ→ Ме+n неМе + nẽ→ Ме-n (катион) (анион) ХИМИЧЕСКИЕ ЭЛЕМЕНТЫ МЕТАЛЛЫ Ме))) 1-3ê НЕМЕТАЛЛЫ
- 19. ИЗМЕНЕНИЕ СВОЙСТВ АТОМОВ ХИМИЧЕСКИХ ЭЛЕМЕНТОВ ПО ПЕРИОДУ ПО ГРУППЕ По периоду слева направо металлическая активность убывает,
- 21. Скачать презентацию










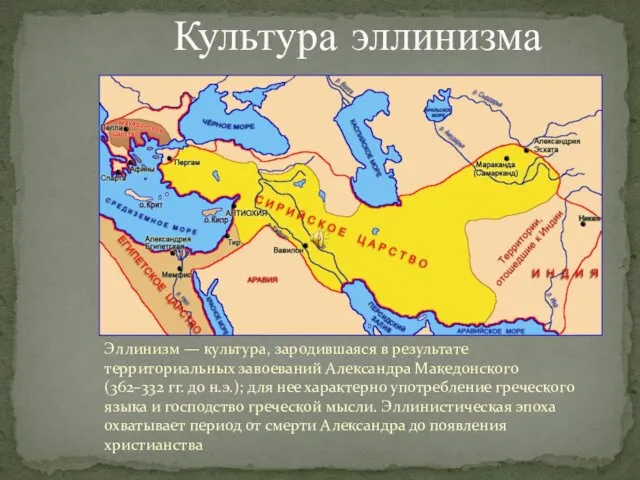 Культура Эллинизма
Культура Эллинизма 1С Парфюм Логистик
1С Парфюм Логистик Применение нетрадиционных источников энергии в Чувашской Республике
Применение нетрадиционных источников энергии в Чувашской Республике zanyatie_10_pro_zaychat_i_zaychihu
zanyatie_10_pro_zaychat_i_zaychihu Джон Эверетт Милле (John Everett Millais)
Джон Эверетт Милле (John Everett Millais) Мои земляки - труженики полей
Мои земляки - труженики полей Перу. План описания страны Латинской Америки
Перу. План описания страны Латинской Америки Имя прилагательное.Суффиксы прилагательных
Имя прилагательное.Суффиксы прилагательных Культура ислама. Основы духовно – нравственной культуры народов России
Культура ислама. Основы духовно – нравственной культуры народов России Что такое дисграфия и как с ней бороться?
Что такое дисграфия и как с ней бороться? Секреты семейного воспитания
Секреты семейного воспитания Презентация Игра в жизни ребенка
Презентация Игра в жизни ребенка E-learning и дистанционные технологии
E-learning и дистанционные технологии Microsoft Office Power Point
Microsoft Office Power Point Луч и угол
Луч и угол Глобальная энергетическая и сырьевая проблема
Глобальная энергетическая и сырьевая проблема Система мотивации за инновационные проекты
Система мотивации за инновационные проекты Тема поэта и поэзии в лирике А.С. Пушкина
Тема поэта и поэзии в лирике А.С. Пушкина Шляпный этикет, как правильно вписать аксессуар из прошлого в современный образ
Шляпный этикет, как правильно вписать аксессуар из прошлого в современный образ Кабинет географии
Кабинет географии Кроссворд Что мы знаем о пчёлах
Кроссворд Что мы знаем о пчёлах Органы растений. Побег
Органы растений. Побег Газообразное состояние вещества
Газообразное состояние вещества Гидроэлектростанции. Типы ГЭС
Гидроэлектростанции. Типы ГЭС Жигули. ОАО АвтоВАЗ
Жигули. ОАО АвтоВАЗ Отчет по искусствоведческой практике. Шаблон
Отчет по искусствоведческой практике. Шаблон Презентация Интеллектуальное развитие дошкольников
Презентация Интеллектуальное развитие дошкольников Винсент Ван Гог - краткая биография и картины художника
Винсент Ван Гог - краткая биография и картины художника