Содержание
- 2. Задание С1(36). Составление уравнения ОВР методом электронного баланса. Максимальное количество баллов за это задание – 3:
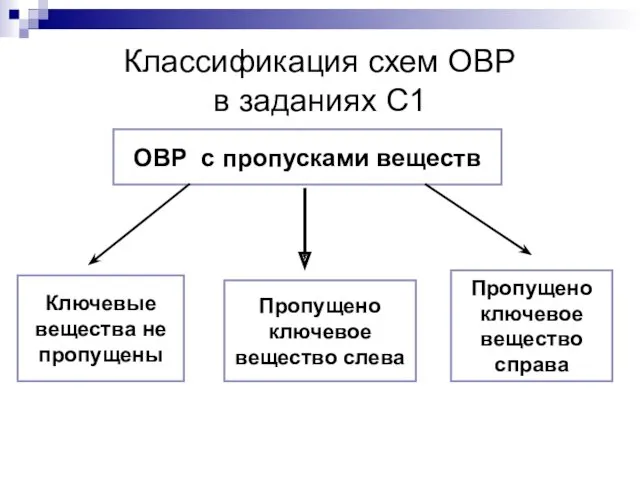
- 7. Классификация схем ОВР в заданиях С1 ОВР с пропусками веществ Пропущено ключевое вещество слева Пропущено ключевое
- 8. ПРИМЕР 1. Ключевые вещества в ОВР не пропущены. N+2O + KCl+1O + … → KN+5O3 +
- 9. 2NO + 3KClO + … → 2KNO3 + 3KCl + … В правой части схемы больше
- 10. ПРИМЕР 2. В ОВР пропущено ключевое вещество слева. …+ KMn+7O4 + … → N02 + К2Mn+6O4
- 11. N-3H3+ KMn+7O4 + … → N02 + К2Mn+6O4 + … Составляем уравнение электронного баланса 2N-3 -
- 12. Итоговое уравнение реакции: 2NH3 + 6KMnO4 + 6КОН → N2 + 6К2MnO4 + 6Н2О Исходная схема
- 13. ПРИМЕР 3. В ОВР пропущено ключевое вещество справа. Р-3Н3 + Ag+1NO3 + … → Ag0 +
- 14. Р-3Н3 + Ag+1NO3+ …→ Ag0+Н3РО4+HNO3. Составляем уравнение электронного баланса: Р-3 - 8ē →Р+5 1 восстановитель, окисляется
- 15. Пример 4. Используя метод электронного баланса, составьте уравнение реакции: NaI + NaNO2 + H2SO4 → I2↓
- 16. Составляются уравнения электронного баланса: 2 I-1 – 2ē → I02 1 окисляется N+3 + 1ē →
- 17. Задание С2 (37). Предложено описание химического эксперимента, в соответствии с которым нужно составить 4 уравнения реакции.
- 18. Трудности , с которыми сталкиваются учащиеся при выполнении задания С2: 1. Описание действий с веществами (фильтрование,
- 19. Соль, полученную при растворении железа в горячей концентрированной серной кислоте, обработали избытком раствора гидроксида натрия. Выпавший
- 20. toC 1) 2Fe + 6H2SO4(к)→Fe2(SO4)3+ 3SO2↑+ 6H2O 2) Fe2(SO4)3+ 6NaOH(к)→2Fe(OH)3↓+3Na2SO4 toC 3) 2Fe(OH)3 → Fe2O3+ 3H2O
- 21. Оранжевый оксид меди поместили в концентрированную серную кислоту и нагрели. К полученному голубому раствору прилили избыток
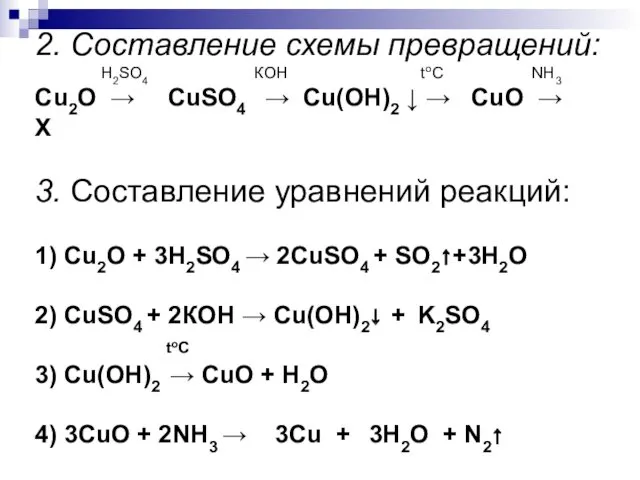
- 22. 2. Составление схемы превращений: Н2SO4 КОН toC NH3 Cu2O → СuSO4 → Cu(OH)2 ↓ → CuO
- 23. Учащиеся могут сами составить тексты заданий в соответствии со схемами превращений. toC toC/H2 HNO3( конц) NaOH,
- 24. Окислительно-восстановительные реакции, а не реакции обмена!
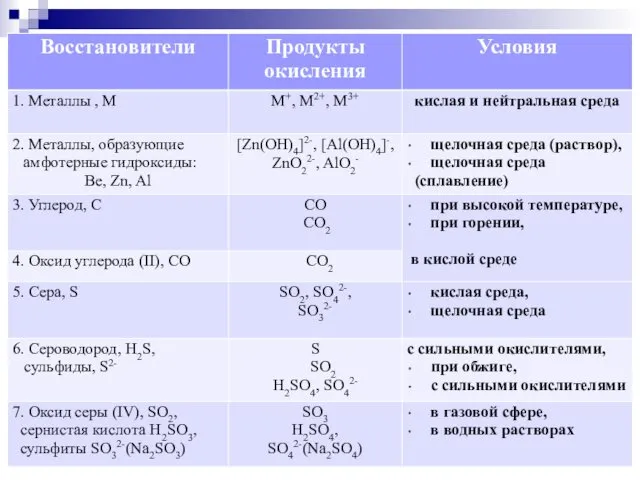
- 25. 1. Окислители – соединения железа (III), восстановители – сульфиды, йодиды. При этом катион Fe3+ →Fe2+, сульфид
- 26. 2FeCl3 + Na2S = S↓ + 2FeCl2 +2NaCl 2FeCl3 + H2S = S↓ + 2FeCl2 +
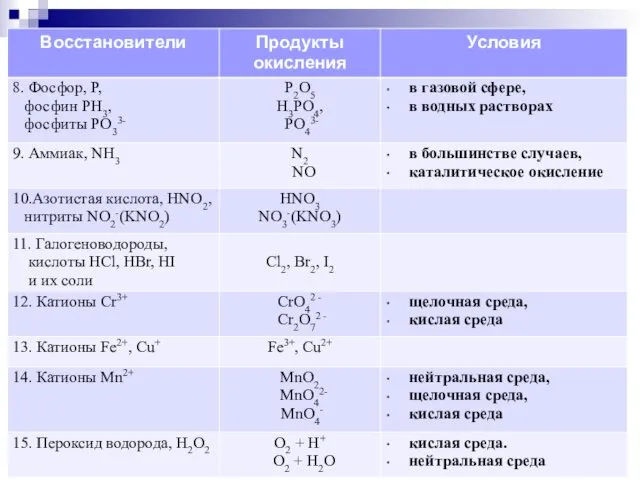
- 27. 2. Окислители – соединения меди (II), восстановители - йодиды. При этом: Cu2+ → Cu+, I- →I2
- 28. 2CuSO4 + 4KI = 2CuI↓ + I2↓+2K2SO4 2CuCl2 + 4KI = 2CuI↓ + I2↓ + 4KCl
- 29. 3. Окислитель – азотная кислота, восстановитель – сульфиды, йодиды, сульфиты. При этом азотная кислота, восстанавливается до
- 30. 8HNO3 (к) + CuS = CuSO4 + 8NO2↑ +4H2O или 4HNO3 (к)+ CuS = S↓ +
- 31. Амфотерные свойства веществ. Сплавление: Zn(OH)2 + 2NaOH = Na2ZnO2 + 2H2O ZnO + 2NaOH = Na2ZnO2
- 32. Реакции в растворе происходят с образованием комплексных солей: Zn(OH)2 + 2NaOH = Na2 [Zn(OH)4] ZnO +
- 33. Cоединения хрома (III) и железа (III) - Cr2O3, Cr(OH)3, Fe2O3, Fe(OH)3. оксиды этих металлов взаимодействуют со
- 34. Гидроксиды Cr (ІІІ) и Fe (ІІІ) взаимодействуя со щелочами в растворе, образуют комплексные соли с координационным
- 35. Ве, Zn, Al взаимодействуют с растворами щелочей : Be + 2NaOH + 2H2O = Na2[Be(OH)4] +
- 36. Cпособы разрушения комплексных солей. 1. При действии избытка сильной кислоты получаются две средних соли и вода:
- 37. 2. При действии недостатка сильной кислоты получается средняя соль активного металла, амфотерный гидроксид и вода: Na[Al(OH)4]
- 38. 3. При действии слабой кислоты получается кислая соль активного металла, амфотерный гидроксид и вода: Na[Al(OH)4] +
- 39. 4. При действии углекислого или сернистого газа получается кислая соль активного металла и амфотерный гидроксид: Na[Al(OH)4]
- 40. 5. При нагревании выделяется вода: Na[Al(OH)4] → NaAlO2 + 2H2O
- 42. Скачать презентацию
































![5. При нагревании выделяется вода: Na[Al(OH)4] → NaAlO2 + 2H2O](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/36098/slide-39.jpg)
 А песни тоже воевали
А песни тоже воевали Культура України 1960-х – 1980-х років ХХ ст
Культура України 1960-х – 1980-х років ХХ ст Материаловедение и технология конструкционных материалов раздел ТКМ
Материаловедение и технология конструкционных материалов раздел ТКМ для будущих водителей и их родителей
для будущих водителей и их родителей Итоговое родительское собрание 2 класс
Итоговое родительское собрание 2 класс Западная Европа в IX-XI веках
Западная Европа в IX-XI веках Селекторы. Урок 9
Селекторы. Урок 9 ИССЛЕДОВАТЕЛЬСКАЯ РАБОТА к юбилею Д.И. Менделеева
ИССЛЕДОВАТЕЛЬСКАЯ РАБОТА к юбилею Д.И. Менделеева Вещества и их свойства
Вещества и их свойства Гранд Макет Россия
Гранд Макет Россия Божа благодать в житті християнина
Божа благодать в житті християнина Перемешивание в жидких средах. Лекция 3
Перемешивание в жидких средах. Лекция 3 Электроснабжения инструментального цеха завода по производству запасных изделий к тракторам
Электроснабжения инструментального цеха завода по производству запасных изделий к тракторам Правописание безударных личных окончаний глаголов
Правописание безударных личных окончаний глаголов Подземная гидродинамика
Подземная гидродинамика Елочка из сена
Елочка из сена Криминологическая характеристика половых преступлений
Криминологическая характеристика половых преступлений Экономика и государство
Экономика и государство Путешествие по Санкт-Петербургу
Путешествие по Санкт-Петербургу Укрепление и сохранеие семейных ценностей и традиций
Укрепление и сохранеие семейных ценностей и традиций Европейский Юг
Европейский Юг Презентация Воспитание культуры поведения детей дошкольного возраста
Презентация Воспитание культуры поведения детей дошкольного возраста Международное движение рабочей силы
Международное движение рабочей силы Выпуклый анализ. Выпуклые множества. Лекция 8
Выпуклый анализ. Выпуклые множества. Лекция 8 Элементы экрана. Рабочий стол Windows XP (desktop)
Элементы экрана. Рабочий стол Windows XP (desktop) Турнир по быстрым шахматам 2015-16-01
Турнир по быстрым шахматам 2015-16-01 Целевая аудитория (или целевая группа)
Целевая аудитория (или целевая группа) Петр и Феврония Муромские
Петр и Феврония Муромские