Содержание
- 2. Цель урока. 1) Обобщить знания учащихся о составе атома и атомного ядра. 2) Раскрыть физический смысл
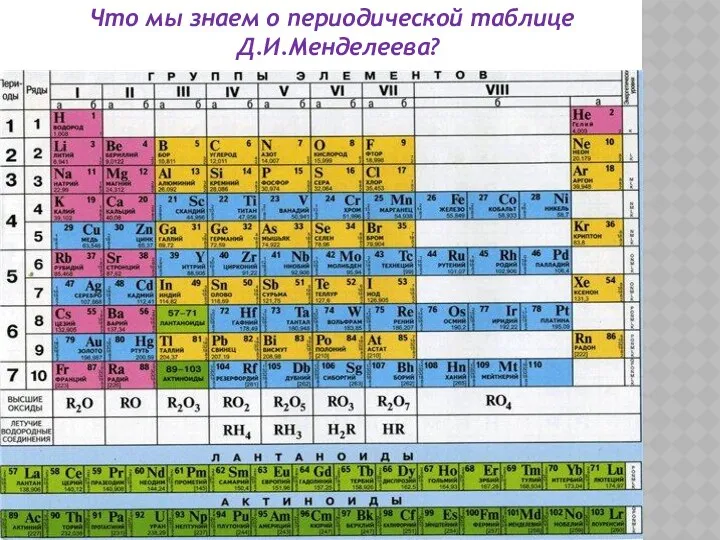
- 3. Что мы знаем о периодической таблице Д.И.Менделеева?
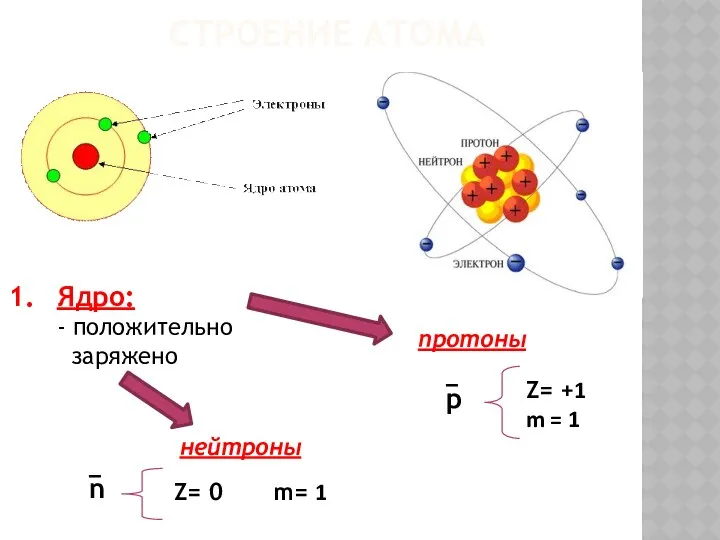
- 4. СТРОЕНИЕ АТОМА Ядро: - положительно заряжено протоны нейтроны p – n – Z= +1 m =
- 5. 2. Электроны e – m = 0 Z = –1 Атом – электронейтральная частица, следовательно число
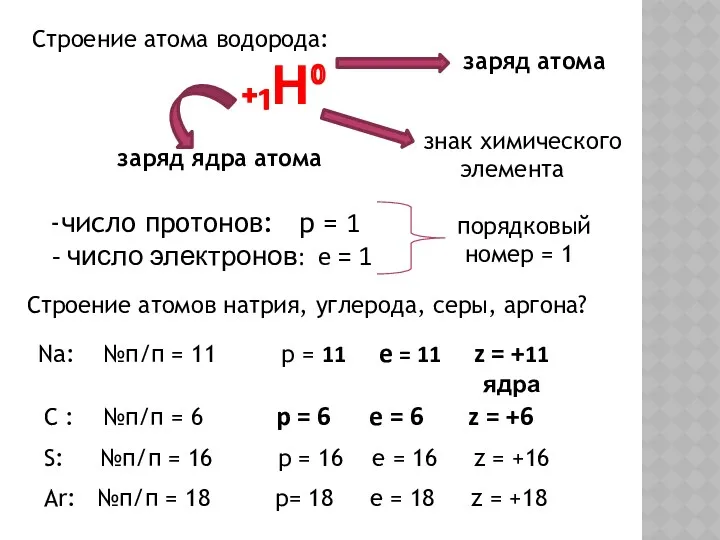
- 6. Строение атома водорода: ₊₁Н⁰ заряд ядра атома заряд атома знак химического элемента число протонов: p =
- 7. Как узнать число нейтронов в ядре атома? N = Ar(элемента) – № п/п n – Определите
- 8. ВЫВОДЫ: 1. Строение атома: 2. Определите строение атомов химических элементов с зарядом ядра атома: а) +
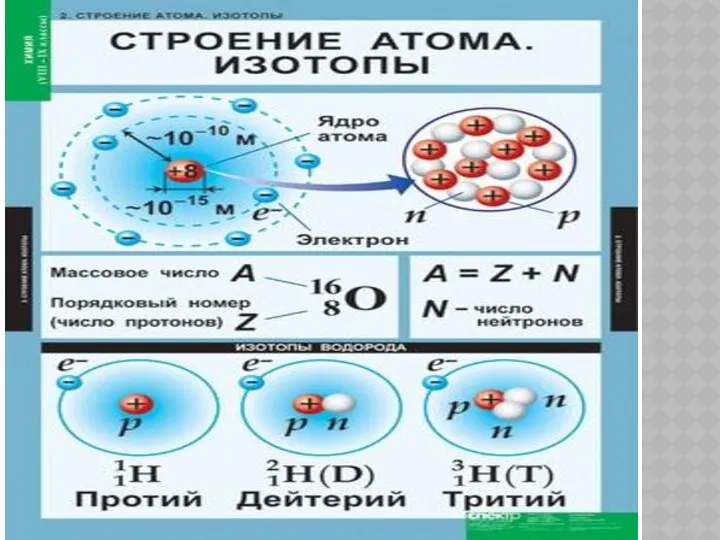
- 9. ИЗОТОПЫ +1Hº +1Hº +1Hº ¹ ² ³ протий дейтерий тритий правильная форма обозначения изотопа :массовое число
- 12. Скачать презентацию





 Выступление на Новый год Сказка в Новогоднюю ночь
Выступление на Новый год Сказка в Новогоднюю ночь Презентация музыкальные инструменты
Презентация музыкальные инструменты Методическая разработка раздела образовательной программы по футболу Тактическая и техническая подготовка футболистов 7-9 лет
Методическая разработка раздела образовательной программы по футболу Тактическая и техническая подготовка футболистов 7-9 лет Деловой этикет в профессиональной деятельности педагога.
Деловой этикет в профессиональной деятельности педагога. Методы и технологии конструирования изделий. Поверхностное моделирование объектов. (Лекция 3)
Методы и технологии конструирования изделий. Поверхностное моделирование объектов. (Лекция 3) Сравнение стандартов 2004 г. и ФГОС второго поколения. Изменения в содержании образования и в подходах к преподаванию.
Сравнение стандартов 2004 г. и ФГОС второго поколения. Изменения в содержании образования и в подходах к преподаванию. Страны Евразии. Обобщение. Задания
Страны Евразии. Обобщение. Задания Пиломатериалы. Виды и классификация пиломатериалов
Пиломатериалы. Виды и классификация пиломатериалов Строгание. Виды рубанков
Строгание. Виды рубанков Семинар-тренинг по подготовке к квалификационному экзамену по направлению движимое имущество
Семинар-тренинг по подготовке к квалификационному экзамену по направлению движимое имущество Богоматерь Владимирская. Первая треть XII в
Богоматерь Владимирская. Первая треть XII в Проективный графический тест Дерево
Проективный графический тест Дерево Презентация по методической теме: Балаларда туган җиребезгә мәхәббәт, аның табигатенә карата сакчыл караш тәрбияләү һәм экологик тәрбия бирү 2011-2015 год
Презентация по методической теме: Балаларда туган җиребезгә мәхәббәт, аның табигатенә карата сакчыл караш тәрбияләү һәм экологик тәрбия бирү 2011-2015 год Подбор сечения балки КМ. Прокатное сечение
Подбор сечения балки КМ. Прокатное сечение Средства для похудения
Средства для похудения Работа с семьей воспитанника с расстройством аутистического спектра (РАС)
Работа с семьей воспитанника с расстройством аутистического спектра (РАС) Презентация мини-музея Русская изба с детьми старшего дошкольного возраста
Презентация мини-музея Русская изба с детьми старшего дошкольного возраста Основы строения органических соединений
Основы строения органических соединений тест оксиды
тест оксиды Образ России в искусстве. Виды изобразительного искусства
Образ России в искусстве. Виды изобразительного искусства Сущ
Сущ Музыкальное развитие ребенка. Презентация.
Музыкальное развитие ребенка. Презентация. ИжГТУ имени М. Т. Калашникова. Итоги учебного года 2019/2020 и задачи нового учебного года
ИжГТУ имени М. Т. Калашникова. Итоги учебного года 2019/2020 и задачи нового учебного года 20230921_frazeologizmeher_0
20230921_frazeologizmeher_0 Мемориал Хатынь
Мемориал Хатынь Чем занять детей дома
Чем занять детей дома Шаблон Фракталы-25
Шаблон Фракталы-25 Внутренняя политика Александра I в 1815 – 1825
Внутренняя политика Александра I в 1815 – 1825