Содержание
- 2. 1 8 7 4 5 6 3 2 9
- 3. 1 Опытным путём определить, в каких пробирках содержатся растворы гидроксида натрия, хлорида натрия и соляная кислота.
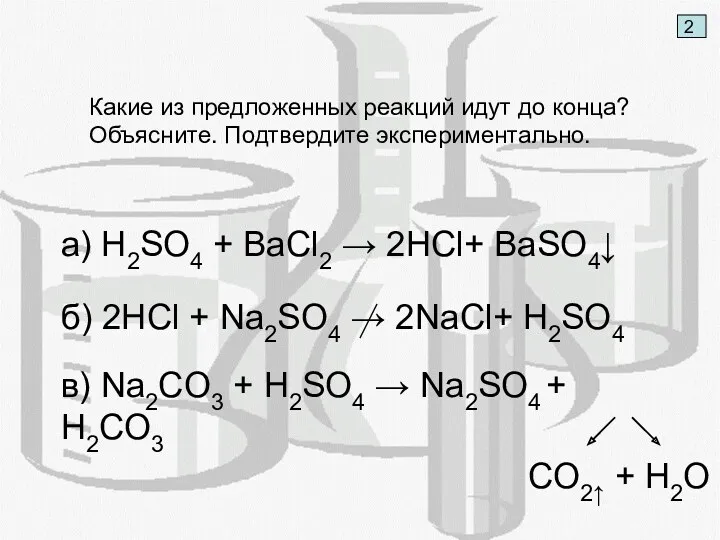
- 4. 2 Какие из предложенных реакций идут до конца? Объясните. Подтвердите экспериментально. a) H2SO4 + BaCl2 →
- 5. 3 «Третий лишний». Среди каждой тройки веществ найти вещество, отличающееся от двух других. Указать признак отличия:–
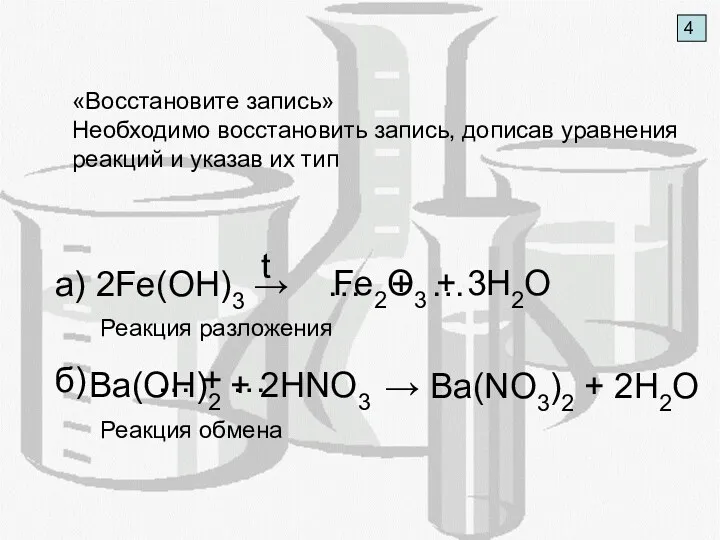
- 6. 4 «Восстановите запись» Необходимо восстановить запись, дописав уравнения реакций и указав их тип → Ba(NO3)2 +
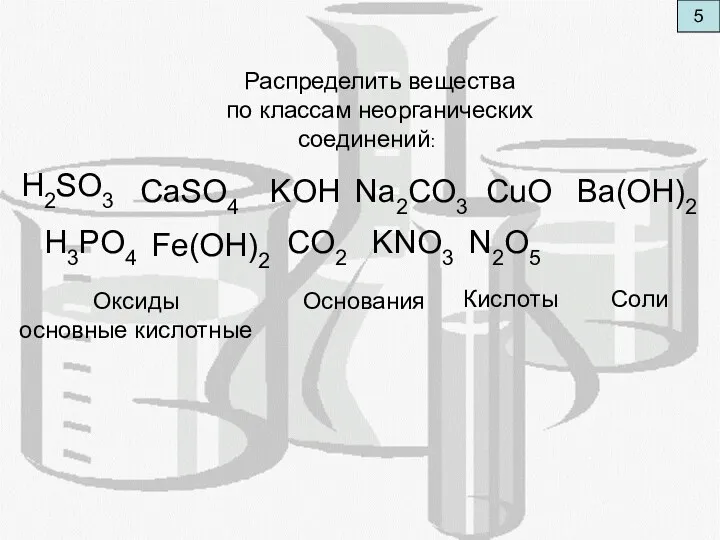
- 7. 5 Распределить вещества по классам неорганических соединений: Оксиды основные кислотные Кислоты Основания Соли CO2 CaSO4 Ba(OH)2
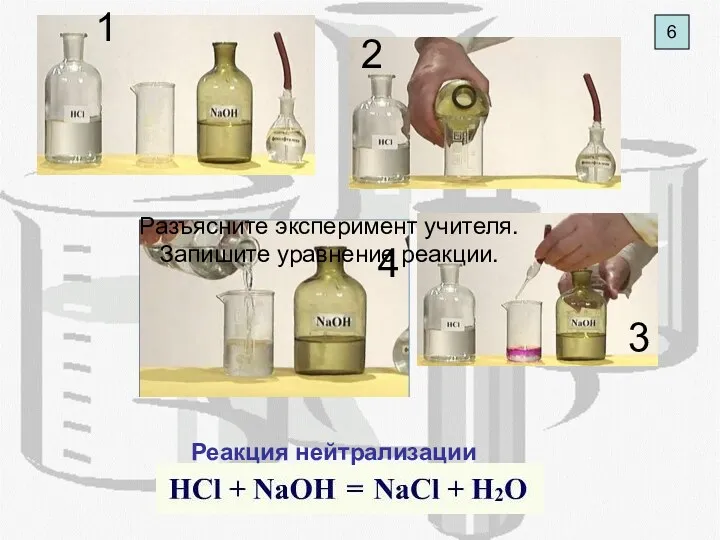
- 8. 6 Реакция нейтрализации Разъясните эксперимент учителя. Запишите уравнение реакции.
- 9. Запишите реакции взаимодействия А) Алюминия с соляной кислотой Б) Цинка с серной кислотой В) Меди с
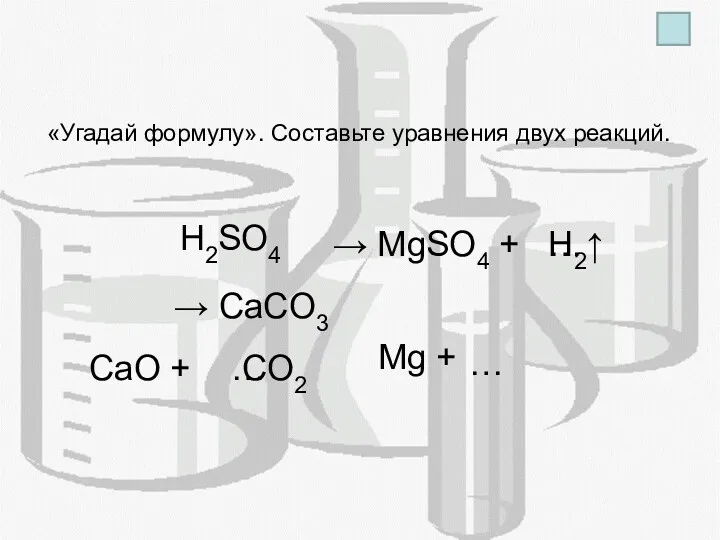
- 10. «Угадай формулу». Составьте уравнения двух реакций. CaO + Mg + → MgSO4 + → CaCO3 …
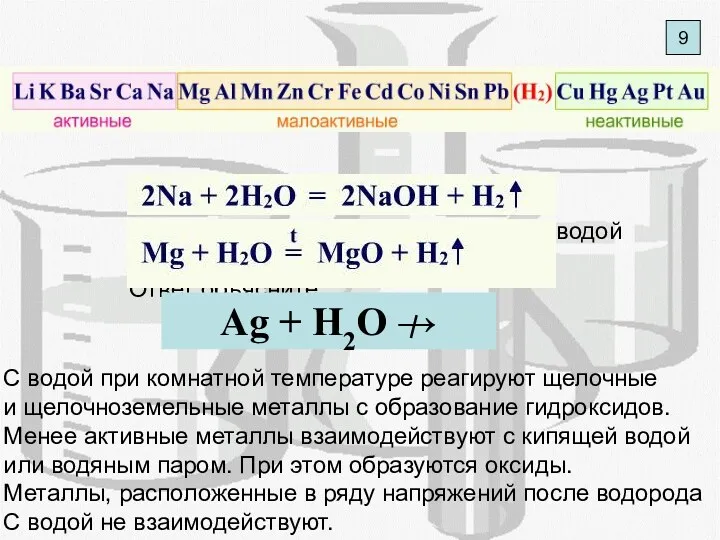
- 11. 9 Запишите реакцию взаимодействия с водой А) Na Б) Mg В) Ag Ответ объясните. С водой
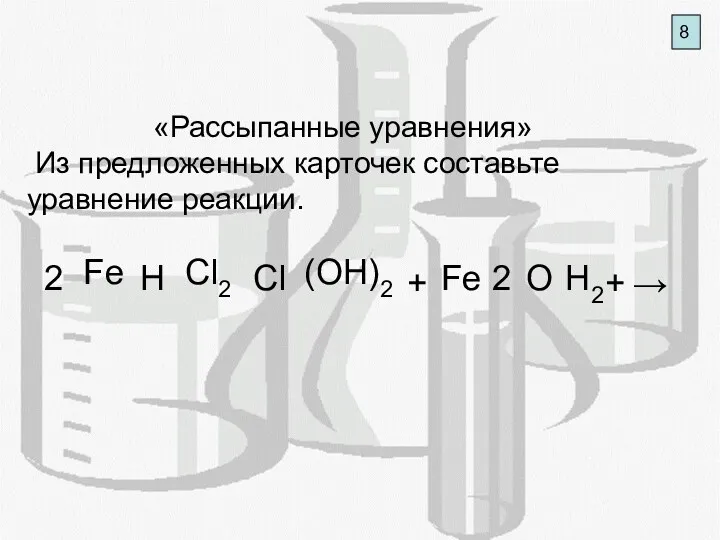
- 12. 8 «Рассыпанные уравнения» Из предложенных карточек составьте уравнение реакции. 2 Fe H Cl2 Cl (OH)2 +
- 13. Дистиллированная (очищенная) вода, стоящая на воздухе имеет кислую реакцию среды. Поясните, почему так происходит, запишите уравнение
- 14. «Кто быстрее». Даны вещества: CO2, HCl, Mg, Ba(OH)2, Na2O, Cu(OH)2. Какие из них взаимодействуют друг с
- 15. • Какое из перечисленных утверждений справедливо для солей: 1) Всегда растворимы; 2) Всегда твердые; 3) Бывают
- 17. Скачать презентацию






 Презентация Театральная деятельность в детском саду, из опыта работы ГБОУ СОШ ж-д ст.Погрузная
Презентация Театральная деятельность в детском саду, из опыта работы ГБОУ СОШ ж-д ст.Погрузная Исламское право. Источники
Исламское право. Источники Урок ОРКСиЭ. Тема :Дружба
Урок ОРКСиЭ. Тема :Дружба Логопедический проект Моя удивительная буква
Логопедический проект Моя удивительная буква Логопедическая ритмика
Логопедическая ритмика Я великан. Игра
Я великан. Игра Силосы и бункеры
Силосы и бункеры 9 Мая
9 Мая Музеи в жизни города. 3 класс
Музеи в жизни города. 3 класс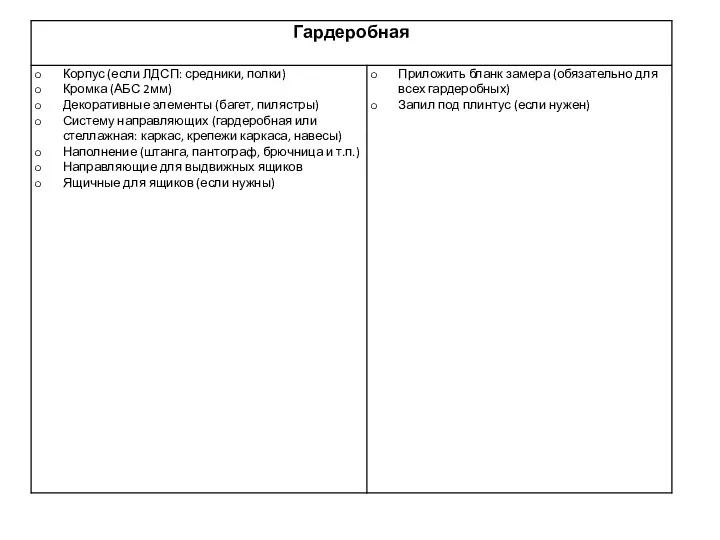 Гардеробная. Бланк замера
Гардеробная. Бланк замера Защита от антигенов. Иммунитет
Защита от антигенов. Иммунитет Окна Роста. Агитационные плакаты
Окна Роста. Агитационные плакаты Имидж педагога
Имидж педагога Родители как полноправные участники образовательных отношений в аспекте реализации основных образовательных программ
Родители как полноправные участники образовательных отношений в аспекте реализации основных образовательных программ Прощай, начальная школа. 4-б класс
Прощай, начальная школа. 4-б класс Первая полоса - лицо газеты
Первая полоса - лицо газеты Prezentatsia_Vlad_D-11
Prezentatsia_Vlad_D-11 Мои деды: участники ВОВ
Мои деды: участники ВОВ Презентация по теме Жидкие вещества
Презентация по теме Жидкие вещества Бароко: архітектура, скульпура, живопис
Бароко: архітектура, скульпура, живопис Взаимосвязь эмпатии личности и выбора стратегий поведения в конфликте (на примере общеобразовательной организации)
Взаимосвязь эмпатии личности и выбора стратегий поведения в конфликте (на примере общеобразовательной организации) Протон и нейтрон. Строение ядра
Протон и нейтрон. Строение ядра Развивающие игры палочки Кюизенера
Развивающие игры палочки Кюизенера Здоровый образ жизни
Здоровый образ жизни Конспект занятия по безопасности жизнедеятельности дошкольников с включением компьютерной игры На тему опасности дома (+ презентация)
Конспект занятия по безопасности жизнедеятельности дошкольников с включением компьютерной игры На тему опасности дома (+ презентация) Дисграфия и дислексия у учащихся начальных классов
Дисграфия и дислексия у учащихся начальных классов Петербургские музеи-хранители истории
Петербургские музеи-хранители истории Города и сельские поселения
Города и сельские поселения