Слайд 2

Химическое равновесие
Реакции, которые одновременно протекают в прямом и обратном направлении, называются
обратимыми
Состояние химического обратимого процесса, при котором скорость прямой реакции равна скорости обратной реакции, называется химическим равновесием
Слайд 3

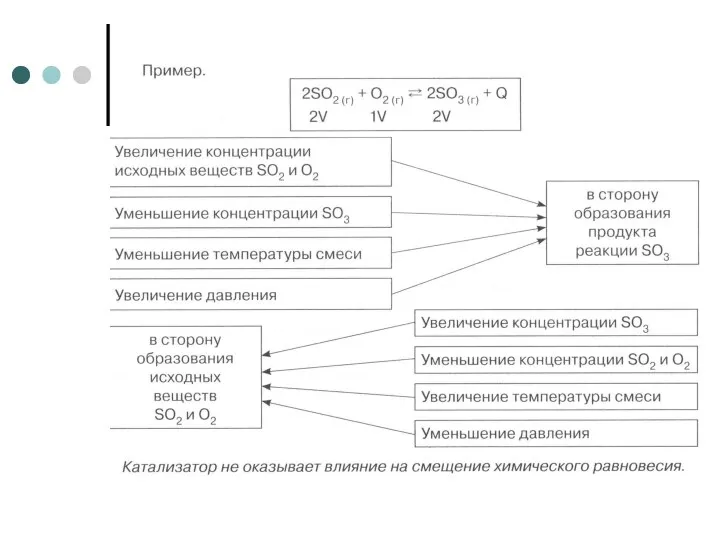
Смещение химического равновесия осуществляется в соответствии с принципом Ле Шателье
Если на
систему, находящуюся в состоянии химического равновесия, оказать внешнее воздействие (изменить концентрацию, температуру, давление), то равновесие смещается в сторону той реакции, которая ослабляет это воздействие
Слайд 4
Слайд 5

Процессы, протекающие при обратимых реакциях
Слайд 6

Процессы, протекающие при обратимых реакциях
прямая реакция
αА + βВ γС
+ δD
обратная реакция
υ ═ k1 · [A]α · [B]β
Слайд 7
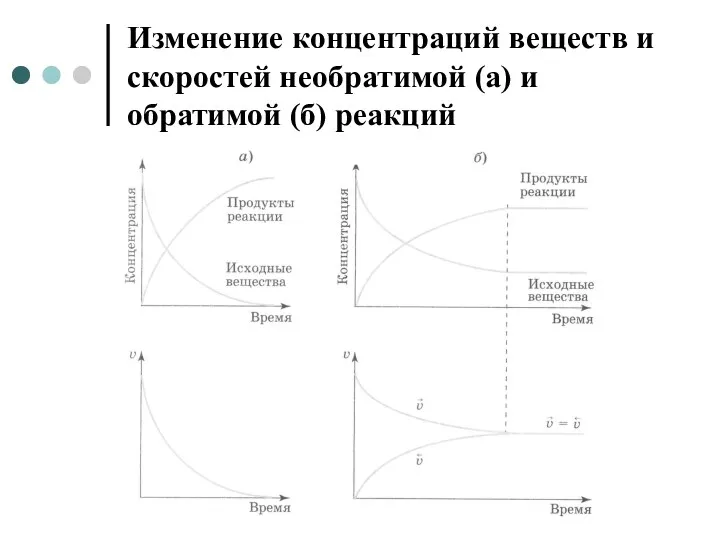
Изменение концентраций веществ и скоростей необратимой (а) и обратимой (б) реакций
Слайд 8








 Влияние ИКТ на качество знаний
Влияние ИКТ на качество знаний Ветеран в истории села Хлебное. Пылёв Николай Васильевич
Ветеран в истории села Хлебное. Пылёв Николай Васильевич Использование интерактивных технологий на занятиях с детьми раннего возраста
Использование интерактивных технологий на занятиях с детьми раннего возраста А. Плещеев Сельская песенка, А. Майков Ласточка примчалась…, Весна
А. Плещеев Сельская песенка, А. Майков Ласточка примчалась…, Весна Виды рукавов
Виды рукавов Такая разная любовь (по повести А.И. Куприна Гранатовый браслет)
Такая разная любовь (по повести А.И. Куприна Гранатовый браслет) Развивающее предметное пространство
Развивающее предметное пространство Технология ремонта автосцепного устройства в объёме ДР
Технология ремонта автосцепного устройства в объёме ДР Модест Петрович Мусоргский презентация.
Модест Петрович Мусоргский презентация. Матримониальные планы молодёжи
Матримониальные планы молодёжи День памяти жертв политических репрессий 30 октября отмечается в России
День памяти жертв политических репрессий 30 октября отмечается в России Социальный проект
Социальный проект ООО Котлетарь
ООО Котлетарь Четырехугольник. Виды четырехугольника
Четырехугольник. Виды четырехугольника Жидкое биотопливо. Проблемы и перспективы
Жидкое биотопливо. Проблемы и перспективы ПроектКомпетентность родителей как условие содействия нравственному и эмоциональному благополучию ребенка
ПроектКомпетентность родителей как условие содействия нравственному и эмоциональному благополучию ребенка Металлорежущие станки
Металлорежущие станки Толерантность - путь к миру
Толерантность - путь к миру Метод проектов в дошкольном образовании.
Метод проектов в дошкольном образовании. Технологии развивающего обучения
Технологии развивающего обучения Презентация Удивительные сооружения
Презентация Удивительные сооружения Презентация к уроку Атлантический океан7 класс
Презентация к уроку Атлантический океан7 класс Публичное выступление 2013
Публичное выступление 2013 А. Платонов Ещё мама 15 ап
А. Платонов Ещё мама 15 ап Методы воспитания
Методы воспитания Бактериологическое оружие и его воздействие на организм человека
Бактериологическое оружие и его воздействие на организм человека Анализ аптечного ассортимента лекарственного растительного сырья, содержащего эфирные масла и препаратов из него
Анализ аптечного ассортимента лекарственного растительного сырья, содержащего эфирные масла и препаратов из него Театральный и музыкальный Петербург
Театральный и музыкальный Петербург