Слайд 2

Цели урока:
дидактическая:показать практическое применение понятия «наименьшее общее кратное при составлении химических
формул
образовательная: обобщить знания учащихся о НОК и научиться применять данное понятие при решении химических задач
развивающая: формировать умения применять приемы и понятия одной области знаний- математики- на на примерах из других областей.
Воспитательная: создать условия для развития коммуникативной культуры,диалогической речи учащихся,прививать навыки работы с веществами,используемыми в быту
Слайд 3

Найти НОК ( 120; 180 )
Разложим данные числа на простые
множители:
126 = 2*3*3*7 180 = 2*2*3*3*5
63 90
21 45
7 15
1 5
1
Слайд 4

3.Выпишем множители, входящие в состав первого числа:
(2*3*3*7 )
4. Добавим недостающие множители
остальных чисел:
(2*3*3*7 )*2*5
Слайд 5

4. Получим :
НОК ( 126; 180 )=
= (2*3*3*7 )* 2*5=
126 *10 =
=1260
Слайд 6

Найти НОК чисел:
1. 2 и 3
2. 4 и 12
3.
7 и 2
4. 5 и 2
5. 6 и 8
6. 8 и 12
Слайд 7

Составить химическую формулу вещества, образованную атомами серы и кислорода
1. Запишите рядом
символы химических элементов, которые входят в состав вещества
S O
Слайд 8

2. Над знаками химических элементов поставьте их степень окисления
+6 -2
S O
Слайд 9

3. Определим НОК чисел, выражающих степень окисления этих элементов
Запишем НОК под
формулой
S O
НОК(6,2)=6
Слайд 10

4. Разделим НОК на степень окисления каждого элемента. Запишем полученные индексы
SO3
6:6=1 6:2=3
Слайд 11

По степени окисления составим формулы четырех веществ, образованных атомами:
1. водорода и
кислорода
2.азота и водорода
3.кальция и кислорода
4. углерода и кислорода
Слайд 12
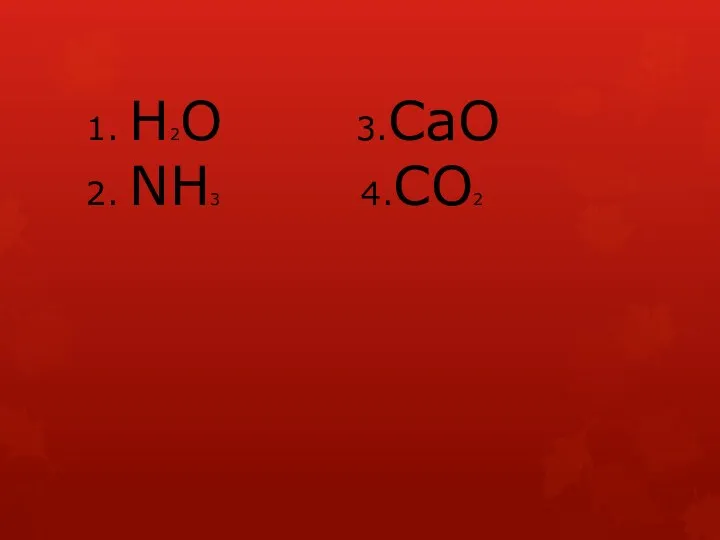
1. Н2О 3.СаО
2. NH3 4.CO2
Слайд 13

Слайд 14

Слайд 15

Слайд 16

Углекислый газ
В твердом состоянии-сухой лед















 Презентация (1)
Презентация (1) Аналитико-синтетическая переработка информации (АСПИ). Составление заголовков и библиографических описаний
Аналитико-синтетическая переработка информации (АСПИ). Составление заголовков и библиографических описаний Презентация Кто есть кто
Презентация Кто есть кто Развивающая игра Угадай эмоцию
Развивающая игра Угадай эмоцию Изложение на тему Зимний сон
Изложение на тему Зимний сон Технологии эксплуатации газовых и нефтяных скважин. Влияние свободного газа на работу ЭЦН
Технологии эксплуатации газовых и нефтяных скважин. Влияние свободного газа на работу ЭЦН Уголовная ответственность несовершеннолетних
Уголовная ответственность несовершеннолетних Десятичная запись дробных чисел
Десятичная запись дробных чисел Статус-отчет по проекту Строительство головного гидрографического лоцмейстерского судна ледового класса Arc7
Статус-отчет по проекту Строительство головного гидрографического лоцмейстерского судна ледового класса Arc7 Формирование универсальных учебных действий на занятиях объединения Занимательный английский
Формирование универсальных учебных действий на занятиях объединения Занимательный английский Методическая разработка Организация деятельности обучающихся в группах продленного дня Диск
Методическая разработка Организация деятельности обучающихся в группах продленного дня Диск Психологічне насильство над дітьми
Психологічне насильство над дітьми Veryu-ne_veryu_ot_02_02_2024
Veryu-ne_veryu_ot_02_02_2024 Нормативно-правовые документы и рекомендации, регламентирующие деятельность образовательных организаций
Нормативно-правовые документы и рекомендации, регламентирующие деятельность образовательных организаций Правда и ложь, или путешествие Лунтика в страну поЗНАЙка. § Что легче? В.А. Осеева Рассказ для детей про ложь
Правда и ложь, или путешествие Лунтика в страну поЗНАЙка. § Что легче? В.А. Осеева Рассказ для детей про ложь вышивка лентами
вышивка лентами Испарение воды листьями
Испарение воды листьями Наклонно направленные скважины
Наклонно направленные скважины День Земли
День Земли Самопрезентация на конкурс Учитель года
Самопрезентация на конкурс Учитель года Проверяем качество документов по охране труда
Проверяем качество документов по охране труда ООО ПИК-Энергия Единый щит
ООО ПИК-Энергия Единый щит ЕГЭ. Задание 25. Пишем сочинение
ЕГЭ. Задание 25. Пишем сочинение Новейший продукт на российском рынке - фитнес-ежедневник
Новейший продукт на российском рынке - фитнес-ежедневник Свободные и экономические блага
Свободные и экономические блага Транспорт Европы
Транспорт Европы 9cd9b985c8410b91
9cd9b985c8410b91 Ислам
Ислам