Содержание
- 2. * Al + I2 → AlI3 ν ν Взаимодействие с простыми веществами. б) с галогенами: Fe
- 3. * I. Взаимодействие с простыми веществами. в) с серой Al + S → Al2S3 (сульфид алюминия)
- 4. * II. Взаимодействие со сложными веществами. 1.Взаимодействие с водой до Mg; Al после Mg После Н
- 5. * II. Взаимодействие со сложными веществами. 2) Взаимодействие с солями CuSO4 + Fe → FeSO4 +
- 6. * II. Взаимодействие со сложными веществами. б) Ме + кислота = соль + вода + продукт
- 7. Cu0 + HN+5O3 (к) → Al + H2SO4 (k) →
- 8. Al + HNO3 (p) → Zn + HNO3 (k) →
- 10. Скачать презентацию





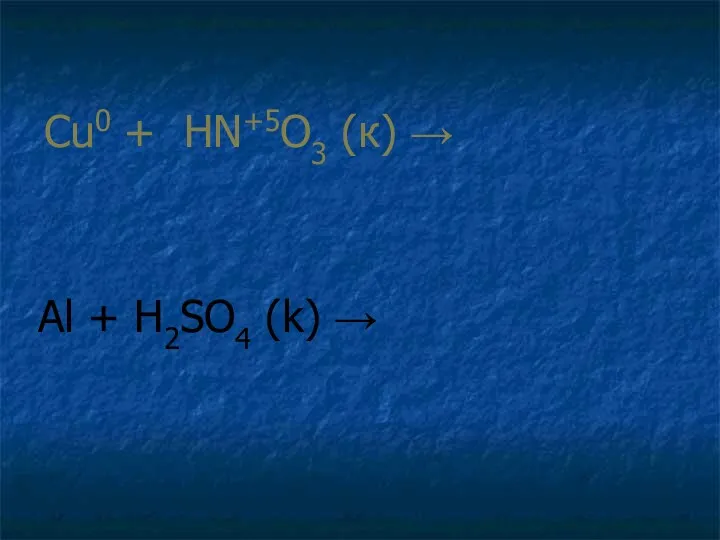
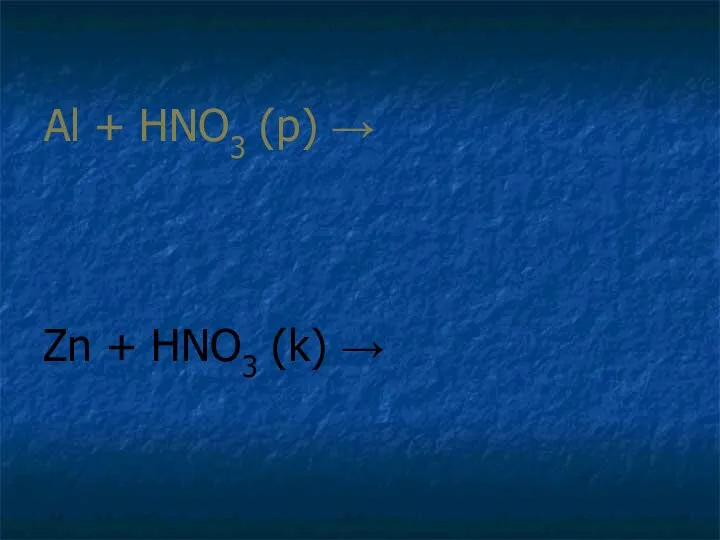
 Ұрықтың құрсақ ішілік дамуының тежелуі және жүктілікті жүргізу ерекшеліктері
Ұрықтың құрсақ ішілік дамуының тежелуі және жүктілікті жүргізу ерекшеліктері Творческий проект Приключения у новогодней елки
Творческий проект Приключения у новогодней елки Сенім дегеніміз не? Евр 11:1-2
Сенім дегеніміз не? Евр 11:1-2 мама
мама Профилактика виктимного поведения у обучающихся группы риска
Профилактика виктимного поведения у обучающихся группы риска Принципы построения отказоустойчивых информационных систем (ИС)
Принципы построения отказоустойчивых информационных систем (ИС) Циклические алгоритмы
Циклические алгоритмы Шаблон СГУ
Шаблон СГУ Библейские сказания. История Древнего мира
Библейские сказания. История Древнего мира Основы физиологии труда и комфортные условия жизнедеятельности
Основы физиологии труда и комфортные условия жизнедеятельности Новая линейка продуктов Micellife
Новая линейка продуктов Micellife Вода на земле
Вода на земле Внеурочная деятельность в 1 классе. Урок здоровья. Тема Наше здоровье
Внеурочная деятельность в 1 классе. Урок здоровья. Тема Наше здоровье A l’école
A l’école Акустика. Защита от шума. Акустическая перегородка. Материал на основе стеклянного штапельного волокна для звукоизоляции
Акустика. Защита от шума. Акустическая перегородка. Материал на основе стеклянного штапельного волокна для звукоизоляции Повышение эффективности работы компрессорной станции Еты - Пуровского месторождения
Повышение эффективности работы компрессорной станции Еты - Пуровского месторождения Люби и знай свой край родной
Люби и знай свой край родной Урок, география 6 класс Озера (ФГОС)
Урок, география 6 класс Озера (ФГОС) Презентация Мы - за здоровый образ жизни для проведения игры Поле чудес на внеурочной деятельности Здоровей-ка
Презентация Мы - за здоровый образ жизни для проведения игры Поле чудес на внеурочной деятельности Здоровей-ка Графические диктанты (Рисование по клеточкам) детям от 5 – 10 лет
Графические диктанты (Рисование по клеточкам) детям от 5 – 10 лет Беременность и роды при резус-несовместимости крови матери и плода
Беременность и роды при резус-несовместимости крови матери и плода Сервисный тренинг EXD06 Телефонный пакет rSAP Phaeton Телефонный пакет Touaregl
Сервисный тренинг EXD06 Телефонный пакет rSAP Phaeton Телефонный пакет Touaregl Изготовление ватных игрушек
Изготовление ватных игрушек Разработка рекомендаций по использованию солнечных батарей в условиях Республики Марий Эл
Разработка рекомендаций по использованию солнечных батарей в условиях Республики Марий Эл Общие сведения о полупроводниковых диодах (ППД)
Общие сведения о полупроводниковых диодах (ППД) Профилактика суицидальных тенденций среди несовершеннолетних в условиях урочной и внеурочной деятельности
Профилактика суицидальных тенденций среди несовершеннолетних в условиях урочной и внеурочной деятельности С Юбилеем, Любимый муж и папа!!!
С Юбилеем, Любимый муж и папа!!! Обобщающий урок по теме Африка. География. 7 класс
Обобщающий урок по теме Африка. География. 7 класс