Слайд 2

Степень окисления. Составление формул бинарных соединений.
8 класс.
Слайд 3

Цели урока:
1. Дать понятие степень окисления.
2. Научить рассчитывать степени
окисления по формулам бинарных соединений и составлять химические формулы по с.о.
3. Дать первоначальные представления о номенклатуре химических соединений.
4. Формировать химически правильную речь.
5. Содействовать формированию научного мировоззрения, нравственности.
Слайд 4

Степень окисления
– соответствует числу отданный, принятых или смещенных электронов.
Слайд 5

I.Степень окисления для веществ с различными видами связи.
Слайд 6

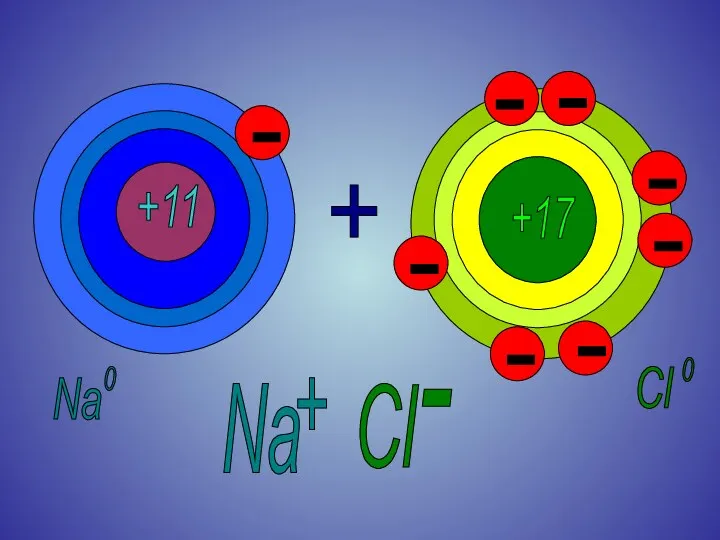
Степень окисления
для веществ с ионной связью
на примере NaCl.
Слайд 7
Слайд 8

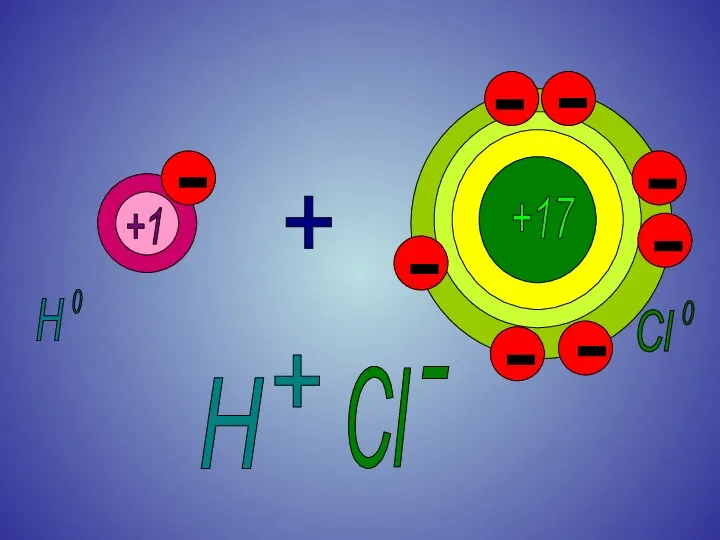
Степень окисления
для веществ с КПС
на примере HCl.
Слайд 9
Слайд 10

Степень окисления для простых веществ.
Слайд 11
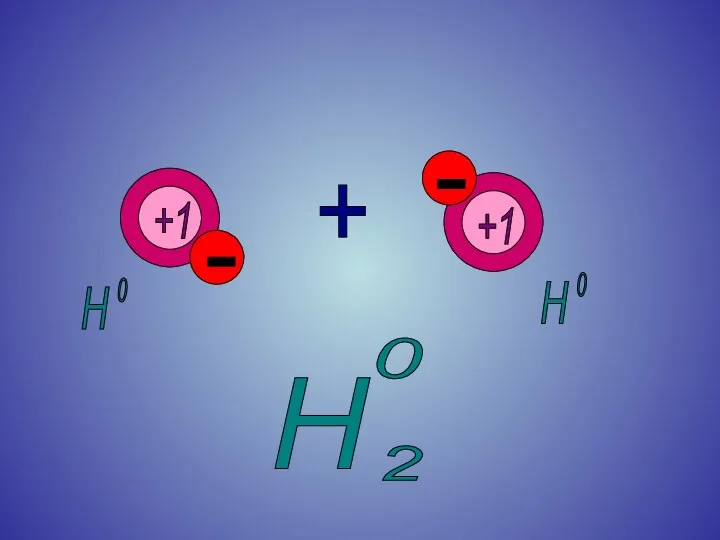
Слайд 12

II.Определение
степени окисления в бинарных соединениях.
Слайд 13

Определим основные ЗАКОНОМЕРНОСТИ.
Слайд 14
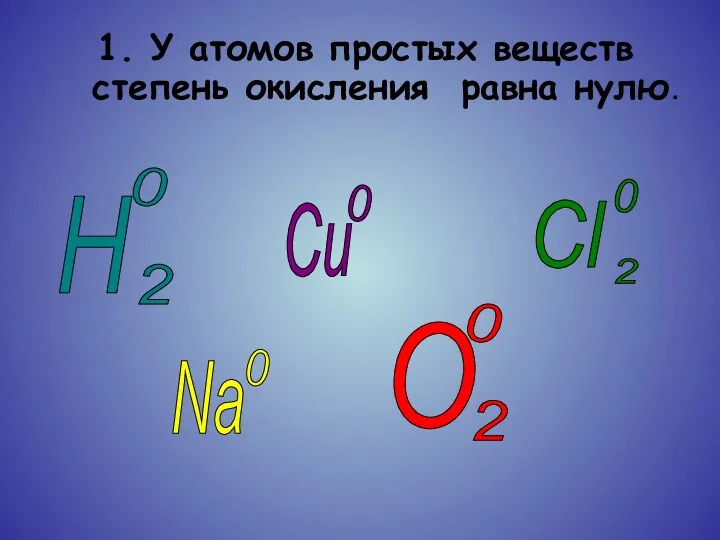
1. У атомов простых веществ степень окисления равна нулю.
0
2
H
0
Cl
2
0
Cu
0
Na
Слайд 15

2. Степень окисления бывает:
Положительная
Отрицательная
Нулевая
+
Na
+2
Сa
+3
Al
0
2
H
0
Na
Cl
-
Слайд 16

3. Для более
электроотрицательного атома степень окисления высчитывают, как
№ группы
- 8
Слайд 17

Воспользуемся
Алгоритмом №1
для определения
степеней окисления.
Слайд 18

Например:
O
3
6-8=-2
-2
x
-6
+6
S
Слайд 19

Выполните задание №1 из Листов заданий.
Проверьте получившийся результат:
+4 -2 +4
-2 +7 -2 +6 -2
CO2, NO2, Cl2O7, CrO3
+4 -4 +4 -4 +14 -14 +6 -6
Слайд 20

III.Составление формул по степеням окисления.
Слайд 21

Воспользуемся
Алгоритмом №2
для составления формул.
Слайд 22
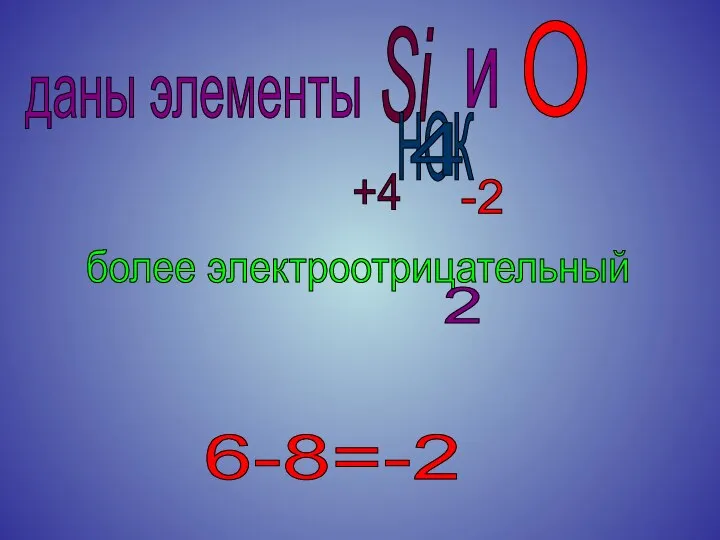
даны элементы
более электроотрицательный
Si
O
и
6-8=-2
-2
+4
НОК
4
2
Слайд 23

Выполните задание №2 из Листов заданий.
Проверьте получившийся результат:
НОК НОК НОК
6 6 5
+2 -3 +3 -2 +5 -
Mg N , Al S , PCl ,
3
2
2
3
5
Слайд 24

IV.Номенклатура бинарных соединений.
Слайд 25

Слайд 26

Воспользуемся
Правилами номенклатуры бинарных соединений.
Слайд 27

Для названия веществ воспользуйтесь таблицей
«Корни латинских названий некоторых элементов»
Слайд 28

FeS
CrCl
3
P O
2
5
Na N
3
CaH
2
-
-
-
-
-
сульфид железа
хлорид хрома
гидрид кальция
нитрид натрия
оксид фосфора
(II)
(III)
(V)
Выполните задание №3
из Листов заданий.
Слайд 29

Домашнее задание.
§ 17 читать, упр 2 письменно.









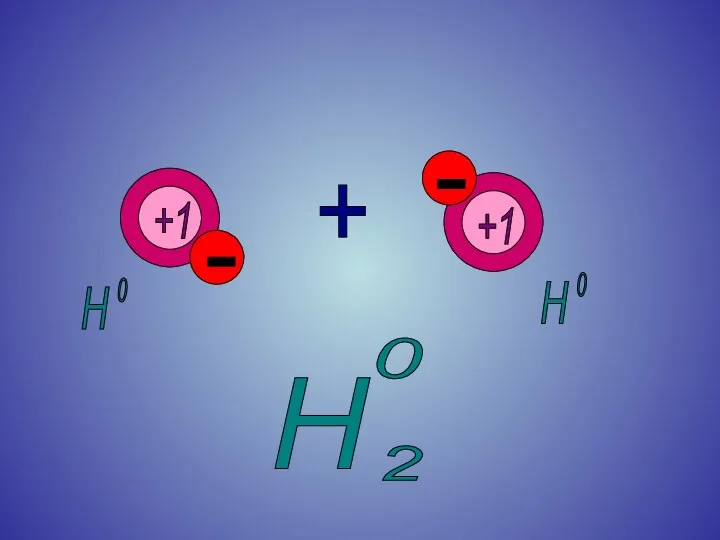










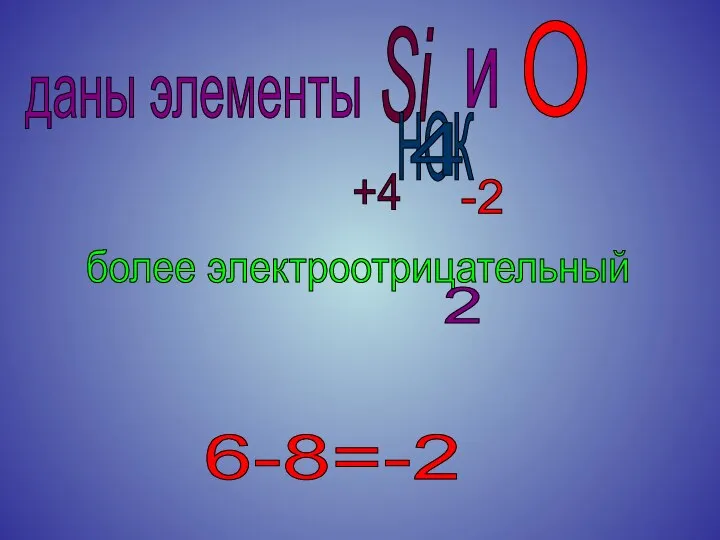







 Математическая система Mathcad. Компьютерные технологии решения математических задач
Математическая система Mathcad. Компьютерные технологии решения математических задач Викторина по произведениям Корнея Чуковского. (Презентация)
Викторина по произведениям Корнея Чуковского. (Презентация) Моделирование системы управления качеством организации дополнительного образования детей
Моделирование системы управления качеством организации дополнительного образования детей Мое увлечение - каратэ. Фотоальбом
Мое увлечение - каратэ. Фотоальбом 20230924_zadanie_123
20230924_zadanie_123 презентация кабинета физики
презентация кабинета физики Разработка технологии получения отливки
Разработка технологии получения отливки Вища освіта України в європейському просторі вищої освіти та наукових досліджень
Вища освіта України в європейському просторі вищої освіти та наукових досліджень Физические свойства древесины
Физические свойства древесины Презентация мини-музея Наш верный друг-собака
Презентация мини-музея Наш верный друг-собака Өрт сөндіру поездары
Өрт сөндіру поездары Мобильная торговля
Мобильная торговля Синтоизм
Синтоизм Ассортимент и оценка качества чая. Оргонолептические методы исследования
Ассортимент и оценка качества чая. Оргонолептические методы исследования Спасение, вера, покаяние и рождение свыше
Спасение, вера, покаяние и рождение свыше Возрастные особенности детей и подростков. Врачебный контроль за состоянием здоровья школьников
Возрастные особенности детей и подростков. Врачебный контроль за состоянием здоровья школьников Великая Отечественная Война
Великая Отечественная Война Календарь и его виды
Календарь и его виды Изменения в жизни людей и животных зимой
Изменения в жизни людей и животных зимой Проект Мы в ответе за тех кого приручили
Проект Мы в ответе за тех кого приручили Презентация Развитие мелкой моторики руки
Презентация Развитие мелкой моторики руки класс ТЕХН Колодец
класс ТЕХН Колодец Методы обнаружения утечек в магистральных нефтепроводах
Методы обнаружения утечек в магистральных нефтепроводах Гражданская оборона в современном мире
Гражданская оборона в современном мире СОЛНЫШКО, МАМА И ПАПА.
СОЛНЫШКО, МАМА И ПАПА. Проект по профессиям Южного Урала – профессия Репортер!
Проект по профессиям Южного Урала – профессия Репортер! Прокуратура России - 300 лет на страже закона
Прокуратура России - 300 лет на страже закона Жилой дом. Этапы строительства
Жилой дом. Этапы строительства