Содержание
- 2. четвертый по распространенности в земной коре, второй среди металлов Fe элемент № 26 в периодической системе
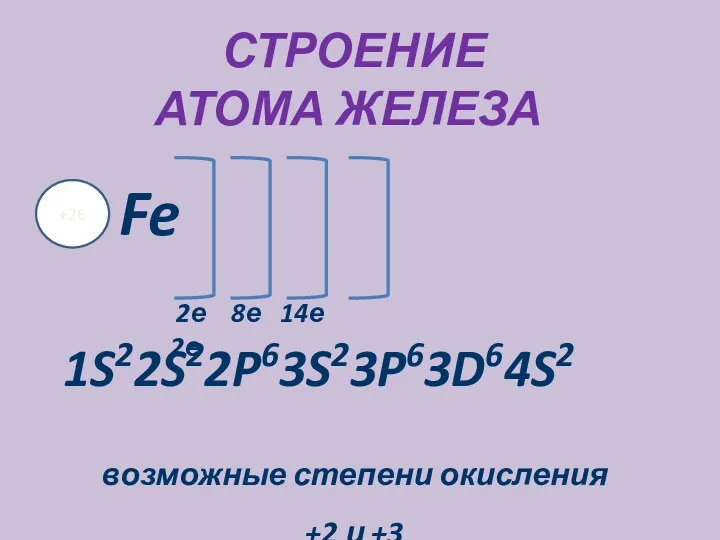
- 3. строение атома железа +26 Fe 2е 8е 14е 2е 1S22S22P63S23P63D64S2 возможные степени окисления +2 и +3
- 4. Железо в природе В земной коре на долю железа приходится около 4,1% массы земной коры (4-е
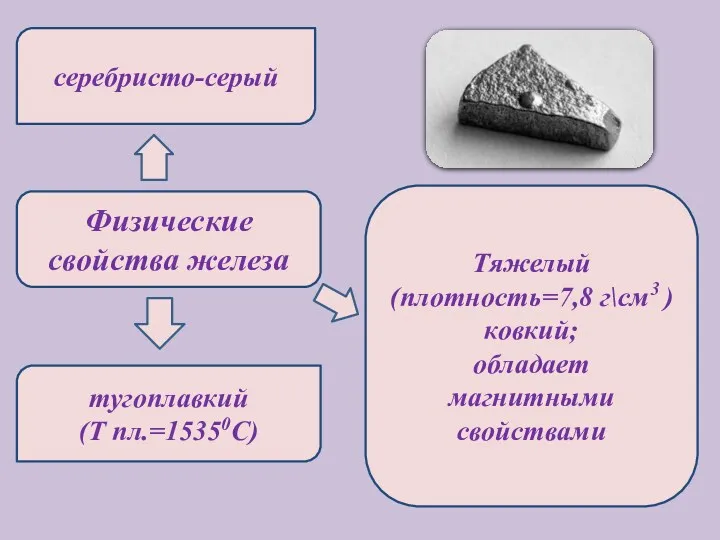
- 5. Физические свойства железа серебристо-серый тугоплавкий (Т пл.=15350C) Тяжелый (плотность=7,8 г\см3 ) ковкий; обладает магнитными свойствами
- 6. Химические свойства Реакции с простыми веществами Железо сгорает в кислороде при нагревании: 4Fe +3O2=2Fe2O3 Реагирует с
- 7. Химические свойства Реакции со сложными веществами С кислотами: А) с соляной кислотой 2HCL + Fe =
- 8. 4Fe + 2Н2О + ЗО2 = 2(Fe2O3•Н2О) Железо разрушается под действием окружающей среды, т.е. подвергается коррозии
- 10. Скачать презентацию





 презентация урока 10 класс Альдегиды
презентация урока 10 класс Альдегиды Этносоциология. Предметная область єтнической социологии
Этносоциология. Предметная область єтнической социологии Телефония и компьютер
Телефония и компьютер 20190917_11prezentatsiya_k_uroku_10_klass
20190917_11prezentatsiya_k_uroku_10_klass Респираторные аллергозы у детей
Респираторные аллергозы у детей ГЭС обязана стоять так же незыблемо, как египетские пирамиды
ГЭС обязана стоять так же незыблемо, как египетские пирамиды 20231023_tehnologiya_razvitiya_kriticheskogo_myshleniya_cherez_smyslovoe_chtenie_miheeva_v.v._2
20231023_tehnologiya_razvitiya_kriticheskogo_myshleniya_cherez_smyslovoe_chtenie_miheeva_v.v._2 84-я Всероссийская научная конференция с международным участием Вопросы теоретической и практической медицины
84-я Всероссийская научная конференция с международным участием Вопросы теоретической и практической медицины Экономический кризис 1998 года
Экономический кризис 1998 года Лекция 5__
Лекция 5__ Презентация Исторический музей
Презентация Исторический музей X Powerpoint Template_Dark
X Powerpoint Template_Dark Спортивные мероприятия. Школьные соревнования
Спортивные мероприятия. Школьные соревнования Электрическая схема тепловоза ТЭМ-18Д
Электрическая схема тепловоза ТЭМ-18Д Средства, влияющие на функции органов пищеварения
Средства, влияющие на функции органов пищеварения 20231023_ekologiya_i_literatura_1
20231023_ekologiya_i_literatura_1 Методы исследования слуха
Методы исследования слуха To say, to tell, to speak, to talk
To say, to tell, to speak, to talk презентация к уроку технология УМК Гармония 1 класс
презентация к уроку технология УМК Гармония 1 класс Всероссийский конкурс исследовательских краеведческих работ учащихся Отечество.
Всероссийский конкурс исследовательских краеведческих работ учащихся Отечество. Тема 2: Военнослужащие и взаимоотношения между ними
Тема 2: Военнослужащие и взаимоотношения между ними Внеклассное мероприятие Вся семья вместе, так и душа на месте
Внеклассное мероприятие Вся семья вместе, так и душа на месте Методическая разработка занятия в ГПД для развития мелкой моторики и творческих способностей учащихся
Методическая разработка занятия в ГПД для развития мелкой моторики и творческих способностей учащихся Использование нестандартного оборудования в физкультурно – оздоровительной работе в детском дошкольном учреждении
Использование нестандартного оборудования в физкультурно – оздоровительной работе в детском дошкольном учреждении Виды работы с текстом учебника на разных ступенях обучения
Виды работы с текстом учебника на разных ступенях обучения Риджионализм. Период наибольшего расцвета
Риджионализм. Период наибольшего расцвета Нация и этнос. Становление и развитие теоретических положений в мировой и российской этнологии
Нация и этнос. Становление и развитие теоретических положений в мировой и российской этнологии Новый империализм. Происхождение Первой мировой войны
Новый империализм. Происхождение Первой мировой войны