Слайд 2
Слайд 3

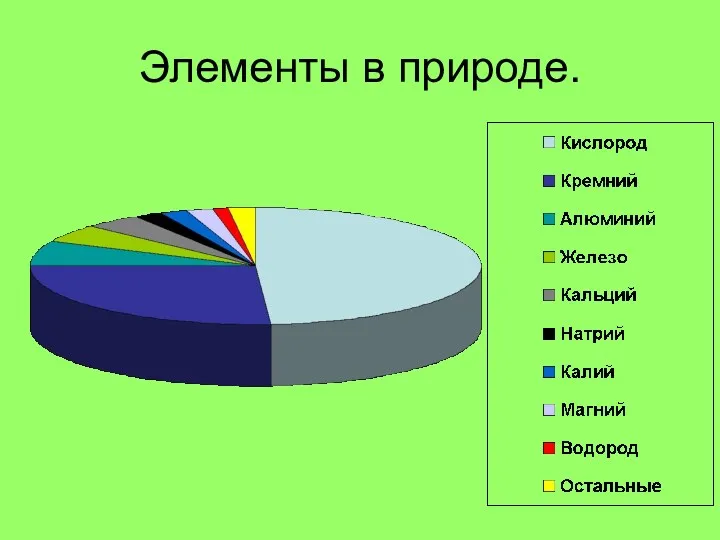
Нахождение в природе.
Самородные элементы
Сера
Графит С
Алмаз С
Азот и кислород, инертные газы
в составе воздуха
Слайд 4

Нахождение в природе
← Апатиты Р
Галит NaCl →
← FeS2 пирит
Кварц SiO2 →
Слайд 5

Неметаллы - это химические элементы, которые могут проявлять свойства как окислителя
( принимают электроны), так и восстановителя (отдают электроны).
НеМ – элементы с высокой ОЭО (2 - 4)
Исключения : фтор – только окислитель,
инертные газы – могут только отдавать электроны.
Гелий, неон и аргон – соединений не образуют.
Слайд 6

Соединения неметаллов.
Оксиды – только кислотные
SO3, SO2, CO2 и другие.
(кроме NO
и CO –безразличные)
Гидроксиды – только кислоты
H2SO4, H2SO3,H2CO3 и другие
Образуют летучие соединения с водородом HCl, NH3…
Слайд 7
Слайд 8

Слайд 9

Слайд 10

Слайд 11

Слайд 12

Слайд 13
Строение атомов НеМ
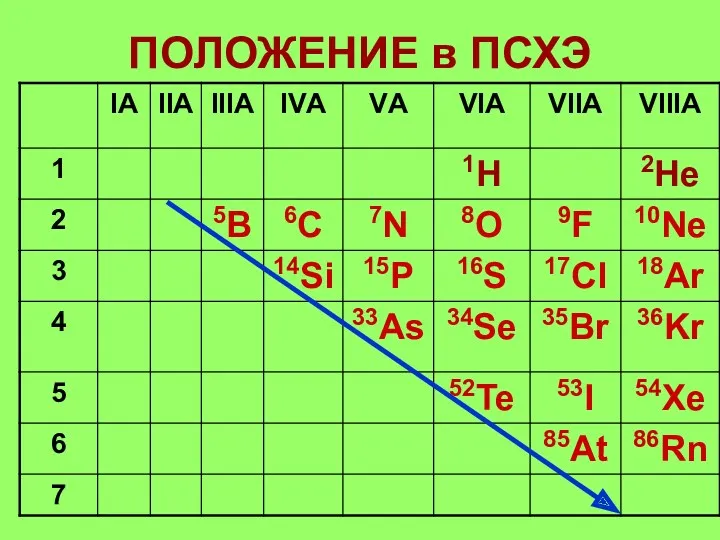
1. Элементы расположены в главных подгруппах III –VIII групп
(А).
2. На последнем уровне 3 – 7(8) электронов.
3. Радиус атома уменьшается
растёт
4. Неметаллические свойства
В периоде – увеличиваются
В группе - уменьшаются
Слайд 14

Строение атомов НеМ
5. Высокая электроотрицательность.
6. Принимают электроны и отдают.
7. НеМ →
кислотный оксид→кислота
8. Летучие водородные соединения
(кислоты, основания и безразличные)
Слайд 15

Физические свойства
Агрегатное состояние.
Газообразные – азот, кислород, хлор, инертные газы, водород.
Жидкий
– бром,
Твёрдые – сера, фосфор, углерод…
Растворимость в воде.
Нерастворимы.
Отношение к электрическому току.
Неэлектропроводные: сера, кислород…
Проводники: графит
Полупроводники: кремний
Слайд 16

Строение неметаллов.
Молекулярное (НеМ), где
Инертные газы He, Ar, Ne…
H2, Cl2, N2…
P4
белый
Pn красный
Атомное строение
(С)n -алмаз, графит;
(Si)n кремний;
(B)n бор
Слайд 17

Кислород, водород – пример газообразных бесцветных неметаллов
Слайд 18

Большинство неметаллов имеют твёрдое агрегатное состояние
Сера – кристаллическое вещество жёлтого цвета
Красный
Слайд 19

Неметаллы малорастворимы в воде
Уголь
Фосфор
Сера не смачивается водой


















 Шаблон курсового проекта
Шаблон курсового проекта Использование ИКТ в образовательном пространстве ДОУ
Использование ИКТ в образовательном пространстве ДОУ Тема: Здоровый образ жизни.
Тема: Здоровый образ жизни. Волоховой
Волоховой Реконструкция подстанции 110/10 кВ с разработкой релейной защиты силового трансформатора
Реконструкция подстанции 110/10 кВ с разработкой релейной защиты силового трансформатора Программа по внеурочной деятельности пректного направления Мой родной край
Программа по внеурочной деятельности пректного направления Мой родной край Презентация Виды работы с текстом учебника географии
Презентация Виды работы с текстом учебника географии Лучевая диагностика туберкулеза органов дыхания
Лучевая диагностика туберкулеза органов дыхания Презентация Механизм взаимодействия учителя-логопеда с педагогом-психологом и социальным педагогом в рамках деятельности ПМПконсилиума общеобразовательной организации
Презентация Механизм взаимодействия учителя-логопеда с педагогом-психологом и социальным педагогом в рамках деятельности ПМПконсилиума общеобразовательной организации Презентация к уроку 70 лет со дня освобождения Кубани от фашистских захватчиков
Презентация к уроку 70 лет со дня освобождения Кубани от фашистских захватчиков презентация к уроку Географическое положение Африки
презентация к уроку Географическое положение Африки Первоклассник
Первоклассник Под знаком двойной розы. Англия при Тюдорах
Под знаком двойной розы. Англия при Тюдорах презентацияАзбука нравственности
презентацияАзбука нравственности Вторая Мировая война. Тихоокеанский фронт
Вторая Мировая война. Тихоокеанский фронт Рождение протестантизма православия
Рождение протестантизма православия Витамин В-12. Дефицитная анемия
Витамин В-12. Дефицитная анемия Природные зоны Австралии
Природные зоны Австралии Сити-фермер - профессия будущего
Сити-фермер - профессия будущего Зажимные устройства технологической оснастки и их расчёт
Зажимные устройства технологической оснастки и их расчёт Химический состав клетки. (9 класс)
Химический состав клетки. (9 класс) бизнес план
бизнес план Саул. Царственные задатки и непослушание, гордость, зависть
Саул. Царственные задатки и непослушание, гордость, зависть Центральная и осевая симметрии презентации по геометрии для 8АВ
Центральная и осевая симметрии презентации по геометрии для 8АВ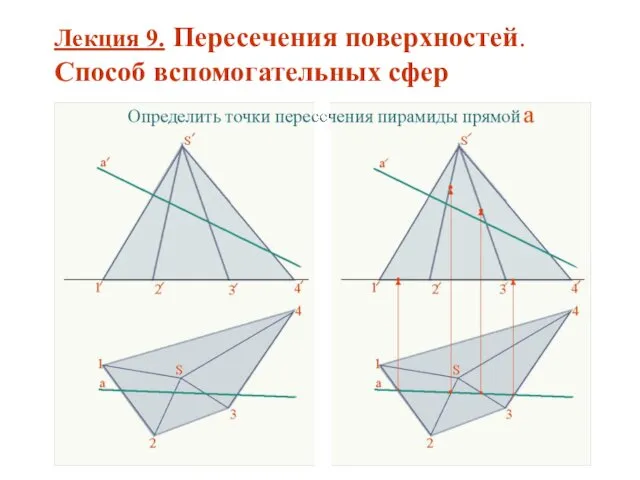 Пересечения поверхностей. Способ вспомогательных сфер. (Лекция 9)
Пересечения поверхностей. Способ вспомогательных сфер. (Лекция 9) Атлас педагогических идей
Атлас педагогических идей Слесарное дело. Тест
Слесарное дело. Тест Век медный, бронзовый, железный. Презентация к уроку химии 9 класс.
Век медный, бронзовый, железный. Презентация к уроку химии 9 класс.