Содержание
- 2. Цель урока: 1. Познакомить учащихся с новым классом неорганических соединений – основаниями. 2. Рассмотреть классификацию, состав
- 3. ЗНАЧЕНИЕ ОСНОВАНИЙ Основания – один из классов неорганических веществ, который наряду с кислотами, оксидами и солями
- 4. План изучения темы: Состав, названия и определение оснований. Классификация оснований. Индикаторы. Физические свойства оснований, их значение
- 5. Определение. Номенклатура. Основания – это сложные вещества, состоящие из ионов металлов и связанных с ними гидроксид-ионов.
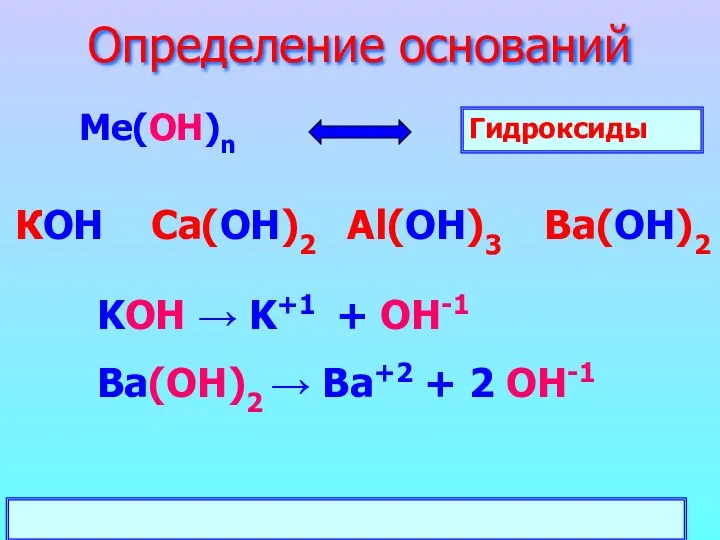
- 6. Определение оснований Ме(ОН)n КОН Ca(ОН)2 Al(ОН)3 Ba(ОН)2 Гидроксиды KOH → K+1 + OH-1 Ba(ОН)2 → Ba+2
- 7. Физкультминутка
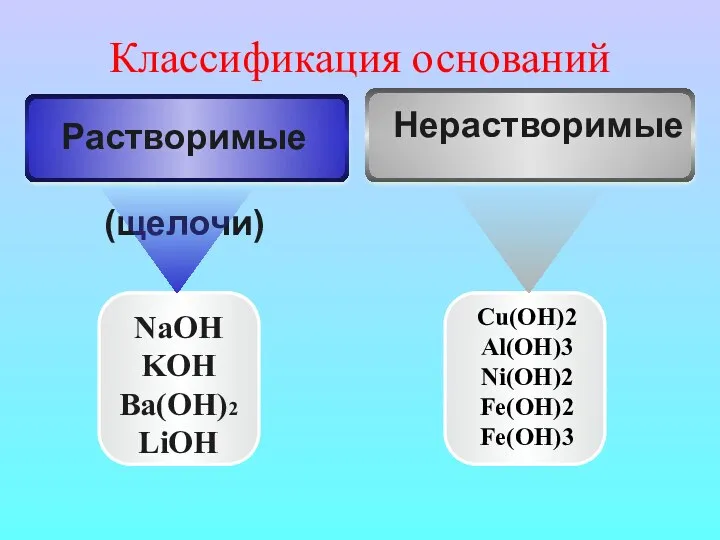
- 8. Классификация оснований NaOH KOH Ba(OH)2 LiOH Cu(OH)2 Al(OH)3 Ni(OH)2 Fe(OH)2 Fe(OH)3 Нерастворимые Растворимые (щелочи)
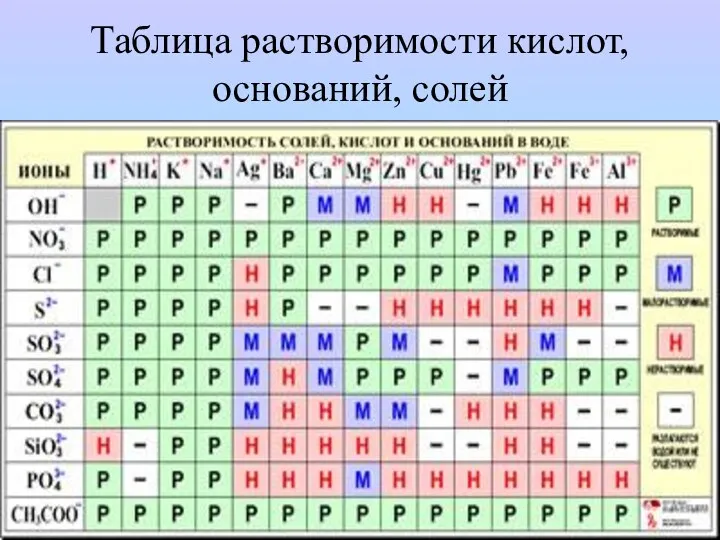
- 9. Таблица растворимости кислот, оснований, солей
- 10. Соблюдайте правила ТБ при обращении с основаниями Растворимые основания – щелочи – могут вызвать химический ожог
- 11. Что делать? В случае попадания щелочи на одежду или участок кожи следует немедленно сообщить учителю о
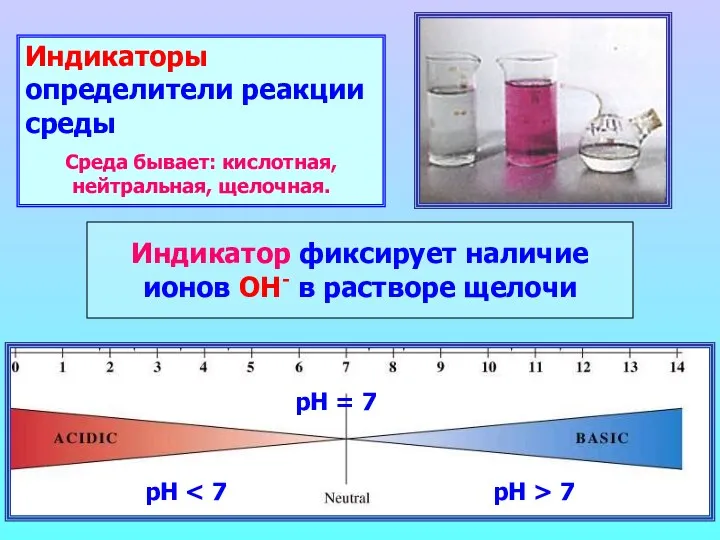
- 12. Индикаторы определители реакции среды Среда бывает: кислотная, нейтральная, щелочная. Индикатор фиксирует наличие ионов ОН- в растворе
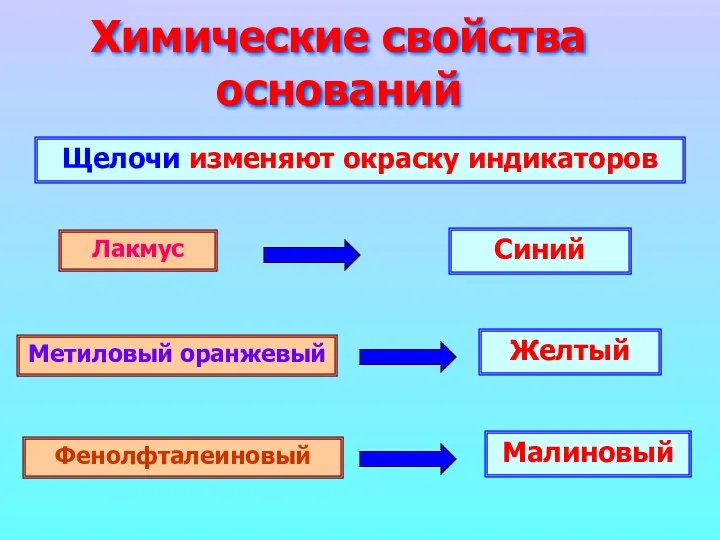
- 13. Химические свойства оснований Щелочи изменяют окраску индикаторов Лакмус Метиловый оранжевый Фенолфталеиновый Синий Желтый Малиновый
- 14. Гидроксид кальция Ca(OH)₂ (гашеная известь)
- 15. Гидроксид калия KOH (едкое кали)
- 16. Гидроксид натрия NaOH (натр едкий, каустическая сода )
- 17. Применение: LiOH – в аккумуляторах. NaOH – для очистки нефти, производства мыла, в текстильной промышленности, для
- 18. Закрепление 1. Что такое основание, общая формула? 2. Какими по растворимости бывают основания? 3. Как называются
- 19. Тест «Пятерочка» 1. Выберите формулы оснований: а) SO3 б) Mg(OH)2 в) H2SO4 г) СаО 2. К
- 20. Ответы 1. б 2. в 3. б 4. а 5. а
- 21. Ответьте на вопросы: Как работал на уроке? Какую (и почему) ставлю себе оценку? – мнение ученика
- 23. Скачать презентацию















 Осложнения и аварии в бурении
Осложнения и аварии в бурении Бумажная аппликация
Бумажная аппликация Синтез систем автоматического управления
Синтез систем автоматического управления Чувашская легенда
Чувашская легенда Самарская региональная общественная еврейская благотворительная организация. Курсы иврита
Самарская региональная общественная еврейская благотворительная организация. Курсы иврита Презентация по теме Работа по развитию мелкой моторики в системе здоровьесберегающих технологий
Презентация по теме Работа по развитию мелкой моторики в системе здоровьесберегающих технологий Лекарственные поражения печени
Лекарственные поражения печени Слайды
Слайды PartnerPlusBenefit - специальная бонусная программа для малых и средних предприятий
PartnerPlusBenefit - специальная бонусная программа для малых и средних предприятий Словосочетание
Словосочетание О мерах противодействия распространения ВИЧ-инфекции на территории города Вологды
О мерах противодействия распространения ВИЧ-инфекции на территории города Вологды Компьютерные игры. Советы для родителей.
Компьютерные игры. Советы для родителей. Новый год и Рождество в разных странах
Новый год и Рождество в разных странах Учение с увлечением!
Учение с увлечением! Религия в современном мире. Религиозные объединения и организации в Российской Федерации
Религия в современном мире. Религиозные объединения и организации в Российской Федерации Музыка в стиле джаз
Музыка в стиле джаз Упражнения для закрепления правильного употребления в речи предлогов.
Упражнения для закрепления правильного употребления в речи предлогов. Францияның еңбек туралы заңы
Францияның еңбек туралы заңы Презентация Какие растения самые важные
Презентация Какие растения самые важные Евреи (иудеи)
Евреи (иудеи) Инструктаж по поведению на льду
Инструктаж по поведению на льду Зачарована Десна (1956) - автобіографічна повість, спогади Олександра Довженка
Зачарована Десна (1956) - автобіографічна повість, спогади Олександра Довженка МИНИ МУЗЕЙ В ГРУППЕ РАННЕГО ВОЗРАСТА ТЕМА № 2 В ГОСТЯХ У СКАЗКИ Диск Диск
МИНИ МУЗЕЙ В ГРУППЕ РАННЕГО ВОЗРАСТА ТЕМА № 2 В ГОСТЯХ У СКАЗКИ Диск Диск Правила оформления презентации
Правила оформления презентации Борис Пастернак (1890-1960)
Борис Пастернак (1890-1960) Посвящается выпускникам 2020 года …
Посвящается выпускникам 2020 года … Телевизоры. Ключевые характеристики
Телевизоры. Ключевые характеристики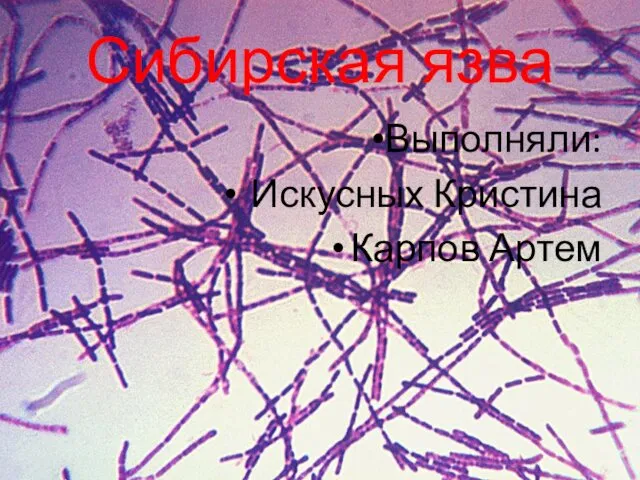 Сибирская язва
Сибирская язва