Содержание
- 2. «Немало сера знаменита, И в древности ее Гомер воспел, С ней много тысяч лет прожито, И
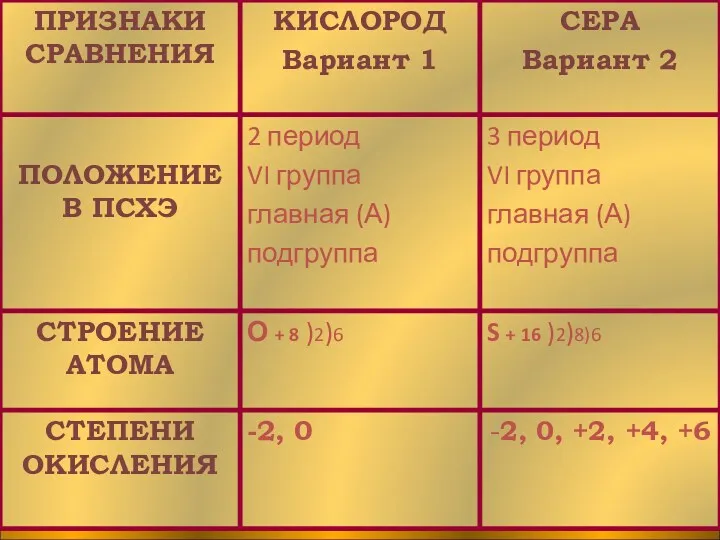
- 4. СЕРА Химические свойства Положение в Периодической системе химических элементов Физические свойства Нахождение в природе Применение серы
- 6. nº=16 p+=16 ē=16 Z=+16 Степени окисления серы: −2 (окислительные свойства); 0; +2, +4, +6 (восстановительные свойства).
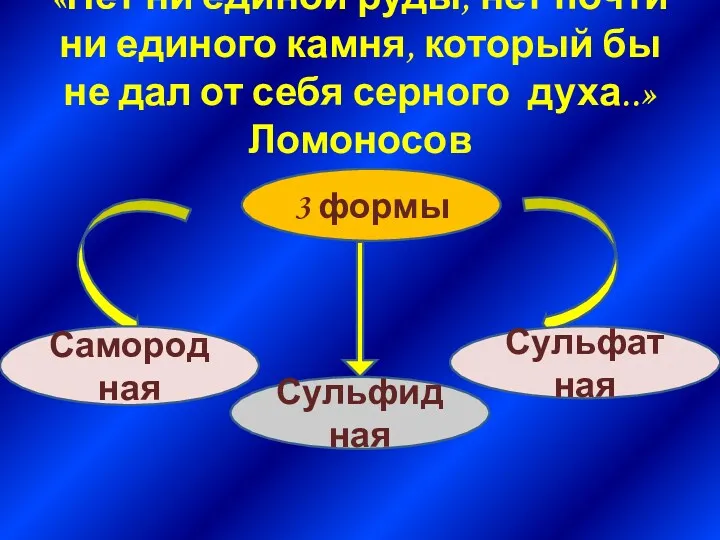
- 7. «Нет ни единой руды, нет почти ни единого камня, который бы не дал от себя серного
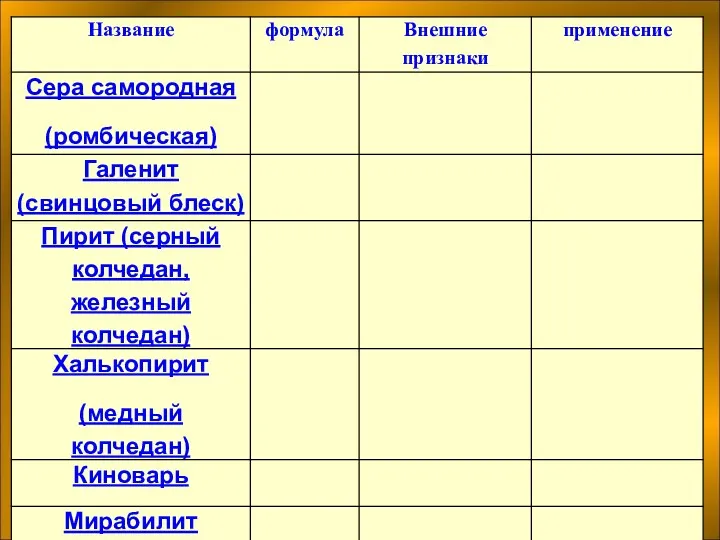
- 9. Сера самородная
- 10. Галенит (свинцовый блеск)
- 11. ПИРИТ - FeS2
- 12. ХАЛЬКОПИРИТ - CuFeS2.
- 13. КИНОВАРЬ - HgS.
- 14. МИРАБИЛИТ - Na2SO4 • 10H2O
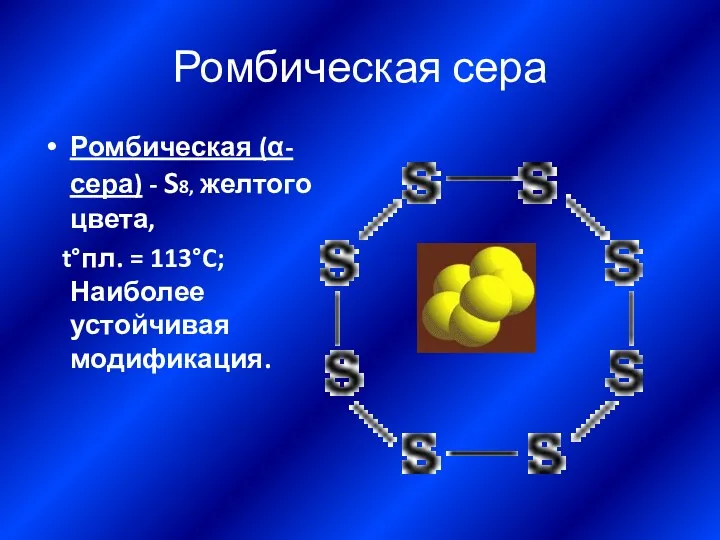
- 16. Ромбическая сера Ромбическая (α-сера) - S8, желтого цвета, t°пл. = 113°C; Наиболее устойчивая модификация.
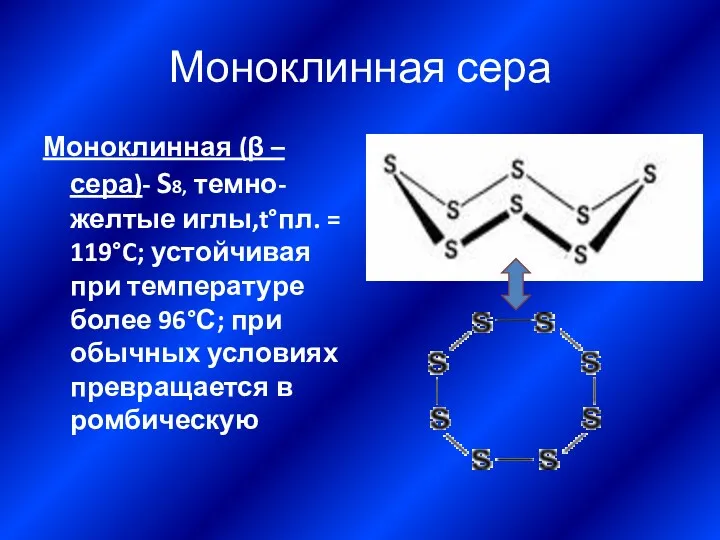
- 17. Моноклинная сера Моноклинная (β –сера)- S8, темно-желтые иглы,t°пл. = 119°C; устойчивая при температуре более 96°С; при
- 18. Пластическая сера Пластическая сера- коричневая резиноподобная (аморфная) масса. Она неустойчива и через некоторое время становится хрупкой,
- 19. Физические свойства Рассмотрите образец серы, определите: Агрегатное состояние; Цвет; Растворимость в воде (опустите кусочек серы в
- 20. Флотация –это (фр. flottation, от flotter — плавать) — процесс разделения мелких твёрдых частиц (главным образом,
- 21. Химические свойства серы окислительные восстановительные
- 22. ДЕМЕРКУРИЗАЦИЯ (от франц. démercurisation
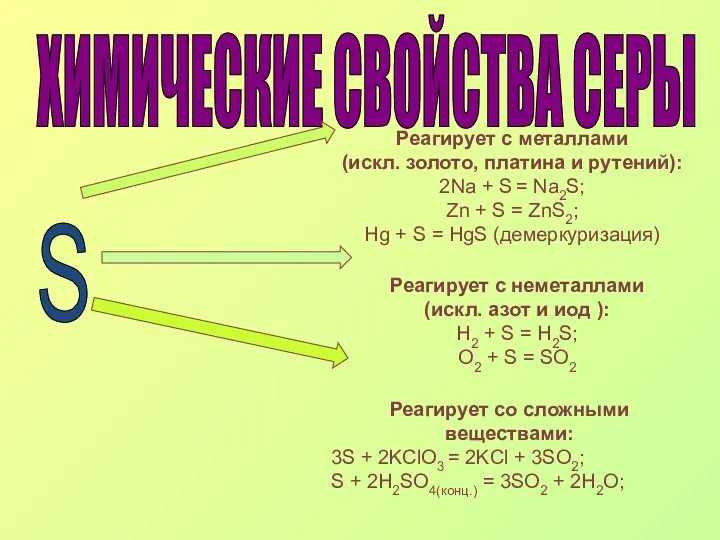
- 23. ХИМИЧЕСКИЕ СВОЙСТВА СЕРЫ S Реагирует с металлами (искл. золото, платина и рутений): 2Na + S =
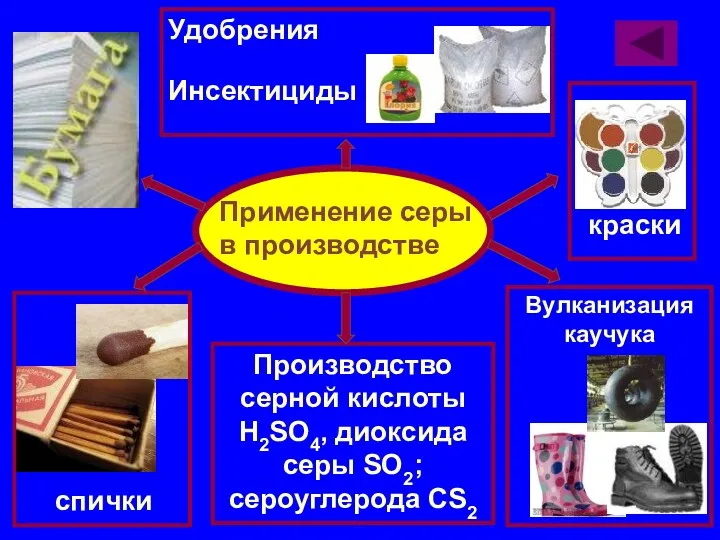
- 24. Применение серы в производстве Производство серной кислоты H2SO4, диоксида серы SO2; сероуглерода CS2 Удобрения Инсектициды краски
- 26. Скачать презентацию













 Буддизм в России
Буддизм в России Проект Подарок маме презентация
Проект Подарок маме презентация Готовность сельской базовой школы к реализации ФГОс
Готовность сельской базовой школы к реализации ФГОс Европейские нормативы теплозащиты зданий. Технологии теплозащиты и естественной вентиляции архитектурных сооружений в Казахстане
Европейские нормативы теплозащиты зданий. Технологии теплозащиты и естественной вентиляции архитектурных сооружений в Казахстане Ценообразование в условиях монополии
Ценообразование в условиях монополии Музика античності
Музика античності Серебро. Текущая динамика и перспективы на 2021 г
Серебро. Текущая динамика и перспективы на 2021 г Учитель года России-2016
Учитель года России-2016 Внеклассное мероприятие для младших школьников. День Петра и Февронии
Внеклассное мероприятие для младших школьников. День Петра и Февронии Информация для размышления Вредные привычки.
Информация для размышления Вредные привычки. Костюмы в стиле Стимпанк
Костюмы в стиле Стимпанк Побочные эффекты антипсихотических препаратов
Побочные эффекты антипсихотических препаратов Сергиев Посад
Сергиев Посад Изоляция газопровода
Изоляция газопровода Алгебра высказываний. Решение логических задач
Алгебра высказываний. Решение логических задач Почки. Опухоль правой почки больших размеров
Почки. Опухоль правой почки больших размеров Перелетные птицы.
Перелетные птицы. Конституция РФ – гарант свобод и прав народных
Конституция РФ – гарант свобод и прав народных презентация проекта Мастерская Самоделкина
презентация проекта Мастерская Самоделкина Профориентационные мероприятия школьников
Профориентационные мероприятия школьников Организация междугородных автобусных перевозок
Организация междугородных автобусных перевозок AROMAgroup. Рекомендованные ароматы
AROMAgroup. Рекомендованные ароматы Роторный экскаватор
Роторный экскаватор Строительные материалы. Строение и основные свойства строительных материалов
Строительные материалы. Строение и основные свойства строительных материалов Градация лекал деталей одежды
Градация лекал деталей одежды Сексуалды мәдениет. Денсаулығында ақауы бар индивидтерді тұлға түрінде гигеналық және жыныстық тәрбиелеу әлеуметтік үрдіс
Сексуалды мәдениет. Денсаулығында ақауы бар индивидтерді тұлға түрінде гигеналық және жыныстық тәрбиелеу әлеуметтік үрдіс Общая характеристика элементов главной подгруппы II группы.
Общая характеристика элементов главной подгруппы II группы. Китайская Народная Республика в 1949-2007 г.г
Китайская Народная Республика в 1949-2007 г.г