Содержание
- 2. пластическая сера (Sn) кристаллическая сера (S8) Физические свойства серы. Химический элемент сера (S) Аллотропия – явление
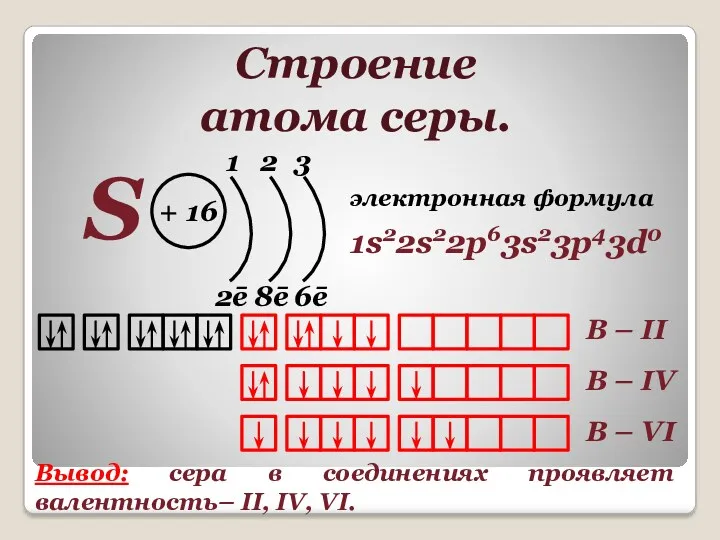
- 3. Строение атома серы. S 1 2 3 2ē 8ē 6ē 1s22s22p63s23p43d0 электронная формула В – II
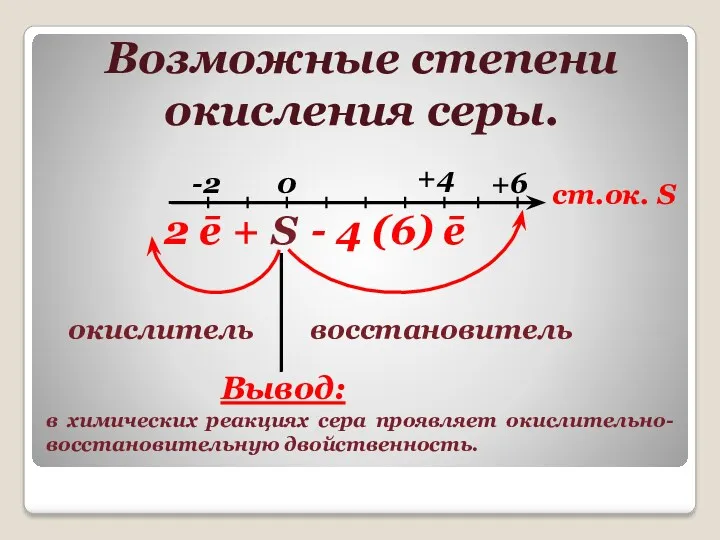
- 4. Возможные степени окисления серы. ст.ок. S -2 0 +4 +6 S - 4 (6) ē 2
- 5. Химические свойства серы. S – окислитель Ме + S → MeS Н2 + S → H2S
- 6. производство лекарственных препаратов вулканизация каучука (производство резины) производство спичек производство серной кислоты Применение серы. S -
- 7. Проверь себя! 1. Функция серы в окислительно-восстановительном процессе: а) S0 - 4ē → S+4 б) S0
- 9. Скачать презентацию




 Трудности адаптации первоклассников в школе.
Трудности адаптации первоклассников в школе. Осенние именинники 2 класс
Осенние именинники 2 класс Литовская сказка Мальчик золотой хохолок и девочка золотая коса
Литовская сказка Мальчик золотой хохолок и девочка золотая коса Безусловное принятие
Безусловное принятие Виталий Бианки. Лесные домишки
Виталий Бианки. Лесные домишки Снижение рисков возникновения нарушений безопасности движения поездов при производстве маневровой и поездной работы
Снижение рисков возникновения нарушений безопасности движения поездов при производстве маневровой и поездной работы Adobe Photoshop. Коррекция изображений
Adobe Photoshop. Коррекция изображений Discovery & IOC Phase Network Architecture
Discovery & IOC Phase Network Architecture Технико-технологические требования по предупреждению газонефтеводопроявлений
Технико-технологические требования по предупреждению газонефтеводопроявлений Артериальная гипертония
Артериальная гипертония Презентация Все профессии важны
Презентация Все профессии важны Имидж педагога в новой образовательной среде
Имидж педагога в новой образовательной среде Кричалки и разминки для детей дошкольного возраста презентация для педагогов и родителей.
Кричалки и разминки для детей дошкольного возраста презентация для педагогов и родителей. Трудный ребенок
Трудный ребенок Технология успешного трудоустройства
Технология успешного трудоустройства Коляда
Коляда С 23 февраля, дорогие наши мальчики
С 23 февраля, дорогие наши мальчики Бедность и богатство
Бедность и богатство День Российской науки – 8 февраля
День Российской науки – 8 февраля Игры для автоматизации звука Ш
Игры для автоматизации звука Ш Опасности, травмы и заболевания, обусловленные неправильными действиями туристов
Опасности, травмы и заболевания, обусловленные неправильными действиями туристов Тайна имени
Тайна имени Оборудование для приготовления и продажи напитков
Оборудование для приготовления и продажи напитков Gravity Falls
Gravity Falls ВКР: Разработка системы автоматизации добычи и промыслового сбора нефти и газа на месторождении
ВКР: Разработка системы автоматизации добычи и промыслового сбора нефти и газа на месторождении Заикание с позиции логопсихокоррекционного подхода
Заикание с позиции логопсихокоррекционного подхода Программы реновации жилья – общая характеристика, возможность тиражирования опыта
Программы реновации жилья – общая характеристика, возможность тиражирования опыта Технология каменных работ
Технология каменных работ