Содержание
- 2. 1891 год Ирландский физик Стони вел понятие ЭЛЕКТРОН (по-гречески «янтарь») – частица, которая переносит электричество. Английский
- 3. 1897 год ДЖ. Томсон предложил модель атома – «Пудинг с изюмом» электрон +
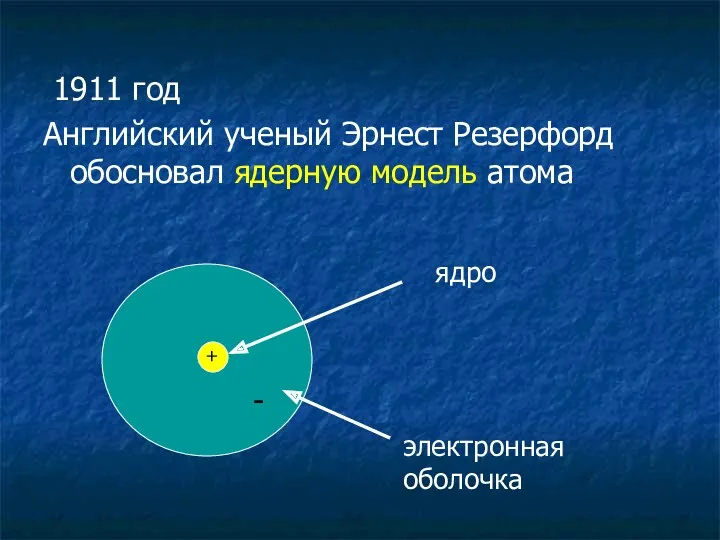
- 4. 1911 год Английский ученый Эрнест Резерфорд обосновал ядерную модель атома + ядро электронная оболочка -
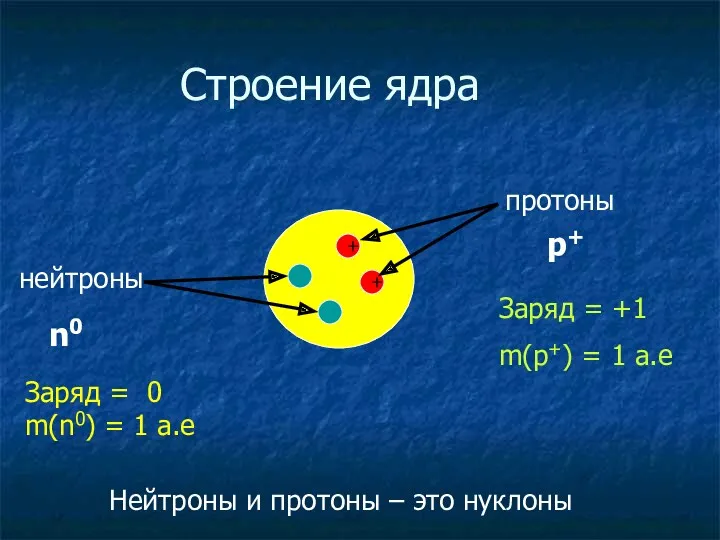
- 5. + + Строение ядра протоны нейтроны n0 p+ Заряд = +1 m(p+) = 1 a.e Заряд
- 6. Строение атома водорода + - Протон (p+) Электрон (ē) Атом электронейтрален
- 7. Число протонов = заряду атомного ядра = = числу электронов = = порядковому номеру элемента Mg
- 8. Масса атома – это масса его ядра. Число протонов + число нейтронов = массовое число (А)
- 9. Задание Укажите состав атома натрия Na 11 23 p+ = 11 ē = 11 n0 =
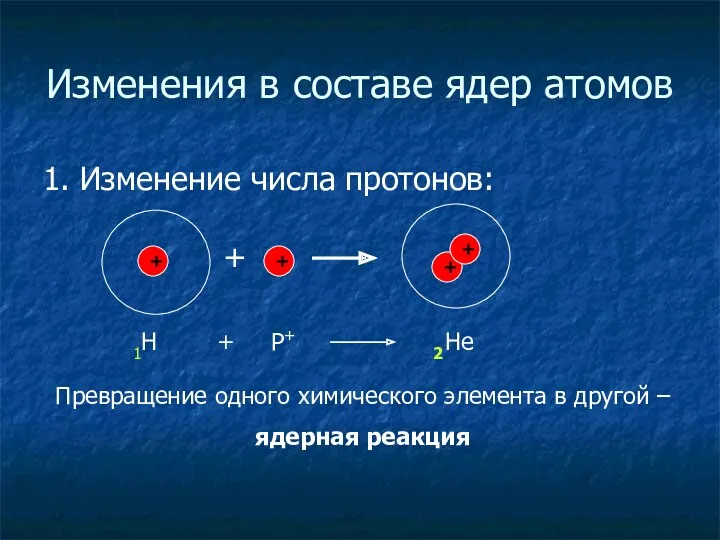
- 10. Изменения в составе ядер атомов 1. Изменение числа протонов: + + + + + 1Н Р+
- 11. Химический элемент – это вид атомов с одинаковым зарядом ядра (с одинаковым числом протонов в ядре)
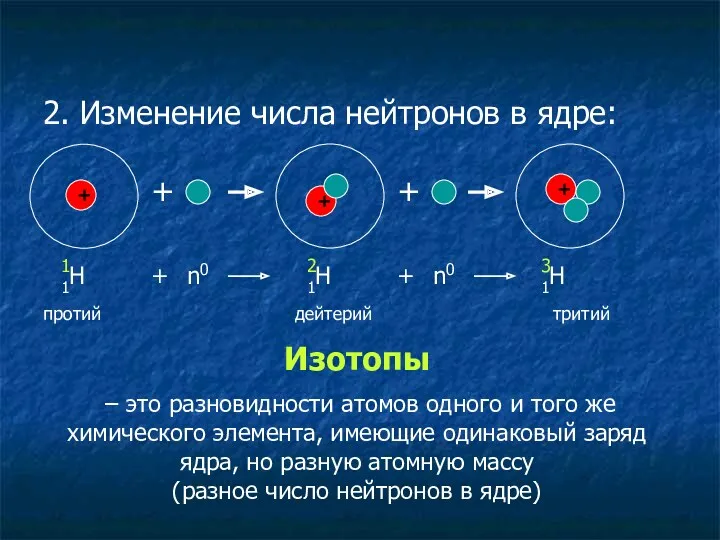
- 12. 2. Изменение числа нейтронов в ядре: + 1Н + + + + 1 + n0 1Н
- 13. 17 Сl 35 17 Сl 37 75% 25% Ar = 0.75 * 35 + 0.25 *
- 15. Скачать презентацию








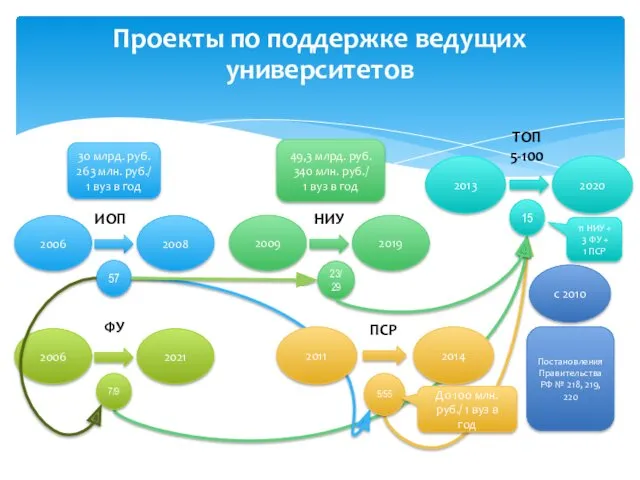 Проекты по поддержке ведущих университетов
Проекты по поддержке ведущих университетов Школьная форма
Школьная форма Услуги по защите окружающей среды
Услуги по защите окружающей среды Біблія
Біблія Презентация: Комплексное изучение ручья Рудки – особо охраняемой природной территории
Презентация: Комплексное изучение ручья Рудки – особо охраняемой природной территории Богу Сыну и Отцу
Богу Сыну и Отцу Ветроэнергетическая установка мощность 7000 кВт
Ветроэнергетическая установка мощность 7000 кВт ХУДОЖЕСТВЕННО- ЭСТЕТИЧЕСКОЕ РАЗВИТИЕ ДЕТЕЙ В УСЛОВИЯХ РЕАЛИЗАЦИИ ПРОГРАММЫ ДОШКОЛЬНОГО ОБРАЗОВАНИЯ
ХУДОЖЕСТВЕННО- ЭСТЕТИЧЕСКОЕ РАЗВИТИЕ ДЕТЕЙ В УСЛОВИЯХ РЕАЛИЗАЦИИ ПРОГРАММЫ ДОШКОЛЬНОГО ОБРАЗОВАНИЯ Подтип Позвоночные (vertebrata), или Черепные (craniata)
Подтип Позвоночные (vertebrata), или Черепные (craniata) МАСТЕР КЛАСС ПО БИСЕРОПЛЕТЕНИЮ
МАСТЕР КЛАСС ПО БИСЕРОПЛЕТЕНИЮ Бу күшті қондырғының негізгі циклы (Ренкин циклы)
Бу күшті қондырғының негізгі циклы (Ренкин циклы) ВКР: Действия локомотивной бригады при отправлении поезда
ВКР: Действия локомотивной бригады при отправлении поезда Первобытные люди. Воспитатель: Корелякова О.Е
Первобытные люди. Воспитатель: Корелякова О.Е Квадратные уравнения с параметрами
Квадратные уравнения с параметрами Пчеловодство
Пчеловодство Мастер - класс Снеговик
Мастер - класс Снеговик Разработка встраиваемой системы управления электропривода уточного накопителя ткацкого станка
Разработка встраиваемой системы управления электропривода уточного накопителя ткацкого станка Все о республике и федеративном государстве. 11 класс
Все о республике и федеративном государстве. 11 класс Деятельность первых типографий
Деятельность первых типографий Внеклассное мероприятие для учащихся 5 класса Осенние посиделки Диск
Внеклассное мероприятие для учащихся 5 класса Осенние посиделки Диск Игры народов Урала
Игры народов Урала The body
The body Буквы ь и ъ
Буквы ь и ъ Дидактическая игра Один - много
Дидактическая игра Один - много Современная Front-End разработка. (Лекция 8)
Современная Front-End разработка. (Лекция 8) Астероиды
Астероиды Государственное регулирование в сфере культуры
Государственное регулирование в сфере культуры Презентация элективного курса по математике
Презентация элективного курса по математике