Слайд 2

Вещества бывают: простые (С, Р), сложные (Н₂О, СО₂).
Для металлов характерна –
металлическая связь, для неметаллов – ковалентная неполярная, ков.полярная,для металлов и неметаллов – ионная.
Слайд 3

Например:NaCl - ионная связь. Na отдает 1 е образует + заряд,
Сl принимает 1 е заряжается в – заряд.
Na⁰ + Cl⁰ = Na⁺Cl⁻
Слайд 4

Например: HCl – ковал. Полярная связь. Образуется общая электронная пара, Н
смещается к Cl т.к. у хлора электроотрицательность больше.
Н•+ Cl = Hδ⁺ + Clδ⁻
Слайд 5

Если представить, что Н полностью перейдет к хлору они получили бы
условные заряды +1 и -1. Такие условные заряды в соединениях с ков. Полярной связью называют степенью окисления.
Слайд 6

Степень окисления – это условный заряд атомов химического элемента в соединениях
вычисленный на основе предположения, что все соединения( и ионные,ков. Поляр.) состоят только из ионов.
Слайд 7

Благодаря ионной и ков. Полярной связей образуется сложные соединения из 2х
элементов бинарные соединения.
Например: NaCl, K₂S, Н₂О
Слайд 8

Степень окисления:
«-» атомы х.элементов, которые принимают е в ионных соединениях, более
электроотрицатнльнее в ков.полярной связи.(только 1элемент)
Слайд 9

«+» -все металлы (от +1до+3)
«0» - для соединений с ков. Неполярной
связью (О,Н)
Слайд 10

1. С.о. у металлов +1до +3, кроме Cu, Au. (№ группы).
Исключения:Au
+3(1гр.),Cu +2(1гр.),+8 только у осмия Os, рутения Ru.
2.С.о у неметаллов +и - в зависимости от соединения:
Слайд 11

У метал. и немет. - немет. с – значением.
У Немет и
немет. + и – значения.
(высшая отрицательная степень окисления 8-№группы, напр.:хлор 8-№7 гр.=1, значит с.о.у хлора -1)
Слайд 12

(высшая отриц.степень= числу е на внешнем уровнет.е №группы. Например: С углерод
4 Гр.+4)
3. С.о. простых веществ = 0(О₂⁰)
Слайд 13
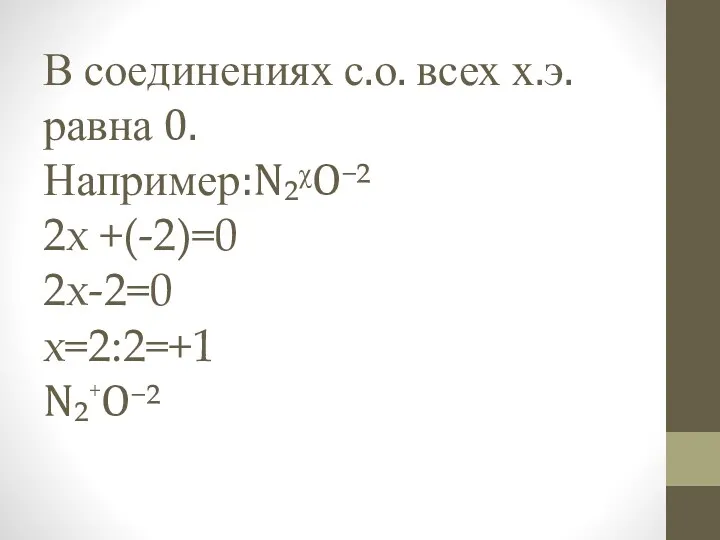
В соединениях с.о. всех х.э. равна 0.
Например:N₂ᵡO⁻²
2х +(-2)=0
2х-2=0
х=2:2=+1
N₂⁺O⁻²
Слайд 14

Правила определений с.о.:
1.х.э. в прост. вещ-ва имеет 0 с.о.(Fe⁰)
2.Все металлы +
с.о.
3.В(бор),Si(кремний) имеют + с.о.
4.Н имеет +1 с.о.
Исключение:
Слайд 15

Гидриды: соединение Н с металлами гл. подгруппы 1 и2 гр.(литий,натрий,калий) С.о.
-1
Например:Са⁺Н⁻
5.О кислород имеет -2 с.о.
Исключение:1.О⁺²F⁻² в соед.с фтором.
2.Перекисях Н₂⁺О₂ ⁻ -1
Слайд 16

6.F фтор имеет -1 с.о.
Таблица постоянные с.о.:
+1:Li,Na,K,Rb,Cs,H(кроме гидридов Na⁺H⁻)
+2:Be,Mg,Ca,Sr,Zn,Cd,Ba.
+3 Al,B.
-1F ,(Cl
,Br, J – если с Н и Мета)
-2 O,(S,Se,Te-если с Н и Ме)
-3 N,P,As- в соед. с Н и Ме.











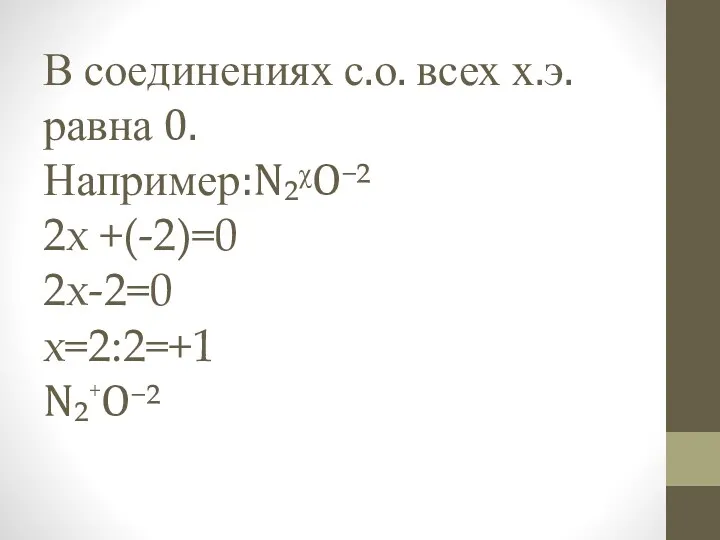



 проверка знаний по теме: Спирты.
проверка знаний по теме: Спирты. 2012-2013 учебный год
2012-2013 учебный год Табышмаклар иленә сәяхәт
Табышмаклар иленә сәяхәт Квантовая физика
Квантовая физика Орошение - V
Орошение - V Компетенция арбитражных судов РФ
Компетенция арбитражных судов РФ Красная книга России. Правила поведения в природе
Красная книга России. Правила поведения в природе Неходжкинская лимфома. Классификация и диагностика
Неходжкинская лимфома. Классификация и диагностика Архит памятники
Архит памятники Подготовка к ГИА-9 (тест)
Подготовка к ГИА-9 (тест) Методические материалы по подготовке к написанию работы по литературе на допуск к ЕГЭ
Методические материалы по подготовке к написанию работы по литературе на допуск к ЕГЭ Воспалительные заболевания височно-нижнечелюстного сустава
Воспалительные заболевания височно-нижнечелюстного сустава Уникальный комплекс позднепалеолитических стоянок Костенки
Уникальный комплекс позднепалеолитических стоянок Костенки Жүректің туа пайда болған ақауының алдын алуда поливитаминдердің тиімділігін бағалау
Жүректің туа пайда болған ақауының алдын алуда поливитаминдердің тиімділігін бағалау Постимпрессионизм. Характерные особенности
Постимпрессионизм. Характерные особенности Поведенческая экономика отраслевых рынков
Поведенческая экономика отраслевых рынков Презентация о Тамбове
Презентация о Тамбове Блокированные дома
Блокированные дома Системное программирование. Язык C. Адреса и указатели. Динамическая память
Системное программирование. Язык C. Адреса и указатели. Динамическая память Презентация Профилактика нарушений голоса
Презентация Профилактика нарушений голоса Благоустройство общественной территории. Бульвар у памятника погибшим воинам Энергия Побед
Благоустройство общественной территории. Бульвар у памятника погибшим воинам Энергия Побед Ядовитые грибы
Ядовитые грибы Всемирный день защиты китов
Всемирный день защиты китов Задачи по авторскому и смежным правам
Задачи по авторскому и смежным правам Исследование границ и структуры отраслевых рынков с помощью индексов
Исследование границ и структуры отраслевых рынков с помощью индексов Готовность к школьному обучению
Готовность к школьному обучению Технология кладки из природных и искусственных камней правильной формы
Технология кладки из природных и искусственных камней правильной формы Объективы и их основные элементы. Фотосъемка
Объективы и их основные элементы. Фотосъемка