Содержание
- 2. Верите ли Вы что…? ФИО ___________________класс_____________
- 3. НЕПРЕДЕЛЬНЫЕ УГЛЕВОДОРОДЫ. ЭТИЛЕН И ЕГО ГОМОЛОГИ.
- 4. Организация урока: 1.Рабочие листы для заполнения-1и2 2.Листы с информацией для каждого ряда: Определение класса алкенов, номенклатура
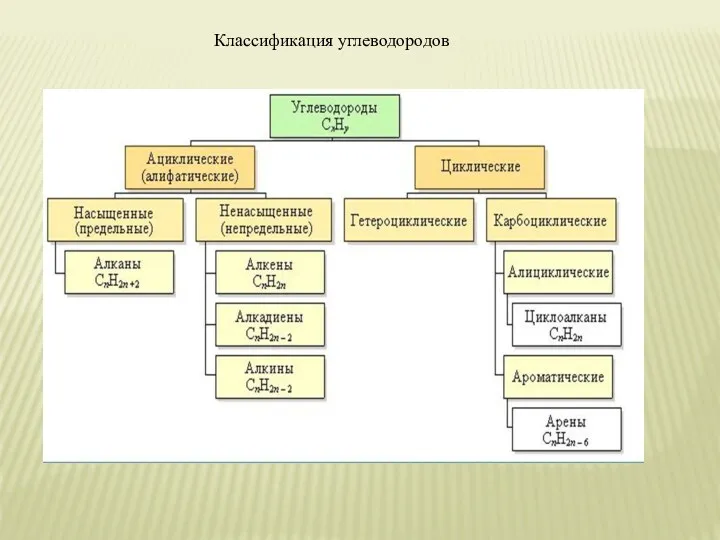
- 5. Классификация углеводородов
- 6. Непредельные, или ненасыщенные, углеводороды ряда этилена (алкены, или олефины)- углеводороды, в молекулах которых между углеродными атомами
- 7. По систематической номенклатуре названия этиленовых углеводородов производят заменой суффикса -ан в соответствующих алканах на суффикс -ен
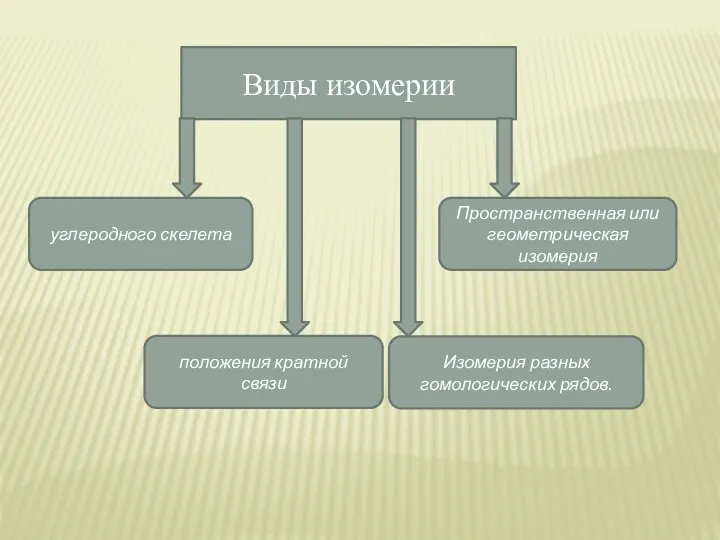
- 8. Виды изомерии углеродного скелета положения кратной связи Изомерия разных гомологических рядов. Пространственная или геометрическая изомерия
- 9. Физические свойства Алкены – этен, пропен и бутен – при обычных условиях (20 °С, 1 атм)
- 10. Получение алкенов: Дегидратация спиртов 2) Дегидрирование алканов 3) Пиролиз и крекинг нефти и природного газа 4)
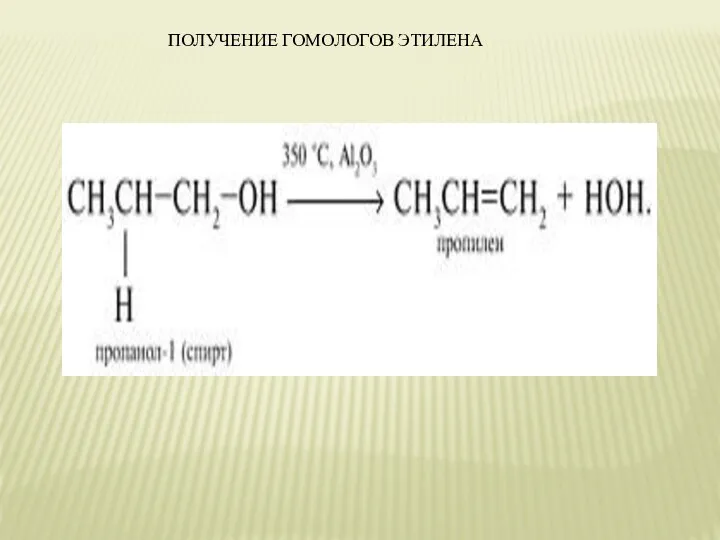
- 12. ПОЛУЧЕНИЕ ГОМОЛОГОВ ЭТИЛЕНА
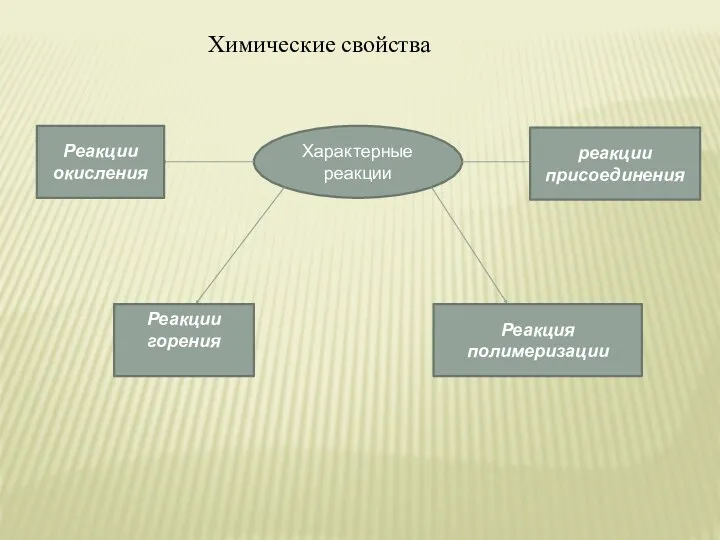
- 13. Химические свойства Характерные реакции Реакции окисления Реакции горения Реакция полимеризации реакции присоединения
- 14. Реакции горения. H2C=CH2 + 3O2 → 2CO2 + 2H2O 2H2C=CH─СН3+ 9O2 → 6CO2 + 6H2O
- 15. Реакции окисления
- 16. Реакции присоединения Гидрирование ( присоединение водорода) 2. Галогенирование ( присоединение галогенов) 3. Гидрогалогенирование ( присоединение галогеноводородов)
- 17. Галогенирование (присоединение галогенов) Гидрирование ( присоединение водорода) H2C=CH2 + Br2→ BrCH2–CH2Br (1,2-дибром-этан) CH3–CH=CH2 + H2 →Ni→
- 18. Гидрогалогенирование H2C=CH2 + HBr → CH3–CH2Br (бромистый этил) Присоединение полярных молекул( галогеноводородов, воды ) к пропену
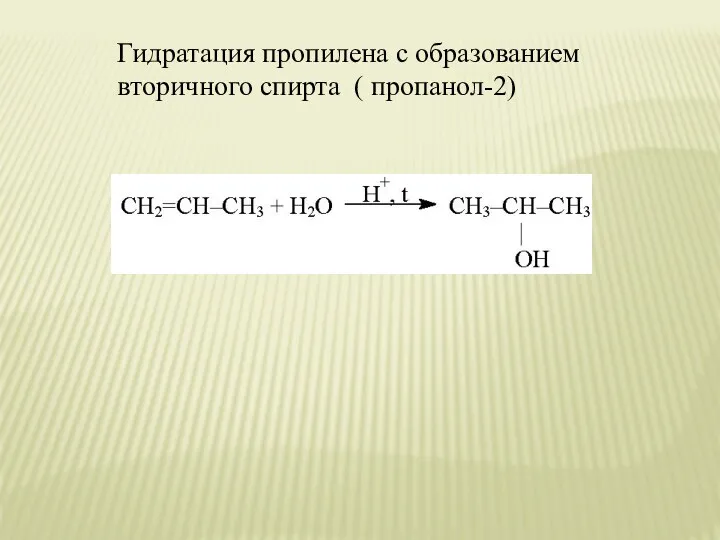
- 19. Гидратация пропилена с образованием вторичного спирта ( пропанол-2)
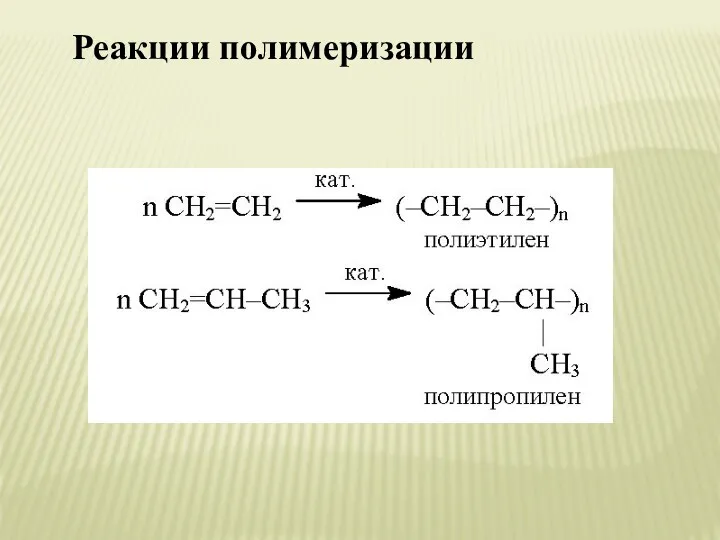
- 20. Реакции полимеризации
- 23. Скачать презентацию














 Национальная идея и реальная политика в области качества в России
Национальная идея и реальная политика в области качества в России Итоговое родительское собрание в 4 классе.
Итоговое родительское собрание в 4 классе. Презентация Бурятский национальный костюм
Презентация Бурятский национальный костюм Политика как предмет политологии
Политика как предмет политологии Родительское собрание на тему:Здоровье детей в наших руках
Родительское собрание на тему:Здоровье детей в наших руках Суворовские источники
Суворовские источники Курсы подготовки вэб-разработчиков
Курсы подготовки вэб-разработчиков Теоретико-практическая система Галена и ее влияние на развитие медицины во II в. – XVI в
Теоретико-практическая система Галена и ее влияние на развитие медицины во II в. – XVI в Модель компетенций персонала ООО Евросеть
Модель компетенций персонала ООО Евросеть Слова с удвоенными согласными
Слова с удвоенными согласными урок 3 класс. месяцы
урок 3 класс. месяцы Ноосферное образование: теория и практика
Ноосферное образование: теория и практика Непосредственное, прямое народовластие. (Тема 7)
Непосредственное, прямое народовластие. (Тема 7) Тренинг: Азбука предпринимателя. День 3
Тренинг: Азбука предпринимателя. День 3 Технология изготовления окантовочного шва
Технология изготовления окантовочного шва Презентация Витамины наши друзья
Презентация Витамины наши друзья Свидетель эпохи. Жак-Луи Давид
Свидетель эпохи. Жак-Луи Давид Команда присаивания
Команда присаивания Жизнь и творчество Дмитрия Ивановича Менделеева.
Жизнь и творчество Дмитрия Ивановича Менделеева. Кирилл и Мефодий. Гимн и Величание
Кирилл и Мефодий. Гимн и Величание презентация Масленица
презентация Масленица Конспект занятия по теме: Изготовление открытки Розы для мамы
Конспект занятия по теме: Изготовление открытки Розы для мамы Презентация Наша Родина
Презентация Наша Родина Быт и обычаи России в 19 веке. 2 часть
Быт и обычаи России в 19 веке. 2 часть Современный урок. Методические требования к современному уроку
Современный урок. Методические требования к современному уроку Патриотическое воспитание как одна из задач воспитания подрастающего поколения
Патриотическое воспитание как одна из задач воспитания подрастающего поколения Птицы Волгоградской области. Семейство утиных
Птицы Волгоградской области. Семейство утиных Мышкинский муниципальный район. Волонтерский отряд Вместе - мы сила!
Мышкинский муниципальный район. Волонтерский отряд Вместе - мы сила!