Содержание
- 2. Химия - наука о веществах … Что изучает химия?
- 3. Как и в каких единицах можно измерить вещество?
- 4. Для измерения вещества выбрана особая единица, которая соединяет в себе число молекул и массу Это единица
- 5. В порции вещества количеством 1 МОЛЬ содержится 6· 1023 молекул (атомов) данного вещества. При этом масса
- 6. Примеры: 1) Аr (Н)=1, => 1 г элементарного водорода содержит 6 ·1023 атомов водорода 3) Mr
- 7. Определение Количество вещества - это физическая величина, которая определяется числом структурных единиц этого вещества (молекул, атомов,
- 8. Определение Моль - это единица измерения количества вещества, то есть такая порция вещества, которая содержит 6
- 9. Постоянная Авогадро - это физическая величина, которая показывает содержание структурных частиц (молекул, атомов ) в 1
- 10. Формула для определения числа частиц вещества N-число структурных частиц (молекул, атомов и др.) N=NA · n
- 11. Определите число молекул, содержащихся в 2 моль водорода. N (H2)= 6 ·1023 · 2 = =12
- 12. 3 моль водорода - 5 моль кислорода - 1 моль оксида углерода - 2 моль азота
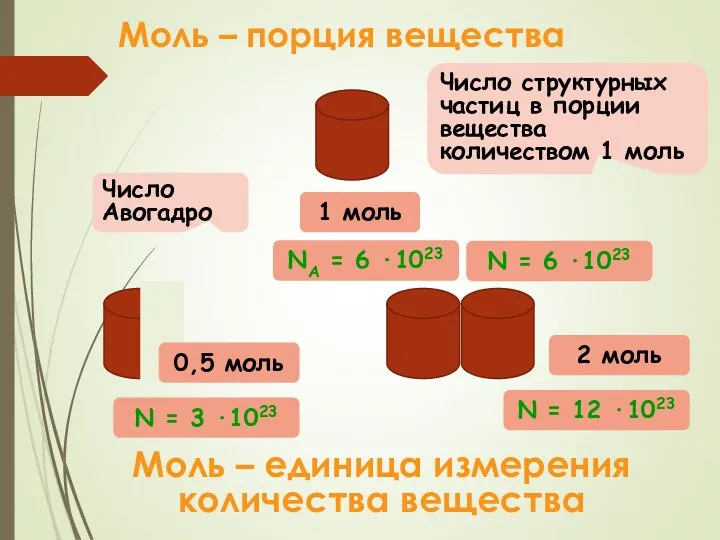
- 13. Моль – порция вещества Моль – единица измерения количества вещества Число структурных частиц в порции вещества
- 14. Молярная масса Это физическая величина, которая показывает массу 1 моль вещества. Обозначается М Численно равна относительной
- 15. Количество вещества n = m/M m = n· M
- 16. Заполняем таблицы 6 и 7, стр. 49 Решаем задачи № 8, стр. 49 № 10, стр.
- 17. Домашнее задание § 15 В тетради на печатной основе Задание 9,11,12, стр. 50
- 19. Скачать презентацию















 Акция Истории спасенных животных
Акция Истории спасенных животных Экспертные модели бизнес-процессов. Экспертные сравнения
Экспертные модели бизнес-процессов. Экспертные сравнения Презентация Герои минувшей войны.
Презентация Герои минувшей войны. Школьные службы примирения как форма профилактики преступлений и правонарушений
Школьные службы примирения как форма профилактики преступлений и правонарушений Фото. Айсберг
Фото. Айсберг Система функционирования и особенности суда в РФ
Система функционирования и особенности суда в РФ Отечественная война 1812 года
Отечественная война 1812 года Презентация по географии на тему : Мой знак зодиака
Презентация по географии на тему : Мой знак зодиака Россия в первой половине ХIХ века
Россия в первой половине ХIХ века Библиотека Высшего медицинского колледжа
Библиотека Высшего медицинского колледжа Ванюков пешінің бай штейндеріндегі сульфидті мыс концентраттарын балқытуды зерттеу
Ванюков пешінің бай штейндеріндегі сульфидті мыс концентраттарын балқытуды зерттеу Сталь. Классификация сталей
Сталь. Классификация сталей Христианство: католицизм, православие и протестантизм
Христианство: католицизм, православие и протестантизм Обработка символьной информации в TurboPascal (задачи, часть 1)
Обработка символьной информации в TurboPascal (задачи, часть 1) Легенды старого Кенигсберга
Легенды старого Кенигсберга Вторичные дистонии
Вторичные дистонии Организаторы военной экономики
Организаторы военной экономики Электробезопасность. Пожаровзрывобезопасность. Механические опасности
Электробезопасность. Пожаровзрывобезопасность. Механические опасности Способы получения металлов
Способы получения металлов Діни ағымдардың қоғамға кері әсері
Діни ағымдардың қоғамға кері әсері Проектная работа Семейные традиции
Проектная работа Семейные традиции Горожане и их образ жизни
Горожане и их образ жизни Иван Сергеевич Тургенев Записки охотника
Иван Сергеевич Тургенев Записки охотника Открытка ко дню матери
Открытка ко дню матери Вимоги до науково-педагогічного працівника
Вимоги до науково-педагогічного працівника Базовая аппаратная конфигурация персонального компьютера
Базовая аппаратная конфигурация персонального компьютера Жизнь и быт городских жителей России 19-го века
Жизнь и быт городских жителей России 19-го века Tovar-moddiy zaxiralar hisobi
Tovar-moddiy zaxiralar hisobi