Содержание
- 2. Дайте характеристику Rb и Сs по его положению в Периодической системе по плану: а)положение в Периодической
- 3. Щелочные металлы. Химические свойства. Важнейшие соединения щелочных металлов.
- 4. Щелочные металлы - хорошие восстановители Взаимодействуют с окислителями: Неметаллами Водой Кислотами
- 5. С кислородом Li + O2 → Li2O оксид лития Na + O2 → Na2O2 пероксид натрия
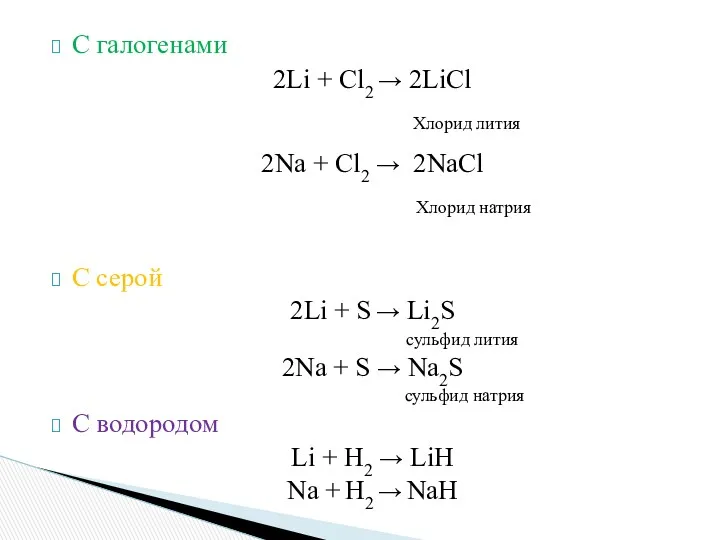
- 6. С галогенами 2Li + Cl2 → 2LiCl Хлорид лития 2Na + Cl2 → 2NaCl Хлорид натрия
- 7. С водой 2Li + 2H2O → 2LiOH +H2 Гидроксид лития 2Na +2H2O → 2NaOH +H2 Гидроксид
- 8. Оксиды Me2O - твердые вещества. Имеют ярко выраженные основные свойства: взаимодействуют с кислотными оксидами, водой, кислотами.
- 9. KOH – гидроксид калия NaOH – гидроксид натрия LiOH – гидроксид лития Гидроксиды щелочных металлов Какова
- 10. Соли щелочных металлов – твердые кристаллические вещества ионного строения. NaCl – каменная соль Na2CO3 – карбонат
- 12. Электролиз расплава МеСl эл.ток Ме+ + Сl- на катоде: Ме+ + 1е Ме0 на аноде: Сl-
- 13. О каком элементе идет речь? Хранят обычно в керосине, и бегает он по воде, В природе,
- 14. Запишите уравнения реакций взаимодействия калия с кислородом, с бромом, с фосфором, с водой. Напишите электронный баланс
- 15. 1.Что нового вы сегодня узнали на уроке, чему научились? 2.Что еще хотели бы узнать, изучить? 3.Что
- 17. Скачать презентацию













 Оборотные активы организации
Оборотные активы организации Тематическая неделя День матери
Тематическая неделя День матери Общий обзор организма человека
Общий обзор организма человека Робототехника. Основные определения
Робототехника. Основные определения Мероприятия туристско-краеведческой направленности. Центр ДЮТТИТ Пушкинского района Санкт-Петербурга
Мероприятия туристско-краеведческой направленности. Центр ДЮТТИТ Пушкинского района Санкт-Петербурга Римская поэзия
Римская поэзия Простейшие задачи в координатах
Простейшие задачи в координатах Кирово – Чепецкая центральная районная больница
Кирово – Чепецкая центральная районная больница Жұқпалы аурулардың иммунопрофилактикасы
Жұқпалы аурулардың иммунопрофилактикасы Механіко-технологічні властивості добрив як об'єкта механізованого внесення в ґрунт
Механіко-технологічні властивості добрив як об'єкта механізованого внесення в ґрунт Культурьное наследие прототюрков
Культурьное наследие прототюрков Презентация Детское экспериментирование
Презентация Детское экспериментирование Механика материалов. Прочность при циклических напряжениях. (Лекция 29)
Механика материалов. Прочность при циклических напряжениях. (Лекция 29) Шаблоны Templatemonster. Сайт. Основы локальных сетей. (Занятие 4.1)
Шаблоны Templatemonster. Сайт. Основы локальных сетей. (Занятие 4.1) Мастер-класс для педагоговАппликация в технике Торцевание
Мастер-класс для педагоговАппликация в технике Торцевание Повседневная жизнь горожан на Руси X-XIII века
Повседневная жизнь горожан на Руси X-XIII века Литературная викторина Волшебная книга сказок
Литературная викторина Волшебная книга сказок Oe vocabulary. Lecture 5
Oe vocabulary. Lecture 5 Школьная неуспеваемость и её причины
Школьная неуспеваемость и её причины Бестраншейные бурения
Бестраншейные бурения Презентация ИКТ на уроках математики
Презентация ИКТ на уроках математики Кислоты. Свойства кислот
Кислоты. Свойства кислот Информирование молодежи Санкт-Петербурга о возможностях профессиональной самореализации
Информирование молодежи Санкт-Петербурга о возможностях профессиональной самореализации Дифференциация звуков [Ч -Ть]
Дифференциация звуков [Ч -Ть] PRIMALADY`S. Персональная программа, включающая все элементы идеальной формулы Вашей красоты
PRIMALADY`S. Персональная программа, включающая все элементы идеальной формулы Вашей красоты Методы исследования аутического расстройства
Методы исследования аутического расстройства Выставка детского и семейного творчества Осенние фантазии
Выставка детского и семейного творчества Осенние фантазии Задачи на совместную работу (урок изучения нового материала)
Задачи на совместную работу (урок изучения нового материала)