Слайд 2

ЦЕЛИ УРОКА:
ОЗНАКОМИТЬСЯ С О СТРОЕНИЕМ МОЛЕКУЛЫ ВОДЫ
РАССМОТРЕТЬ ФИЗИЧЕСКИЕ СВОЙСТВА ВОДЫ
РАССМОТРЕТЬ ХИМИЧЕСКИЕ СВОЙСТВА ВОДЫ
Слайд 3
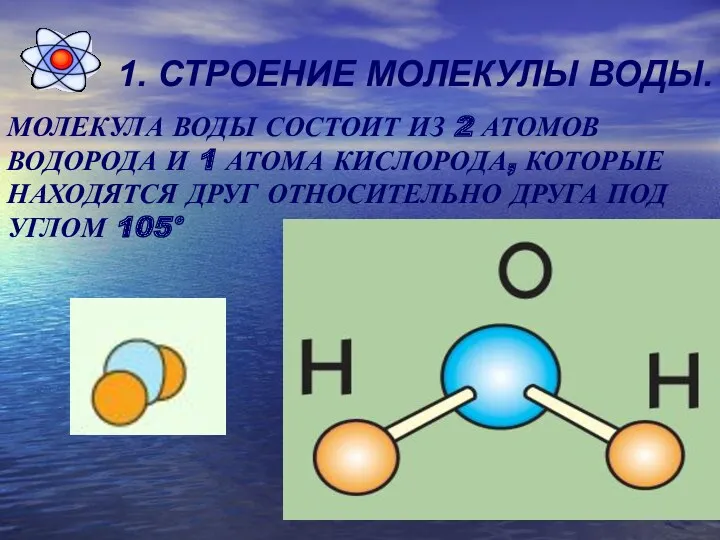
1. СТРОЕНИЕ МОЛЕКУЛЫ ВОДЫ.
МОЛЕКУЛА ВОДЫ СОСТОИТ ИЗ 2 АТОМОВ ВОДОРОДА И
1 АТОМА КИСЛОРОДА, КОТОРЫЕ НАХОДЯТСЯ ДРУГ ОТНОСИТЕЛЬНО ДРУГА ПОД УГЛОМ 105°
Слайд 4

2. ФИЗИЧЕСКИЕ СВОЙСТВА ВОДЫ.
ЧИСТАЯ (ДИСТИЛЛИРОВАННАЯ) ВОДА – БЕСЦВЕТНАЯ ЖИДКОСТЬ, БЕЗ
ЗАПАХА И ВКУСА
ЕДИНСТВЕННОЕ ВЕЩЕСТВО, КОТОРОЕ НА ЗЕМЛЕ СУЩЕСТВУЕТ В ТРЕХ АГРЕГАТНЫХ СОСТОЯНИЯХ
ТЕМПЕРАТУРА КИПЕНИЯ 100°С
ТЕМПЕРАТУРА КРИСТАЛЛИЗАЦИИ (ПЛАВЛЕНИЯ) 0°С
Слайд 5

В XVIII ВЕКЕ ВОДА ПОСЛУЖИЛА ЭТАЛОНОМ ДЛЯ ВЫБОРА ЕДИНИЦЫ МАССЫ:
МАССЕ 1 куб. см. БЫЛО ПРИПИСАНО ЗНАЧЕНИЕ 1г
МАКСИМАЛЬНАЯ ПЛОТНОСТЬ ПРИ 4°С ПРИНЯТА ЗА 1г/мл, ВСЕ ОСТАЛЬНЫЕ ВЕЩЕСТВА СРАВНИВАЮТСЯ ПО ПЛОТНОСТИ И МАССЕ С ВОДОЙ
ПЛОТНОСТЬ ЛЬДА МЕНЬШЕ, ЧЕМ У ЖИДКОЙ ВОДЫ, ЧТО ЯВЛЯЕТСЯ АНОМАЛЬНЫМ СВОЙСТВОМ ВОДЫ
ВОДА ОБЛАДАЕТ САМОЙ БОЛЬШОЙ ТЕПЛОЕМКОСТЬЮ
ОНА НЕ ПРОВОДИТ
ЭЛЕКТРИЧЕСКИЙ ТОК
Слайд 6

3. ХИМИЧЕСКИЕ СВОЙСТВА ВОДЫ.
1. С МЕТАЛЛАМИ.
а) очень активные металлы при взаимодействии
с водой образуют гидроксид и водород
2Na + 2H2O = 2NaOH + H2
гидроксид натрия
2K + 2H2O = 2KOH + H2
гидроксид калия
Ca + 2H2O = Ca(OH)2 + H2
гидроксид кальция
Слайд 7

б) средние по активности металлы при взаимодействии с водой при нагревании
образуют оксид металла и водород
t
Zn + H2O = ZnO + H2
t оксид цинка
3Fe + 4H2O = Fe3O4 + 4H2
в) малоактивные металлы Cu, Hg, Ag, Pt, Au
с водой не реагируют
Слайд 8

2. С ОКСИДАМИ.
а) оксиды металлов при взаимодействии с водой образуют гидроксиды
CaO + H2O = Ca(OH)2
гидроксид кальция
б) оксиды неметаллов при взаимодействии с водой образуют кислоты
SO3 + H2O = H2SO4
серная кислота
Слайд 9

P2O5 + 3H2O = 2H3PO4
фосфорная кислота
Слайд 10
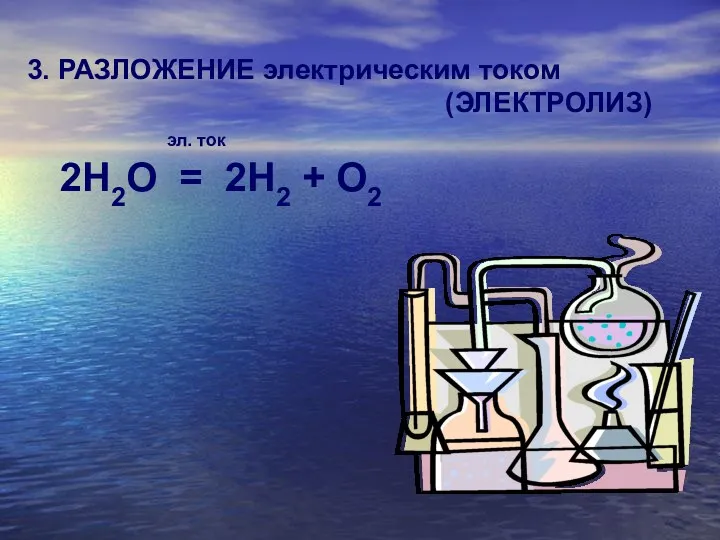
3. РАЗЛОЖЕНИЕ электрическим током
(ЭЛЕКТРОЛИЗ)
эл. ток
2H2O = 2H2
+ O2
Слайд 11

Допишите уравнения реакций
SO2 + H2O= Ca + H2O=
CrO3 + H2O=
Cu + H2O=
BaO + H2O= Li + H2O=
K2O + H2O= Ba + H2O=
Задача.
Вычислите массовую долю сахара в сиропе, если для его приготовления потребовалось 300г сахара и 1000г воды










 Формирование графических навыков у детей раннего возраста
Формирование графических навыков у детей раннего возраста Азотсодержащие соединения: аминокислоты
Азотсодержащие соединения: аминокислоты Иуда Искариот Л. Андреева и Евангельский сюжет
Иуда Искариот Л. Андреева и Евангельский сюжет Пророчий ярус у давніх українських іконостасах: Іконографія та поезія
Пророчий ярус у давніх українських іконостасах: Іконографія та поезія Виды резьбы по дереву
Виды резьбы по дереву Врожденный гипотиреоз
Врожденный гипотиреоз Научные революции и смена типов научной рациональности
Научные революции и смена типов научной рациональности Факторный анализ причин отказов скважин
Факторный анализ причин отказов скважин 12 апреля
12 апреля Тема урока: Вышивка крестом. Изготовление мешочка из конвы.
Тема урока: Вышивка крестом. Изготовление мешочка из конвы. Системы документации. Тема 4
Системы документации. Тема 4 Проект Почта
Проект Почта Отряды рыб
Отряды рыб Устройство для регистрации биоэлектрических сигналов с USB интерфейсом
Устройство для регистрации биоэлектрических сигналов с USB интерфейсом Сварочное производство. Тема 3
Сварочное производство. Тема 3 скорогоговорка на звуки д-б
скорогоговорка на звуки д-б Идентификаторы переменных
Идентификаторы переменных Китайская опера
Китайская опера Языки программирования
Языки программирования Дифференциация звуков [р] - [л]
Дифференциация звуков [р] - [л] Ответственность в хозяйственном праве
Ответственность в хозяйственном праве Скоро в школу
Скоро в школу Роль супервайзера в достижении лидерства ТМ Nemiroff в рознице в г. Одесса
Роль супервайзера в достижении лидерства ТМ Nemiroff в рознице в г. Одесса Портфолио ученика начальной школы.
Портфолио ученика начальной школы. Презентация Правила поведения при землетрясении
Презентация Правила поведения при землетрясении Система охлаждения газа после компримирования
Система охлаждения газа после компримирования История летательных аппаратов
История летательных аппаратов Українська гетьманська держава в системі міжнародних відносин. (Урок 6)
Українська гетьманська держава в системі міжнародних відносин. (Урок 6)