Слайд 2
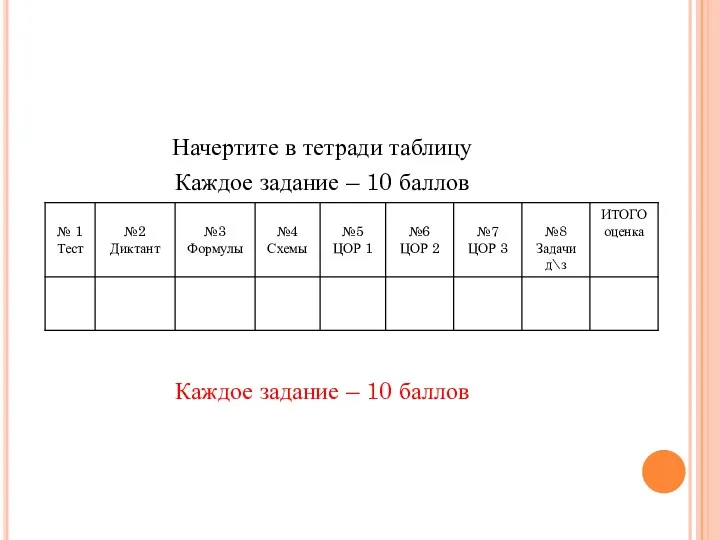
Начертите в тетради таблицу
Каждое задание – 10 баллов
Каждое задание – 10
баллов
Слайд 3

№1. ТЕСТ РЕШИТЕ ТЕСТ
1.
2.
3.
4.
5.
Слайд 4

№1 ТЕСТ
1.К физическим явлениям относится:
А) Горение парафина
Б) Прокаливание медной проволоки
В) Испарение
бензина
Г) Скисание молока
2.К химическим явлениям относится:
А) Таяние снега
Б) Измельчение сахара
В) Обугливание древесины
Г) Замерзание воды
Слайд 5

3. К реакциям замещения относится
А) Zn+ 2НС1 ?ZnCl2+ Н2
Б) 4Na+ 02?2Na20
В)
2КClOз?2КС1+ 3о2
Г) so3 + н2о?H2so4
4. К реакциям соединения относится
А) Zn+ 2НС1 ?ZnCl2+ Н2
Б) 4Na+ 02?2Na20
В) 2КClOз?2КС1+ 3о2
Г) so3 + н2о?H2so4
Слайд 6

5. Запись является не уравнением, а схемой
А) Zn+ 2НС1 ?ZnCl2+ Н2
Б)
Na+ 02?Na20
В) 2КClOз?2КС1+ 3о2
Г) so3 + н2о?H2so4
Слайд 7

ПРОВЕРКА
№1. ТЕСТ
1. В
2. В
3. А
4. Б,Г
5. Б
Запишите балл в таблицу
Слайд 8

№2 ДИКТАНТ
1.
2.
3.
4.
5.
6.
7.
8.
9.
10.
Слайд 9

ПРОВЕРКА
№2 ДИКТАНТ
1. Химическая реакция
2. Индикатор
3. Фенолфталеин
4.Реакция соединения
5. Реакция разложения
6. Реакция
замещения
7. Реакция обмена
8. Индекс
9. Коэффициент
10. Экзотермическая реакция
Запишите балл в таблицу
Слайд 10

№3 ФОРМУЛЫ
ЗАПИШИТЕ ФОРМУЛЫ СЛЕДУЮЩИХ ВЕЩЕСТВ
1. Оксид железа (III)
2. Сернистая кислота
3.
Гидроксид алюминия
4. Карбонат калия
5. Нитрид кальция
6. Угольная кислота
7. Нитрат магния
8. Гидроксид серебра
9. Хлор
10. Сульфит хрома (III)
Слайд 11

ПРОВЕРКА
№3 ФОРМУЛЫ
1. Оксид железа (III) – Fe2O3
2. Сернистая кислота –
H2SO3
3. Гидроксид алюминия - Al(OH)3
4. Карбонат калия - K2CO3
5. Нитрид кальция – Ca3N2
6. Угольная кислота – H2CO3
7. Нитрат магния – Mg(NO3)2
8. Гидроксид серебра - AgOH
9. Хлор – Cl2
10. Сульфит хрома (III) – Cr2(SO3)3
Слайд 12

№4. СХЕМЫ
РАССТАВЬТЕ КОЭФФИЦИЕНТЫ, СОСЧИТАЙТЕ СУММУ КОЭФФИЦИЕНТОВ
1) Fe2O3 + C →
Fe + CO↑
2) O2 + Fe → Fe3O4
3) NaClO3 → O2↑ + NaCl
4) SnO2 + HCl → SnCl4 + H2O
5) Ca(OH)2+H3PO4 →Ca3(PO4)2+H2O
Слайд 13

ПРОВЕРКА
№4. СХЕМЫ
1) Fe2O3 + 3C → 2Fe + 3CO↑ 9
2) 2O2
+ 3Fe → Fe3O4 6
3) 2NaClO3 → 3O2↑ + 2NaCl 7
4) SnO2 + 4HCl → SnCl4 + 2H2O 8
5) 3Ca(OH)2+2H3PO4 →Ca3(PO4)2+6H2O 12
Слайд 14

ЦИФРОВЫЕ РЕСУРСЫ
Просмотрите опыт, запишите уравнение реакции, расставьте коэффициенты, укажите тип реакции
ЦОР
1
ЦОР 2
ЦОР 3
Слайд 15

ПРОВЕРКА ЦОР
ЦОР 1 2 Al+3Br2→2AlBr3 реакция соединения
ЦОР 2 P2O5 +3H2O→ 2H3PO4
реакция соединения
ЦОР 3 Zn+CuSO4 →ZnSO4+Cu реакция замещения














 Обследование звукослоговой структуры слов с использованием ИКТ
Обследование звукослоговой структуры слов с использованием ИКТ Кіномистецтво
Кіномистецтво Проект на тему Человек, которым я горжусь. Владимир Иванович Даль 1801-1872
Проект на тему Человек, которым я горжусь. Владимир Иванович Даль 1801-1872 Иконопись. Русская икона
Иконопись. Русская икона День недели…
День недели… Эстетикалық стоматология үшін оптикалық жүйенің маңызы
Эстетикалық стоматология үшін оптикалық жүйенің маңызы Презентация Интегративный подход в организации экспериментальной деятельности младших дошкольников
Презентация Интегративный подход в организации экспериментальной деятельности младших дошкольников Автомобильные грузовые транспортные средства
Автомобильные грузовые транспортные средства Военно-мостовая подготовка. Итоговый тест
Военно-мостовая подготовка. Итоговый тест ЧПУ станоктары
ЧПУ станоктары Материнская плата
Материнская плата Презентация к классному часу Наши права и обязанности
Презентация к классному часу Наши права и обязанности Межзвёздная среда: Газ и пыль
Межзвёздная среда: Газ и пыль мультик
мультик класс
класс русский 08.02
русский 08.02 Случаи вычитания 16-
Случаи вычитания 16- Клятвы на новый год
Клятвы на новый год Контроль качества строительно-монтажных работ
Контроль качества строительно-монтажных работ Проблематика романа М. Булгакова Белая гвардия
Проблематика романа М. Булгакова Белая гвардия Разработка урока Планеты Солнечной системы.
Разработка урока Планеты Солнечной системы. Сотворение человека. Православная антропология
Сотворение человека. Православная антропология The degrees of comparison of adjectives
The degrees of comparison of adjectives Проектная деятельность обучающихся. Проект по теме Сколько весит здоровье ученика?
Проектная деятельность обучающихся. Проект по теме Сколько весит здоровье ученика? 20191208_kraevedcheskoe_kazino_loyma_i_eyo_okrestnosti
20191208_kraevedcheskoe_kazino_loyma_i_eyo_okrestnosti Советский Союз в 1950--1991 годах
Советский Союз в 1950--1991 годах Испытание № 6. Бутерброд NETWORKING
Испытание № 6. Бутерброд NETWORKING Загадки про игрушки (ранний возраст)
Загадки про игрушки (ранний возраст)