Содержание
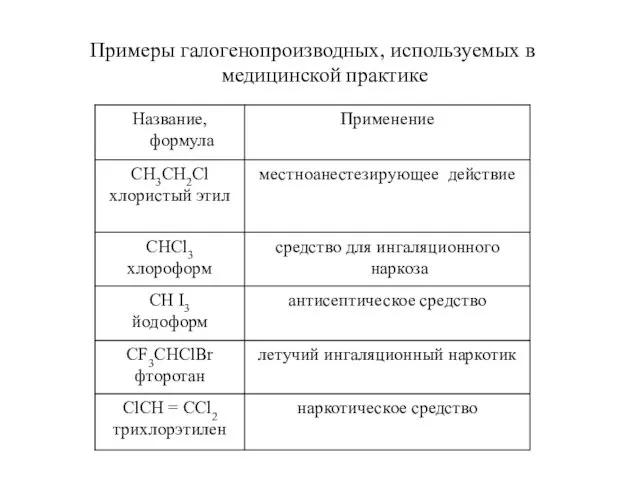
- 2. Примеры галогенопроизводных, используемых в медицинской практике
- 3. Кислотно-основные свойства соединений. По теории Беренстеда –Лоури кислоты - доноры протонов, основания – акцепторы протонов. В
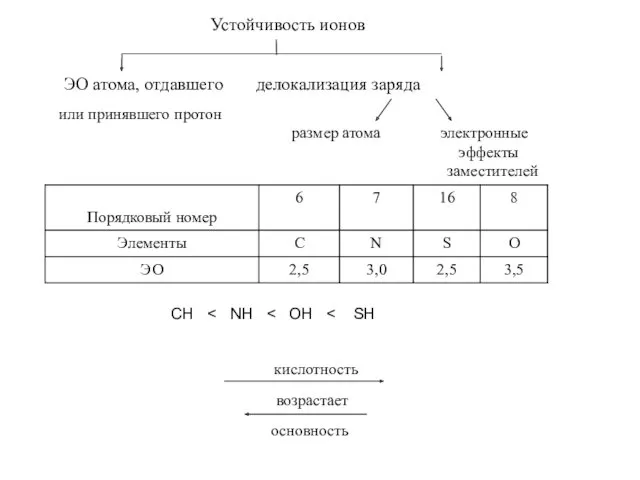
- 4. Устойчивость ионов ЭО атома, отдавшего делокализация заряда или принявшего протон размер атома электронные эффекты заместителей CH
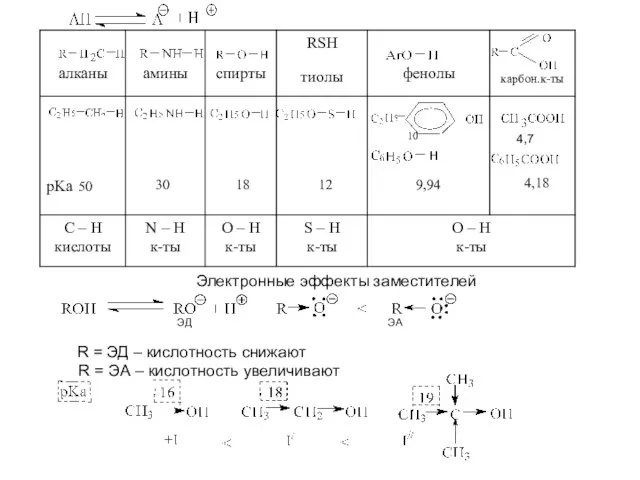
- 5. 10 Электронные эффекты заместителей ЭД ЭА R = ЭД – кислотность снижают R = ЭА –
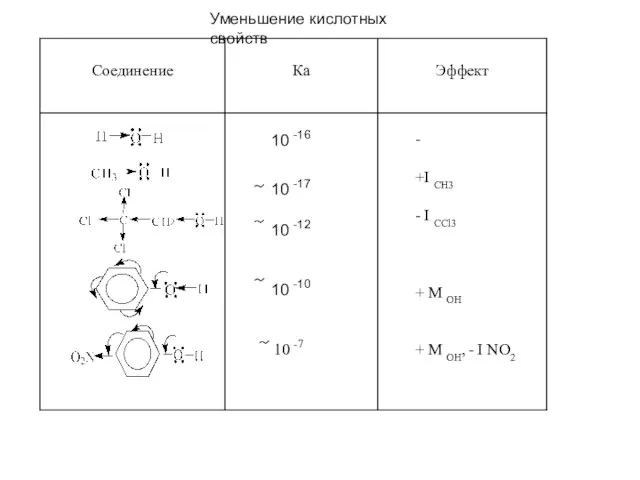
- 6. Уменьшение кислотных свойств
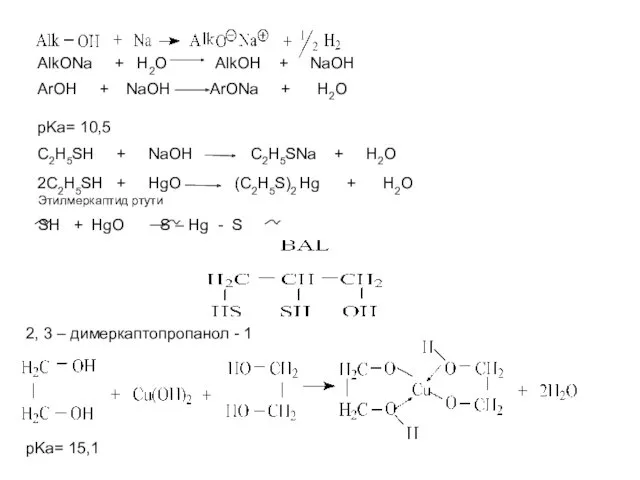
- 7. AlkONa + H2O AlkOH + NaOH ArOH + NaOH ArONa + H2O pKa= 10,5 C2H5SH +
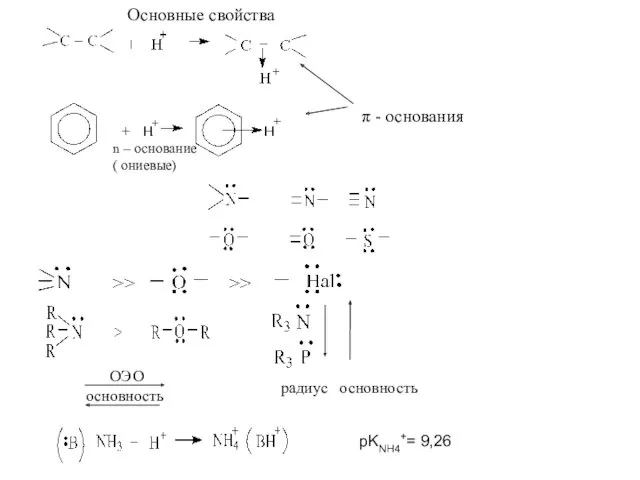
- 8. Основные свойства n – основание ( ониевые) ОЭО основность pKNH4+= 9,26 π - основания радиус основность
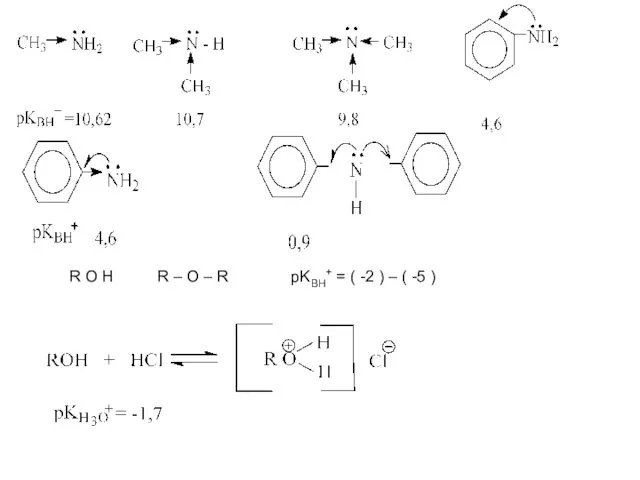
- 9. R O H R – O – R pKBH+ = ( -2 ) – ( -5
- 10. Реакции нуклеофильного замещения SN ( sp3 - ) уходящая группа Хорошо уходящая группа Плохо уходящая группа
- 11. Способность к SN реакциям зависит от факторов: 1) полярность связи электроотрицательность +М 2) легкость разрыва связи
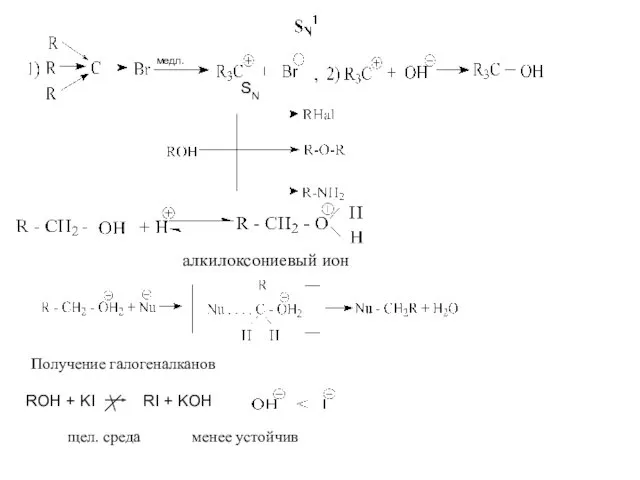
- 12. SN алкилоксониевый ион Получение галогеналканов ROH + KI RI + KOH щел. среда менее устойчив медл.
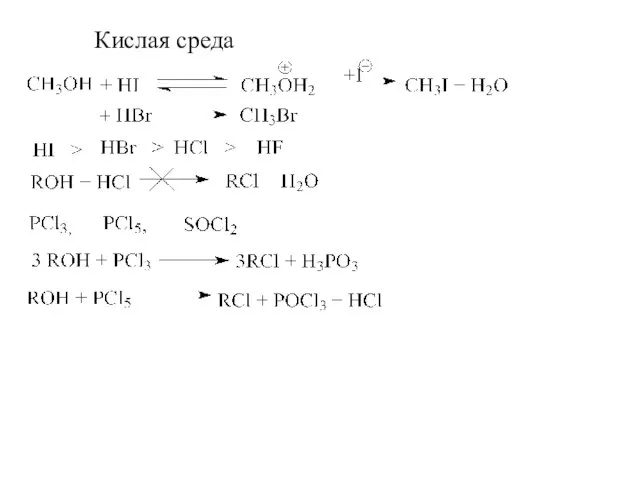
- 13. Кислая среда
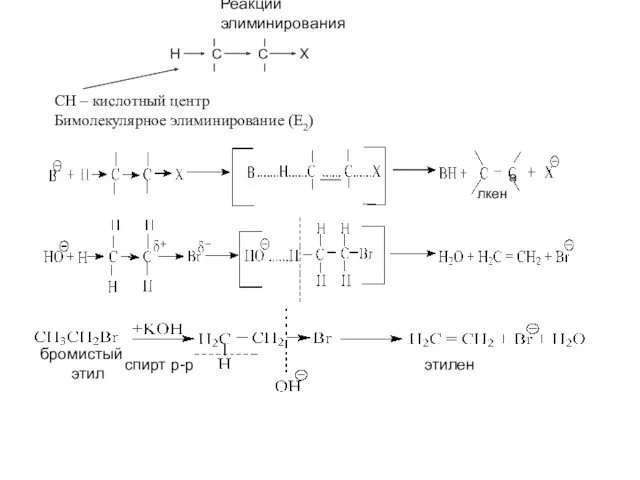
- 14. Реакции элиминирования H C C X CH – кислотный центр Бимолекулярное элиминирование (Е2) алкен спирт р-р
- 16. Скачать презентацию



 Формирование традиций классного коллектива
Формирование традиций классного коллектива Авторитарный режим и суперпрезидентская республика. Режим военной диктатуры, авторитарный национализм
Авторитарный режим и суперпрезидентская республика. Режим военной диктатуры, авторитарный национализм Политическое развитие в 60-80-х гг
Политическое развитие в 60-80-х гг Кирпич, терракота
Кирпич, терракота Презентация к стихотворению Маргариты Агашиной Перекресток
Презентация к стихотворению Маргариты Агашиной Перекресток Методология научного познания
Методология научного познания Установите счётчики. Принцип работы счётчика
Установите счётчики. Принцип работы счётчика Статистические методы определения показателей надежности аппаратного обеспечения автоматизированных систем
Статистические методы определения показателей надежности аппаратного обеспечения автоматизированных систем Презентация для учителей-логопедов Организационная сторона деятельности логопункта и ПМПк в ДОУ
Презентация для учителей-логопедов Организационная сторона деятельности логопункта и ПМПк в ДОУ Презинтация Ласковый сентябрь
Презинтация Ласковый сентябрь Курить-здоровью вредить
Курить-здоровью вредить Материаловедение. Производство чугуна и стали. Строение стального слитка. (Тема 4)
Материаловедение. Производство чугуна и стали. Строение стального слитка. (Тема 4) Подготовка к квалификационному экзамену в области оценочной деятельности по направлению Оценка недвижимости
Подготовка к квалификационному экзамену в области оценочной деятельности по направлению Оценка недвижимости Острая печёночная недостаточность
Острая печёночная недостаточность кинодискуссия - как
кинодискуссия - как Скорость химических реакций
Скорость химических реакций Лев Николаевич Толстой
Лев Николаевич Толстой Орта Азия халықтарының тарихындағы Әмір Темірдің рөлі
Орта Азия халықтарының тарихындағы Әмір Темірдің рөлі Верховино 1917-1920
Верховино 1917-1920 Грейды по уровням ответственности мануальных тестировщиков
Грейды по уровням ответственности мануальных тестировщиков Программно-методическое обеспечение по музыкальному воспитанию детей
Программно-методическое обеспечение по музыкальному воспитанию детей Культивирование жемчуга
Культивирование жемчуга Алексей Михайлович Романов (1629-1676)
Алексей Михайлович Романов (1629-1676) Обладнання для обертання породоруйнівного інструменту
Обладнання для обертання породоруйнівного інструменту Показательная функция
Показательная функция Проблемное обучение на уроках химии
Проблемное обучение на уроках химии Инструкция по технике безопасности обучающихся
Инструкция по технике безопасности обучающихся Комфортная городская среда
Комфортная городская среда