Содержание
- 2. Цели Ознакомиться с историей получения аммиака Рассмотреть основные научные принципы Изучить производство аммиака Рассмотреть области применения
- 3. Габер Фриц Синтез аммиака – процесс связывания азота, который впервые осуществил известный немецкий химик - неорганик
- 4. Карл Бош Немецкие исследователи Ф.Габер и К.Бош создали циркуляционную схему синтеза аммиака под давлением. В 1913
- 5. Подбор оптимальных условий проведения синтеза: N2 + 3H2 = 2NH3 Реакция обратимая, гомогенная и идет с
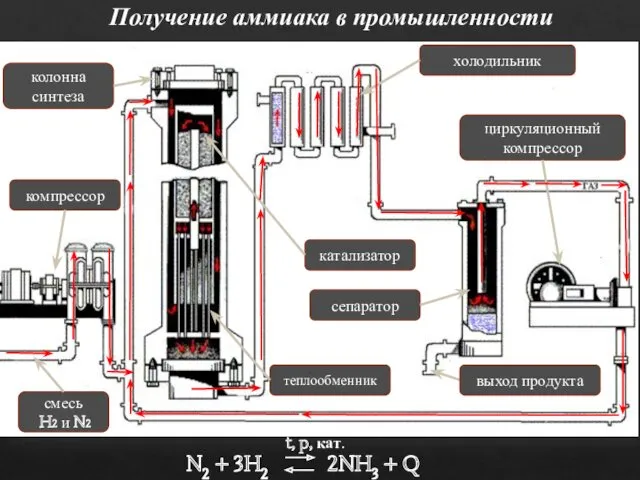
- 6. Получение аммиака в промышленности теплообменник катализатор выход продукта циркуляционный компрессор колонна синтеза
- 7. Научные принципы
- 8. Другие способы получения аммиака Дуговой метод Дуговой метод основан на прямом окислении азота атмосферным воздухом при
- 9. Применение аммиака -аммиачная вода -мочевина -сода пищевая промышленность (хладагент) удобрения HNO3
- 10. Последствия несчастных случаев Выбросы аммиака в атмосферу вызывают серьезную тревогу в обществе и средствах массовой информации.
- 11. Действие аммиака на организм Аммиак сильно раздражает слизистые оболочки уже при 0,5%-ном содержании его в воздухе.
- 12. Способы борьбы с загрязнением окружающей среды 1) Cтроительство различных очистных сооружений. 2) Создание и внедрение безотходных
- 14. Скачать презентацию










 Мета, зміст і організація управлінського обліку, його взаємозв'язок з фінансовим обліком
Мета, зміст і організація управлінського обліку, його взаємозв'язок з фінансовим обліком Особенности развития управления качеством в России
Особенности развития управления качеством в России Крым и Россия - мы вместе
Крым и Россия - мы вместе Мой любимый 1 класс Б
Мой любимый 1 класс Б Николай Михайлович Рубцов Берёзы
Николай Михайлович Рубцов Берёзы Государственный бюджет РФ. Функции государственного бюджета
Государственный бюджет РФ. Функции государственного бюджета Олимпийские символы и талисманы
Олимпийские символы и талисманы Пусковые свойства трехфазных асинхронных двигателей с короткозамкнутым ротором. Пуск асинхронных двигателей с фазным ротором
Пусковые свойства трехфазных асинхронных двигателей с короткозамкнутым ротором. Пуск асинхронных двигателей с фазным ротором Методология и методы педагогики
Методология и методы педагогики Формирование нравственно-патриотических качеств у младших школьников.
Формирование нравственно-патриотических качеств у младших школьников. Пассивные помехи, ложные цели и ловушки. Тема 8
Пассивные помехи, ложные цели и ловушки. Тема 8 Инвестиционные проекты в нефтегазохимическом комплексе РТ
Инвестиционные проекты в нефтегазохимическом комплексе РТ Окончание смутного времени
Окончание смутного времени Обогащение полезных ископаемых. Гравитационный метод обогащения. (Лекция 10)
Обогащение полезных ископаемых. Гравитационный метод обогащения. (Лекция 10) Софизмы в алгебре
Софизмы в алгебре US Sales Analysis
US Sales Analysis Құрылыс алаңдары
Құрылыс алаңдары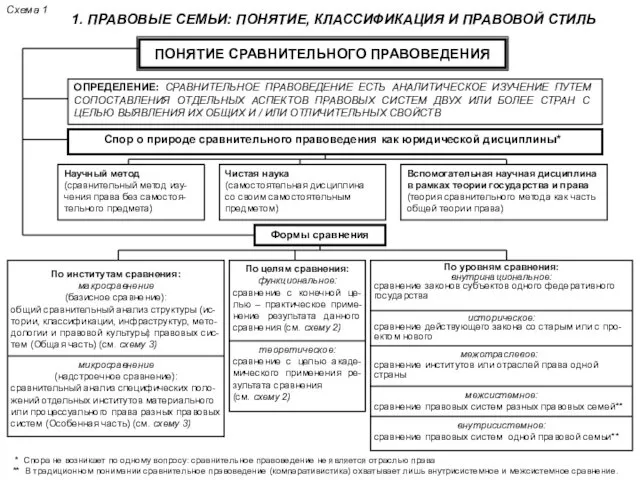 Правовые семьи: понятие, классификация и правовой стиль
Правовые семьи: понятие, классификация и правовой стиль О применении инновационных, в том числе нанотехнологических решений в проекте Сила Сибири и на других объектах ПАО Газпром
О применении инновационных, в том числе нанотехнологических решений в проекте Сила Сибири и на других объектах ПАО Газпром Инвестиционный анализ. (Часть 1)
Инвестиционный анализ. (Часть 1) Портфолио
Портфолио Среда обитания живых организмов. 5 класс. Диск
Среда обитания живых организмов. 5 класс. Диск Методы обнаружения утечек в магистральных нефтепроводах
Методы обнаружения утечек в магистральных нефтепроводах Природа процесса принятия управленческого решения
Природа процесса принятия управленческого решения Картотетка физкультминуток для дошкольников
Картотетка физкультминуток для дошкольников Виртуальная выставка, посвященная юбилею Ларисы Юрьевны Карпенко
Виртуальная выставка, посвященная юбилею Ларисы Юрьевны Карпенко Получение ткани. Ткачество
Получение ткани. Ткачество Подтип хелицеровые. Паукообразные
Подтип хелицеровые. Паукообразные