Апатитовый концентрат содержит примеси – органические вещества, соединения металлов переменной валентности
(железа или церия), являющихся восстановителями по отношению к азотной кислоте.
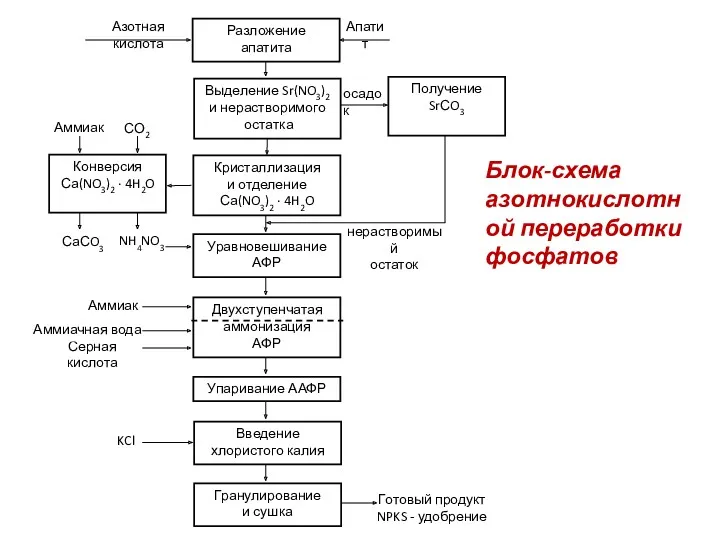
В результате побочных химических реакций, протекающих при вскрытии апатита, в газовую фазу кроме H2SiF6, СО2, паров Н2О выделяются оксиды азота. Для предотвращения газовыделения АК обрабатывается карбамидом в количестве 4 – 5 кг на 1 тонну фосфатного сырья.
2СО(NН2)2 + 3NО2 → 3,5N2 + 2СО2 + 4Н2О, (12)
2СО(NН2)2 + 6NО → 5N2 + 2СО2 + 4Н2О (13)
Однако избыток СО(NН2)2 ухудшает отстой АКВ при сгущении осадка на стадии ее осветления. Это связано с вступлением карбамида в реакцию поликонденсации с ФК, содержащейся в АКВ, и адсорбцией образующихся продуктов на поверхности твердых частиц, что способствует их гидрофобизации.
В результате газы (N2, СО2 и др.), выделяющиеся при взаимодействии оксидов азота с карбамидом, флотируют осадок и препятствуют его отстаиванию.









 Военная служба – особый вид государственной службы
Военная служба – особый вид государственной службы Знакомство дошкольников с дорожными знаками.
Знакомство дошкольников с дорожными знаками. Stylistic analysis of the texts of different functional styles. Lecture 10
Stylistic analysis of the texts of different functional styles. Lecture 10 Живая и неживая природа. Признаки живой природы
Живая и неживая природа. Признаки живой природы Емдік-евакуациялық іс-шараларды ұйымдастыру
Емдік-евакуациялық іс-шараларды ұйымдастыру АО Телеканал НТВ
АО Телеканал НТВ Памятники, памятные места и памятные знаки Отечественной войны 1812 года.
Памятники, памятные места и памятные знаки Отечественной войны 1812 года. 20231013_volgodonskoy_pedagogicheskiy_kolledzh_gbpou_ro_vpk
20231013_volgodonskoy_pedagogicheskiy_kolledzh_gbpou_ro_vpk Электрические цепи однофазного синусоидального тока
Электрические цепи однофазного синусоидального тока Социологический проект Огюста Конта. Социологические законы и категории
Социологический проект Огюста Конта. Социологические законы и категории Конструктивные особенности и устройство БПЛА мультироторного типа
Конструктивные особенности и устройство БПЛА мультироторного типа Внеучебная жизнь студентов
Внеучебная жизнь студентов 4
4 Банки, их функции. Понятие банковская услуга
Банки, их функции. Понятие банковская услуга Подгруппа мышьяка
Подгруппа мышьяка First developing writing and assessment
First developing writing and assessment подготовка к ЕГЭ.Методика решения графических задач по физике
подготовка к ЕГЭ.Методика решения графических задач по физике Экскурсия по уголку живой природы
Экскурсия по уголку живой природы Неравенство треугольника. Урок 46
Неравенство треугольника. Урок 46 Готовимся к 4 классу
Готовимся к 4 классу Education in Great Britain and Belarus
Education in Great Britain and Belarus Знакомство с персональным компьютером. IT Essentials: программное и аппаратное обеспечение ПК v5.0
Знакомство с персональным компьютером. IT Essentials: программное и аппаратное обеспечение ПК v5.0 Повестка общетехникумовского родительского собрания
Повестка общетехникумовского родительского собрания Технические средства и оборудование локальных сетей ЭВМ
Технические средства и оборудование локальных сетей ЭВМ Противофазное включение двигателей СН в момент восстановления питания. ЭЧСЭСП, часть 4, лекции 35-45
Противофазное включение двигателей СН в момент восстановления питания. ЭЧСЭСП, часть 4, лекции 35-45 Теплофикационная установка (ТФУ)
Теплофикационная установка (ТФУ) Презентация к уроку по теме Масштаб и его виды 5 класс ФГОС.
Презентация к уроку по теме Масштаб и его виды 5 класс ФГОС. Общий обзор организма человека
Общий обзор организма человека