Содержание
- 2. Серебро. Общая информация. Положение в Периодической системе: IB группа, 5-й период Электронная конфигурация: [Kr]5s14d10 (проскок электрона!)
- 3. Серебро. Применение Драгоценный металл Электротехника – провода, схемы, контакты, покрытия катодов. Серебро обладает еще большей электропроводностью
- 4. Серебро. Получение 70 место по распространенности в земной коре (редкий элемент!) Распространено по всему миру. Основные
- 5. Хим. свойства Ag0 Правее водорода (и меди) в ряду напряжений. В кислотах-неокислителях и щелочах не растворяется.
- 6. Хим. свойства Ag0 2Ag + 2H2SO4(конц.) →(t°C) Ag2SO4 + SO2 + 2H2O Взаимодействие с простыми веществами:
- 7. Хим. свойства Ag+1 “AgOH” – был бы щелочью, если бы он существовал Ag2O + 2HNO3(разб.) →
- 8. Хим. свойства Ag+1 Многообразие осадков: 1. AgNO3 + NaI → AgI↓ (желтый) + NaNO3 AgCl –
- 9. Хим. свойства Ag+1 Растворение осадков за счет комплексообразования: AgCl + 2NH3 → [Ag(NH3)2]Cl (бесцветный р-р) AgBr
- 10. Серебро. Высокие степени окисления Ag + F2 →(на холоду) “AgF2” На самом деле “AgF2” = Ag+1[Ag+3F4]
- 11. Цинк. Общая информация. Положение в Периодической системе: IIB группа, 4-й период Электронная конфигурация: [Ar]4s23d10 (заполненный d-подуровень)
- 12. Цинк. Применение Около 50% всего потребления – антикоррозионные покрытия (оцинковка) для стали, меди и других металлов/сплавов
- 13. Цинк. Получение 24-й по распространенности в земной коре (медь – 25-я). Основные добывающие страны: Китай, Перу,
- 14. Хим. свойства Zn0 Левее водорода в ряду напряжений металлов. Довольно активный металл. Растворяется в кислотах и
- 15. Хим. свойства Zn+2 Zn(OH)2 – типичный амфотерный гидроксид. Zn(OH)2 + 2HCl → ZnCl2 + 2H2O Zn(OH)2
- 16. Хим. свойства Zn+2 Примеры осадков: 1. ZnCl2 + (NH4)2CO3 → ZnCO3↓ (белый) + 2NH4Cl 2. ZnSO4
- 17. Алюминий. Общая информация. Положение в Периодической системе: IIIA группа, 3-й период Электронная конфигурация: [Ne]3s23p1 (p-элемент!) Степень
- 18. Алюминий. Применение Сплавы - универсальный конструкционный материал. Легкие (по сравнению со сплавами железа) и тоже дешевые.
- 19. Алюминий. Получение Самый распространенности в земной коре металл (и 3-й среди всех элементов после O и
- 20. Хим. свойства Al0 Очень активный металл. На воздухе покрыт прочной оксидной пленкой. После её снятия (кратковременного
- 21. Хим. свойства Al+3 Al(OH)3 – типичный амфотерный гидроксид. Все реакции, характерные для амфотерных гидроксидов. Соли и
- 22. Свинец. Общая информация. Положение в Периодической системе: IVA группа, 6-й период Электронная конфигурация: [Xe]6s24f145d106p2 (p-элемент!) Степень
- 23. Свинец. Применение Свинцовые аккумуляторы (очень широко распространены, например, в автомобилях) PbO2 + 4H+ + SO42– +
- 24. Свинец. Получение 60-й по распространенности элемент (довольно редкий). Основная добывающая страна: Китай – более 50% мировой
- 25. Хим. свойства Pb0 Малоактивный металл. В ряду напряжений – близко к водороду (левее). Пассивируется растворами HCl
- 26. Хим. свойства Pb+2 Pb(OH)2 – амфотерный гидроксид. Для PbO и Pb(OH)2 – все реакции, характерные для
- 27. Хим. свойства Pb+2 Характерные осадки: 1. Pb(NO3)2 + 2NaI → PbI2↓ (золотисто-желтый) + 2NaNO3 PbCl2, PbBr2
- 29. Скачать презентацию


























 Презентация Коллективная разработка ПО
Презентация Коллективная разработка ПО Невынашивание беременности
Невынашивание беременности Мікропроцесорна техніка (лекція 7)
Мікропроцесорна техніка (лекція 7)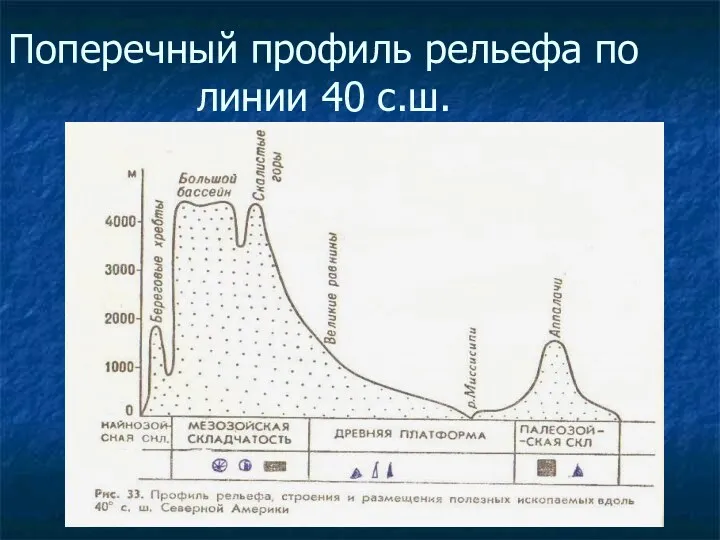 7 класс: Оледенение С.Америки
7 класс: Оледенение С.Америки Чем археолог отличается от криминалиста. Социальные ландшафты: вещи в динамике прошлого
Чем археолог отличается от криминалиста. Социальные ландшафты: вещи в динамике прошлого Functional styles of the english language: newspaper style
Functional styles of the english language: newspaper style Статус - отчет по ремонту Сормовский 3060
Статус - отчет по ремонту Сормовский 3060 К юбилею В.Г. Распутина, Героя Социалистического Труда, дважды лауреата Государственной премии СССР
К юбилею В.Г. Распутина, Героя Социалистического Труда, дважды лауреата Государственной премии СССР Планиметрия. Повторение. Часть 1
Планиметрия. Повторение. Часть 1 Мартеновский способ производства стали. Выплавка стали в электропечах
Мартеновский способ производства стали. Выплавка стали в электропечах How to present in English
How to present in English Интеллектуальные роботы состояние и перспективы
Интеллектуальные роботы состояние и перспективы Презентация С правом по жизни.
Презентация С правом по жизни. особенности изображения Земли на глобусе и на карте
особенности изображения Земли на глобусе и на карте Декоративные злаки
Декоративные злаки Мы вместе. Часть 2
Мы вместе. Часть 2 Рисуем пластилином
Рисуем пластилином Монтаж и эксплуатация ПВО. Противовыбросовое оборудование иностранных производителей
Монтаж и эксплуатация ПВО. Противовыбросовое оборудование иностранных производителей Философия Августина Блаженного
Философия Августина Блаженного Классный час 1сентября Эхо Бесланской печали
Классный час 1сентября Эхо Бесланской печали Конспект урока географии в 6 классе Тайны подземных бурь.
Конспект урока географии в 6 классе Тайны подземных бурь. Закрепление изученного в 4 классе
Закрепление изученного в 4 классе Стандартизация свойств. Физические, механические, физико-химические свойства СМ. Долговечность и надежность
Стандартизация свойств. Физические, механические, физико-химические свойства СМ. Долговечность и надежность презентация
презентация Биосфера Земли. Тест
Биосфера Земли. Тест Презентация Автоматизация звука Л в словах
Презентация Автоматизация звука Л в словах Священная Библейская история Ветхого Завета. Грехопадение и его последствия (Быт.3)
Священная Библейская история Ветхого Завета. Грехопадение и его последствия (Быт.3) Нарушения обмена хромопротеидов
Нарушения обмена хромопротеидов