Содержание
- 2. Скорость химических реакций - Это изменение концентрации одного из реагирующих или одного из продуктов реакции в
- 3. Химические реакции Гомогенные - реагирующие вещества и продукты реакции находятся в одной фазе 2SO2 (г) +
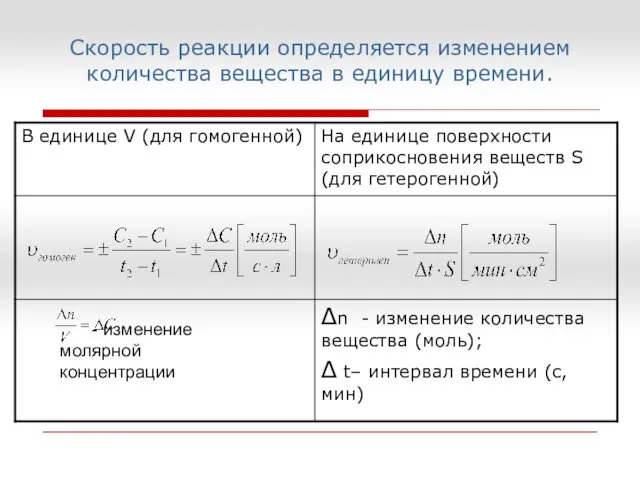
- 4. Скорость реакции определяется изменением количества вещества в единицу времени. - изменение молярной концентрации
- 5. Факторы, влияющие на скорость химической реакции природа реагирующих веществ; температура; концентрация реагирующих веществ; действие катализаторов; поверхность
- 6. Теория столкновений. Основная идея её такова: реакции происходят при столкновении частиц реагентов, которые обладают определённой энергией.
- 7. 1. Природа реагирующих веществ. Под природой реагирующих веществ понимают их состав, строение, взаимное влияние атомов в
- 8. 2. Температура При увеличении температуры на каждые 10° С общее число столкновений увеличивается только на ~
- 9. 3. Концентрации реагирующих веществ. На основе большого экспериментального материала в 1867 г. норвежские учёные К. Гульдберг,
- 10. Математическое выражение закона действующих масс. По закону действующих масс скорость реакции, уравнение которой А+В=С может быть
- 11. 4. Действие катализатора Обсуждение вопросов: 1.Что такое катализатор и каталитические реакции? 2. Приведите примеры известных вам
- 12. 5.Поверхность соприкосновения реагирующих веществ. Скорость реакции увеличивается благодаря: -увеличению площади поверхности соприкосновения реагентов (измельчение); -повышению реакционной
- 14. Скачать презентацию










 Problem of the oil reserves and possible way to solve it
Problem of the oil reserves and possible way to solve it Алексей Петрович Маресьев
Алексей Петрович Маресьев Базовые характеристики микроконтроллеров семейства F2803x Piccolo
Базовые характеристики микроконтроллеров семейства F2803x Piccolo Личный бренд педагога как способ показать свою экспертность
Личный бренд педагога как способ показать свою экспертность Мультиплексор
Мультиплексор Лассификация альтернативных топлив. Сжиженные и сжатые газы
Лассификация альтернативных топлив. Сжиженные и сжатые газы Програмне забезпечення для автоматизації процесу взаємодії з клієнтами
Програмне забезпечення для автоматизації процесу взаємодії з клієнтами История создания георгиевской ленты
История создания георгиевской ленты Николай Николаевич Носов Приключения Незнайки и его друзей
Николай Николаевич Носов Приключения Незнайки и его друзей История развития учений о двс. Основные понятия и определения (лекция 5)
История развития учений о двс. Основные понятия и определения (лекция 5) Климатические пояса Земли
Климатические пояса Земли Путешествие по Тулате
Путешествие по Тулате Николай Петрович Майоров
Николай Петрович Майоров Орієнтування в списку книг електронної бібліотеки
Орієнтування в списку книг електронної бібліотеки Словарные слова
Словарные слова Устойчивость функционирования объектов экономики
Устойчивость функционирования объектов экономики Ecosystem services
Ecosystem services Сети TCP/IP
Сети TCP/IP Кремний
Кремний Вестибулярное головокружение в неотложной неврологии
Вестибулярное головокружение в неотложной неврологии Презентация Видовое разнообразие Пингвиновых
Презентация Видовое разнообразие Пингвиновых Санкт-Петербург - промышленный центр России и Европы
Санкт-Петербург - промышленный центр России и Европы Практическая работапо теме:Внутренние воды Африки
Практическая работапо теме:Внутренние воды Африки Приметы осени
Приметы осени Диссоциация кислот, щелочей и солей
Диссоциация кислот, щелочей и солей Егіз ұрықпен босанушы әйелдерде босанғаннан кейін қан кетудің алдын алу
Егіз ұрықпен босанушы әйелдерде босанғаннан кейін қан кетудің алдын алу Великие русские химики
Великие русские химики урок мужества
урок мужества