Содержание
- 2. Гомогенные и гетерогенные системы Гетерогенные системы Фаза – совокупность всех гомогенных частей системы, одинаковых по составу
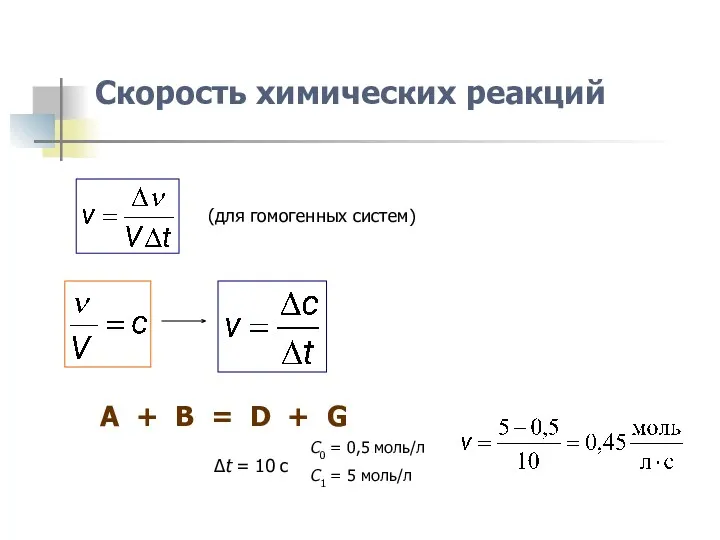
- 3. Скорость химических реакций (для гомогенных систем) A + B = D + G C0 = 0,5
- 4. Скорость химических реакций (для гомогенных систем) A + B = D + G C0 = 2
- 5. Факторы, от которых зависит скорость реакции Природа реагирующих веществ Концентрация веществ в системе Площадь поверхности (для
- 6. Влияние температуры Правило Вант-Гоффа При нагревании системы на 10 ˚С скорость реакции возрастает в 2-4 раза
- 7. Катализ Йенс Якоб Берцелиус ввел термин «катализ» в 1835 г. Катализатор – вещество, изменяющее скорость реакции,
- 8. Механизм разложения пероксида водорода 2H2O2 = 2H2O + O2 (1) H2O2 = H+ + HO2- (2)
- 9. Разложение H2O2 в присутствии Fe3+ H2O2 = H+ + HO2- HO2- + Fe3+ = Fe2+ +
- 10. 17 белых верблюдов Кай Линдерстрём-Ланг (1896-1959) Притча о катализе + 1 черный верблюжонок 1/2 1/3 1/9
- 11. Терминология Катализ, катализатор Ингибитор Промоторы Каталитические яды Гомогенный и гетерогенный катализ Ферменты
- 12. Особенности ферментативного катализа Высокая избирательность и специфичность катализатора Жесткие требования к условиям протекания реакций Классификация ферментов
- 13. Теперь к вопросам ЕГЭ!
- 14. A20-2008-1 На скорость химической реакции между раствором серной кислоты и железом не оказывает влияния 1) концентрация
- 15. A20-2008-2 Для увеличения скорости химической реакции Mg (тв.) + 2H+ = Mg2+ + H2(г.) необходимо 1)
- 16. A20-2008-3 C наибольшей скоростью при обычных условиях протекает реакция 1) 2Ba + O2 = 2BaO 2)
- 17. A20-2008-4 Для увеличения скорости реакции 2CO + O2 = 2CO2 + Q необходимо 1) увеличить концентрацию
- 18. A20-2008-5 Для увеличения скорости реакции Zn (тв.) + 2H+ = Zn2+ + H2(г.) необходимо 1) уменьшить
- 19. 1) Zn + HCl (5%p-p) 2) Zn + HCl (10%p-p) 3) Zn + HCl (20%p-p) 4)
- 20. С наименьшей скоростью при обычных условиях протекает реакция 1) Fe + O2 2) CaCO3 + HCl
- 22. Скачать презентацию


















 Юридические лица как субъекты гражданских правоотношений
Юридические лица как субъекты гражданских правоотношений Турнир любителей прекрасной науки – математики
Турнир любителей прекрасной науки – математики Внутренняя среда организма Кровь
Внутренняя среда организма Кровь Стандарт КП пример- восстановлен
Стандарт КП пример- восстановлен классный час на тему: Курение
классный час на тему: Курение 20231002_7_kl_svetlyachki
20231002_7_kl_svetlyachki Методика преподавания права как учебная дисциплина. Организационно-правовые основы профессионального образования в РФ (Лекция 1)
Методика преподавания права как учебная дисциплина. Организационно-правовые основы профессионального образования в РФ (Лекция 1) Проведение работы свайных фундаментов в сезоннопромерзающих грунтах
Проведение работы свайных фундаментов в сезоннопромерзающих грунтах Деловое общение
Деловое общение Выращивание кристаллов в домашних условиях
Выращивание кристаллов в домашних условиях Железобетонные бункера
Железобетонные бункера Презентация-рекомендации родителям Во что играют наши дети?
Презентация-рекомендации родителям Во что играют наши дети? О живой физике в начальном звене
О живой физике в начальном звене Семья пастора
Семья пастора Презентации для занятий кружка Умники и умницы
Презентации для занятий кружка Умники и умницы Интерфейс RS-232
Интерфейс RS-232 Ранние половые связи и их последствия
Ранние половые связи и их последствия Типичные неотложные состояния
Типичные неотложные состояния Физкультминутки в ДОУ
Физкультминутки в ДОУ Грибы съедобные и несъедобные. Правила сбора грибов. 3 класс
Грибы съедобные и несъедобные. Правила сбора грибов. 3 класс Направление Добро и Зло (2)
Направление Добро и Зло (2) золотая хохлома
золотая хохлома Қол ұшы флегмонасы
Қол ұшы флегмонасы My favourite food
My favourite food Организация сюжетно - ролевой игры в средней группе.
Организация сюжетно - ролевой игры в средней группе. Руководство пользователя серийного пульта управления
Руководство пользователя серийного пульта управления Азаматтық қоғам мен құқықтық мемлекет
Азаматтық қоғам мен құқықтық мемлекет Кормові добавки в годівлі об’єктів рибництва
Кормові добавки в годівлі об’єктів рибництва