Содержание
- 2. Основные положения теории растворов электролитов. Процесс электролитической диссоциации изображают химическими уравнениями, например: Степень электролитической диссоциации По
- 3. Константа диссоциации слабого электролита Константа равновесия, отвечающая диссоциации слабого электролита, называется константой диссоциации
- 4. Закон разбавления Оствальда При разбавлении степень диссоциации увеличивается – активность данного иона – коэффициент активности иона
- 5. Кислотно-основные равновесия в водных растворах В соответствие с протолитической теорией Бренстеда и Лоури все частицы, способные
- 6. Кислотно-основные равновесия в водных растворах согласно современным представлениям в воде осуществляется протолитическое равновесие – автопротолиз воды:
- 7. Кислотно-основные равновесия в водных растворах pH = 7, нейтральная среда pH pH > 7, щелочная среда
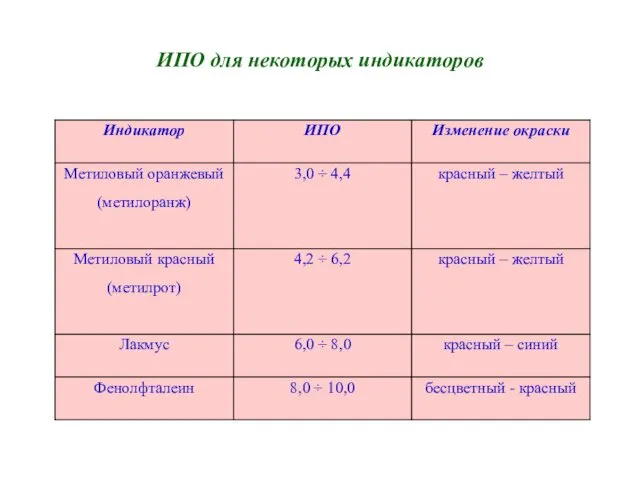
- 8. ИПО для некоторых индикаторов
- 9. Действие одноименнных ионов Степень диссоциации слабого электролита понижается при введении в раствор какого-либо сильного электролита, содержащего
- 10. Буферные растворы Количественной характеристикой способности буферного раствора поддерживать заданную величину pH является буферная емкость, под которой
- 11. Гидролиз солей Количественно гидролиз характеризуется степенью гидролиза h, которая равна отношению числа прогидролизровавшихся частиц nгидр к
- 12. Гидролиз солей При этом, чем слабее образующаяся в результате гидролиза кислота (меньше Ka), тем более сильным
- 13. Гидролиз солей 3. Гидролиз солей, содержащих катион слабого однокислотного основания и анион слабой одноосновной кислоты (ВА).
- 14. Гидролиз солей Так как Kа1 > Ka2, то Kh1 > Kh2 Na2S, K2CO3, Na2SO3, Na2C2O4 K3PO4,
- 15. Произведение растворимости Гетерогенная (неоднородная) система – это система, состоящая из нескольких гомогенных фаз, разделенных между собой
- 16. Произведение растворимости Правило произведения растворимости: произведение активностей ионов в степенях, равных стехиометрическим коэффициентам, в насыщенном растворе
- 17. Произведение растворимости Растворимость зависит 1. от природы малорастворимого соединения, 2. природы растворителя, 3. температуры, 4. давления,
- 19. Скачать презентацию















 Восстание под руководством Емельяна Пугачёва (1773 – 1775 гг.)
Восстание под руководством Емельяна Пугачёва (1773 – 1775 гг.) ПРЕЗЕНТАЦИЯ К МЕРОПРИЯТИЮ ДЛЯ ДЕТЕЙ ПОДГОТОВИТЕЛЬНОЙ ГРУППЫ Я — ПЕРВОКЛАССНИК Диск
ПРЕЗЕНТАЦИЯ К МЕРОПРИЯТИЮ ДЛЯ ДЕТЕЙ ПОДГОТОВИТЕЛЬНОЙ ГРУППЫ Я — ПЕРВОКЛАССНИК Диск Washington is the capital of the United States of America
Washington is the capital of the United States of America ВВЭР (водо-водяной энергетический реактор)
ВВЭР (водо-водяной энергетический реактор) Презентация Парад Победы
Презентация Парад Победы Организация свадебного торжества
Организация свадебного торжества Християнська етика. Щедрість і захланність
Християнська етика. Щедрість і захланність Современные средства поражения
Современные средства поражения prezetantsia
prezetantsia Презентация Проектная технология в начальной школе
Презентация Проектная технология в начальной школе Коротковой Юлии, юс1-11
Коротковой Юлии, юс1-11 past simple
past simple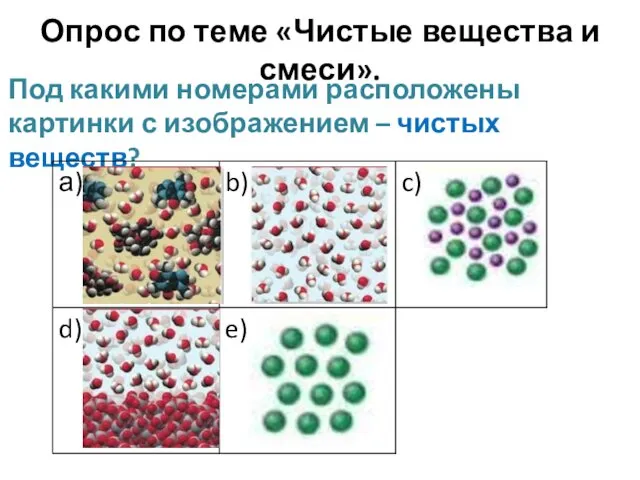 Классификация веществ. Приготовление растворов. Расчёт массовой доли растворённого вещества
Классификация веществ. Приготовление растворов. Расчёт массовой доли растворённого вещества Пізня зрілість (Е. Еріксон)
Пізня зрілість (Е. Еріксон) Проект Вместе лучше. Концепция воспитательной работы в классе.
Проект Вместе лучше. Концепция воспитательной работы в классе. Информационные технологии. Структура технологической системы
Информационные технологии. Структура технологической системы Детская игровая комната
Детская игровая комната Эпоха Просвещения
Эпоха Просвещения Реконструкция и реновация особняков России
Реконструкция и реновация особняков России Presentation Zilubag for customers
Presentation Zilubag for customers Асфиксия – жизнеугрожающее состояние, связанное с нарушением газообмена
Асфиксия – жизнеугрожающее состояние, связанное с нарушением газообмена Предмет органической химии
Предмет органической химии Автозаправочные станции
Автозаправочные станции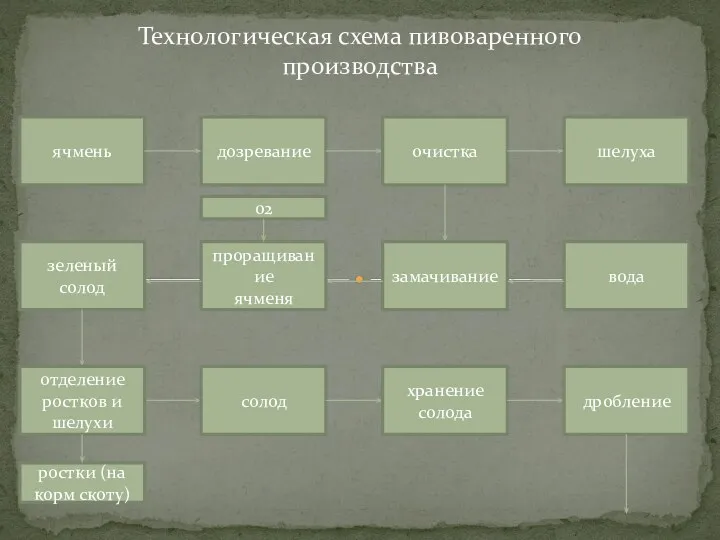 Технология производства пива
Технология производства пива Артикли в английском языке
Артикли в английском языке Сушка
Сушка урок по технологии обработки древесины на деревообрабатывающих станках
урок по технологии обработки древесины на деревообрабатывающих станках Овощи (большой - маленький). Уроки логопеда
Овощи (большой - маленький). Уроки логопеда