Содержание
- 2. цели урока Сформировать представление о практическом значении соляной кислоты; Актуализировать прежние знания о химических и физических
- 3. вопросы Назовите формулу соляной кислоты? Из каких двух элементов состоит соляная кислота? Элементы образующие молекулу хлороводорода
- 4. Задания Запишите электронное строение для атома хлора и водорода. Запишите электронно-графическую формулу для атома хлора и
- 5. С какими из перечисленных веществ будет реагировать бром. Хлор; Медь; Вода; Цинк; Водород;
- 6. Осуществите цепочку превращений и запишите химические реакции. Хлор Хлорид меди(II) Гидроксид меди(II) Оксид меди(II) Медь Хлорид
- 7. Химические свойства соляной кислоты. 1. Изменение окраски индикаторов(лакмуса метилоранжа); 2. Взаимодействие с металлами, стоящими в ряду
- 8. 3. Взаимодействие с основными и амфотерными оксидами. 2HCI + CaO = CaCI2 + H2O 6HCI +
- 9. 5.Взаимодействие с солями: 2HCI + CaCO3 = CaCI2 + H2CО3 Качественная реакция на соляную кислоту и
- 10. Получение хлороводорода. В промышленности H2 + CI2 = 2HCI В лаборатории 2NaCI(тв)+H2SO4 = Na2SO4+2HCI
- 11. Каменная соль (NaCI)
- 12. Вычислите массу осадка, который образуется при взаимодействии хлорида натрия массой 30г с раствором нитрата серебра. задача
- 13. задание с какими веществами будет реагировать соляная кислота ZnO, Fe(OH)3, Cu, Ca,
- 15. Скачать презентацию












 Разработка ассортимента и процесс приготовления сложных муссовых пирожных с ягодными компонентами на предприятии ООО Содексо
Разработка ассортимента и процесс приготовления сложных муссовых пирожных с ягодными компонентами на предприятии ООО Содексо Викторина ВИННИ ПУХ
Викторина ВИННИ ПУХ Реализация проектов в Горнозаводском городском округе
Реализация проектов в Горнозаводском городском округе Материаловедение и технология конструкционных материалов раздел ТКМ
Материаловедение и технология конструкционных материалов раздел ТКМ Локальные и глобальные компьютерные сети
Локальные и глобальные компьютерные сети Ядерная и радиационная безопасность (ЯРБ)
Ядерная и радиационная безопасность (ЯРБ)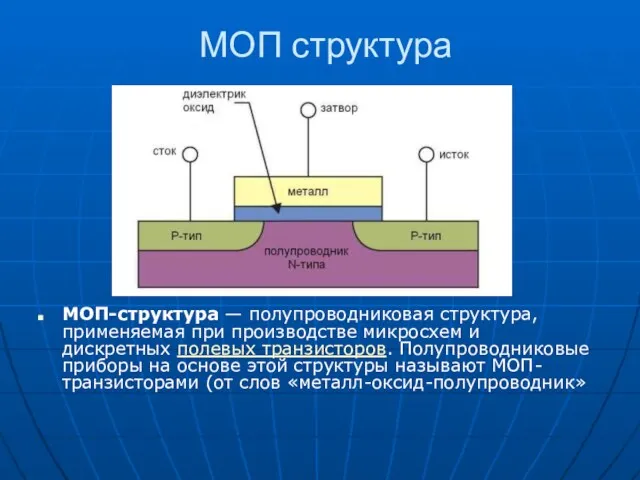 МОП и КМОП структуры
МОП и КМОП структуры Необычные растения и животные в природе
Необычные растения и животные в природе Инфекция. Роль микроорганизмов в развитии инфекционных заболеваний человека
Инфекция. Роль микроорганизмов в развитии инфекционных заболеваний человека Экология города
Экология города Ученический информационный проект Игра света
Ученический информационный проект Игра света Пожарная безопасность, организация противопожарной защиты учреждения
Пожарная безопасность, организация противопожарной защиты учреждения Осадочные горные породы
Осадочные горные породы Презентация к классному часу в 3 классе по теме Моя малая Родина - Шаховская
Презентация к классному часу в 3 классе по теме Моя малая Родина - Шаховская Дифференциация звуков [р] - [л]
Дифференциация звуков [р] - [л] Тест по художественной литературе для дошколят
Тест по художественной литературе для дошколят В мире звуков.
В мире звуков. Цифровые образовательные ресурсы на уроках химии.
Цифровые образовательные ресурсы на уроках химии. Мои этнические корни. Этнография
Мои этнические корни. Этнография Digital Signal Processing - ADC
Digital Signal Processing - ADC Конспект урока: Декорирование в технике декупаж.
Конспект урока: Декорирование в технике декупаж. Православная икона
Православная икона Внедрение автомобилей в жизнь людей
Внедрение автомобилей в жизнь людей Общественный Фонд Поддержки Образования, для собрания 05.02.20г
Общественный Фонд Поддержки Образования, для собрания 05.02.20г Определение сепсиса
Определение сепсиса Основы теории государства и права (введение в Правоведение)
Основы теории государства и права (введение в Правоведение) Что такое туберкулез?
Что такое туберкулез? Тайны шипучей воды
Тайны шипучей воды