Современная модель строения атома. Периодическая система и Периодический закон Д.И. Менделеева презентация
Содержание
- 2. Лекция 1. Современная модель строения атома. Периодическая система и Периодический закон Д.И. Менделеева Тема 1. Строение
- 3. Основные элементы его теории строения атома Все тела состоят из атомов, которые неделимы и имеют неизменную
- 4. Сторонником атомизма был Платон, который считал, что атомы имеют форму идеальных Платоновских тел (правильных многогранников). Одним
- 5. Сущность строения атома доказана фундаментальными открытиями, сделанными в конце XIX и начале XX в Какие же
- 6. Первое открытие основывалось на изучении лучей, испускаемых отрицательно заряженным электродом – катодом, и потому получивших название
- 7. В 1895 г. исследования Ж. Перрена (1870–1942) показали, что вызывающие свечение «катодные лучи» представляют собой отрицательно
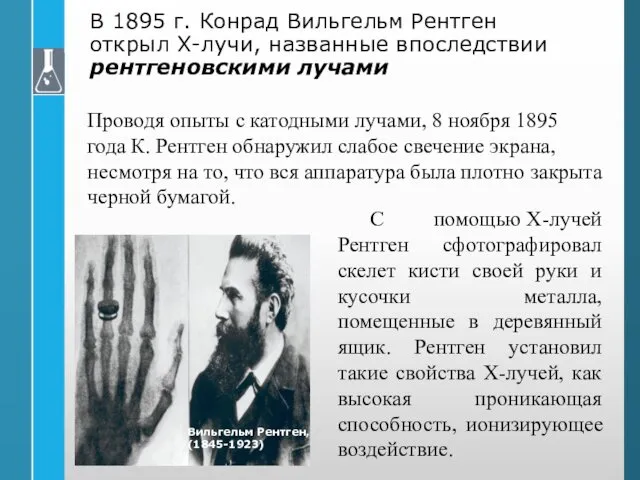
- 8. В 1895 г. Конрад Вильгельм Рентген открыл X-лучи, названные впоследствии рентгеновскими лучами Проводя опыты с катодными
- 9. В 1896 г. Антуан Анри Беккерель показал, что соль урана самопроизвольно испускает невидимое глазу излучение, подобное
- 10. В последующие несколько лет исследования радиоактивности продолжили Эрнест Резерфорд и Фредерик Содди, установившие природу альфа-лучей, представляющих
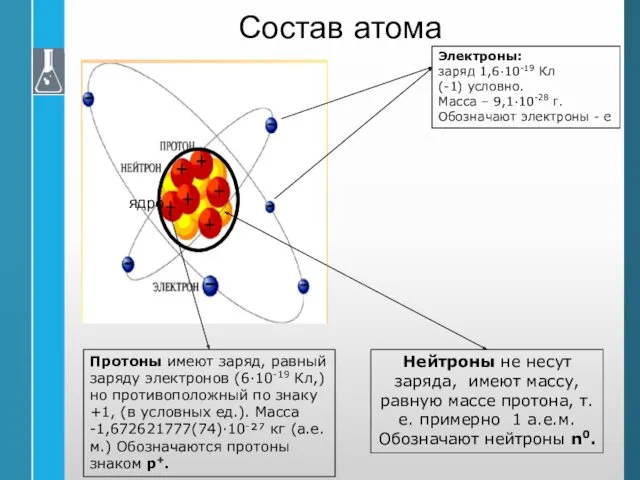
- 11. Состав атома Электроны: заряд 1,6·10-19 Кл (-1) условно. Масса – 9,1·10-28 г. Обозначают электроны - е
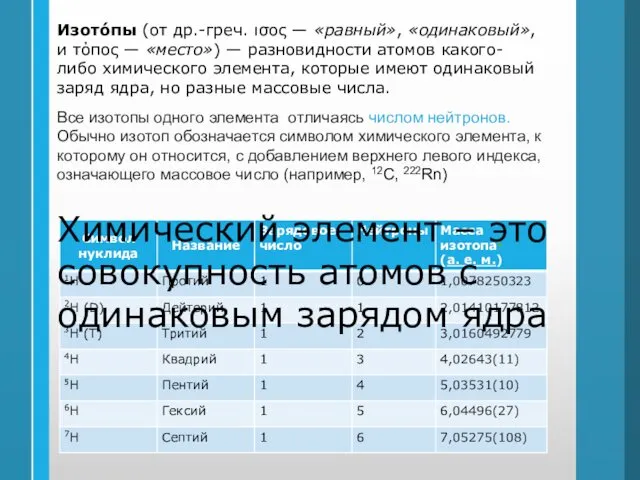
- 12. Изото́пы (от др.-греч. ισος — «равный», «одинаковый», и τόπος — «место») — разновидности атомов какого-либо химического
- 13. В химии часто используют термин нуклид, обозначающий атом с определенным массовым числом А, равным сумме числа
- 14. В Периодической таблице указаны средние атомные массы химического элемента с учетом его изотопного состава, например, атомная
- 15. Модели атома
- 16. в 1904 г Ханатаро Нагаока 1902 году Ульям Томсон В 1903 г. Филипп фон Ленард 1901
- 17. В 1904 г. Томсон Д.Д. развил идею У. Томсона - модель атома представляла собой равномерно заряженную
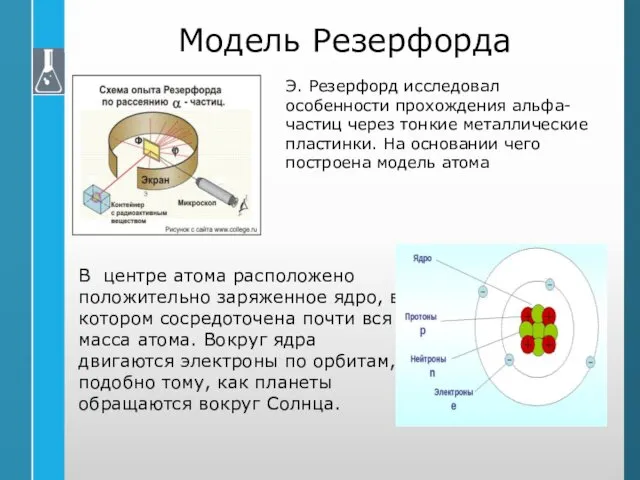
- 18. Модель Резерфорда Э. Резерфорд исследовал особенности прохождения альфа-частиц через тонкие металлические пластинки. На основании чего построена
- 19. Постулаты Бора каждый электрон в атоме может совершать устойчивое движение без излучения энергии, каждый электрон в
- 20. Бор предположил, что энергия электрона в атоме принимает не любые, а лишь строго фиксированные значения. Эти
- 21. В1925–1926гг. Началась эра волновой механики, составившей основу квантово-механической теории атома. В 1925 году, когда Луи-Виктор-Пьер-Раймон де
- 22. В 1927 г. Вернер Карл Гейзенберг сформулировал принцип, ограничивающий эксперименты по изучению отдельных событий микромира. Согласно
- 23. Итак, рождение квантово-механической модели обусловлено тремя особенностями микромира и происходящих в нем процессов: -квантование энергии (энергия
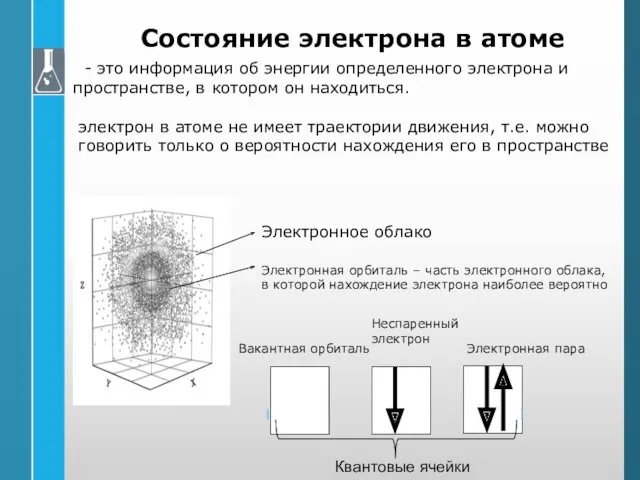
- 24. Состояние электрона в атоме - это информация об энергии определенного электрона и пространстве, в котором он
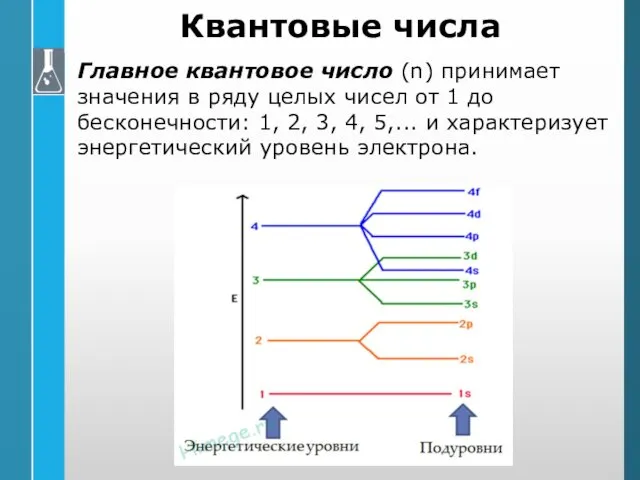
- 25. Квантовые числа Главное квантовое число (n) принимает значения в ряду целых чисел от 1 до бесконечности:
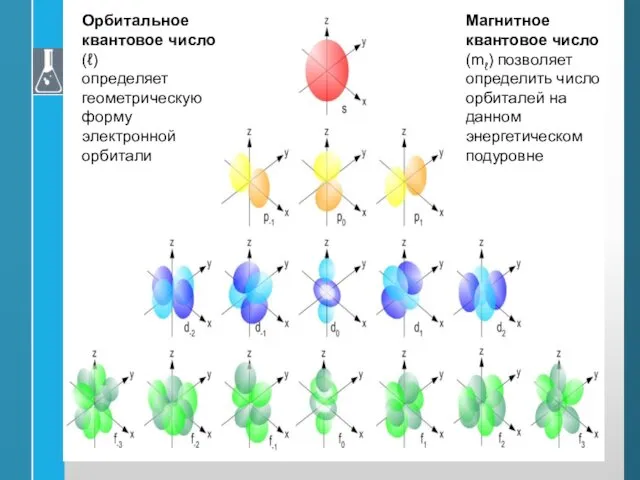
- 26. Орбитальное квантовое число (ℓ) определяет геометрическую форму электронной орбитали Магнитное квантовое число (mℓ) позволяет определить число
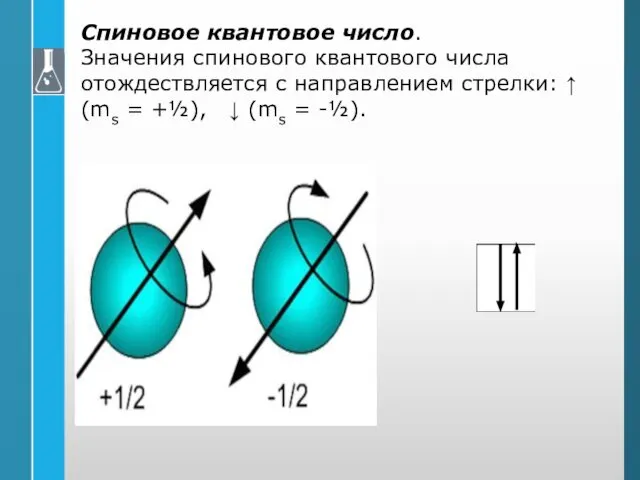
- 27. Спиновое квантовое число. Значения спинового квантового числа отождествляется с направлением стрелки: ↑ (ms = +½), ↓
- 28. 1) При составлении электронных формул следует производить заполнение энергетических подуровней в порядке роста их энергии, низшие
- 29. Правило Хунда Абсолютное значение суммарного спинового числа электронов данного энергетического подуровня должно быть максимальным. Фридрих Хунд,
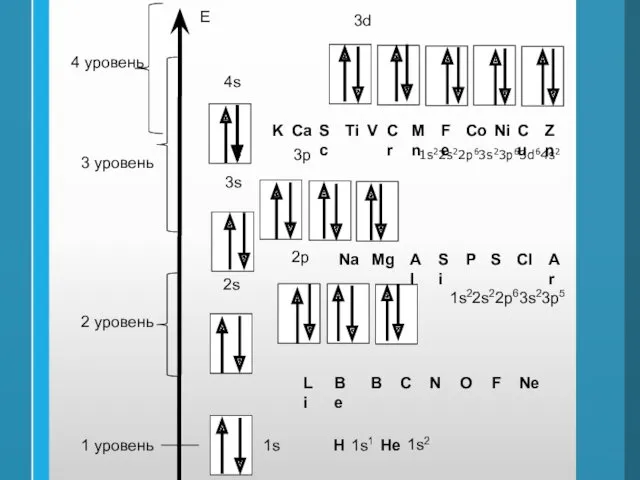
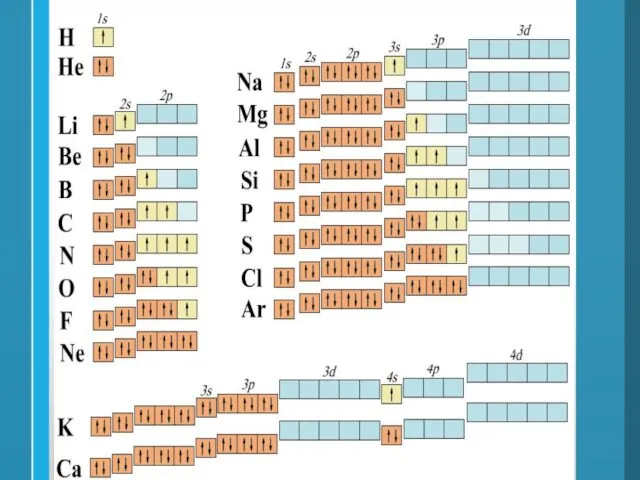
- 30. Е 1 уровень 1s 2 уровень 2s 2р 3s 3р 3d 4s H He 3 уровень
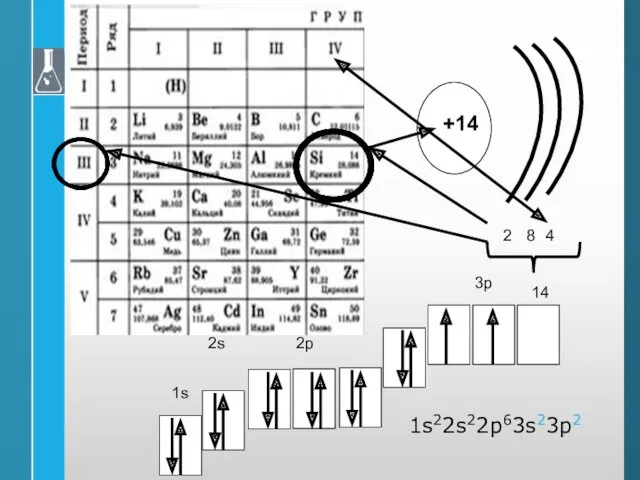
- 32. Периодическая система и строение атома
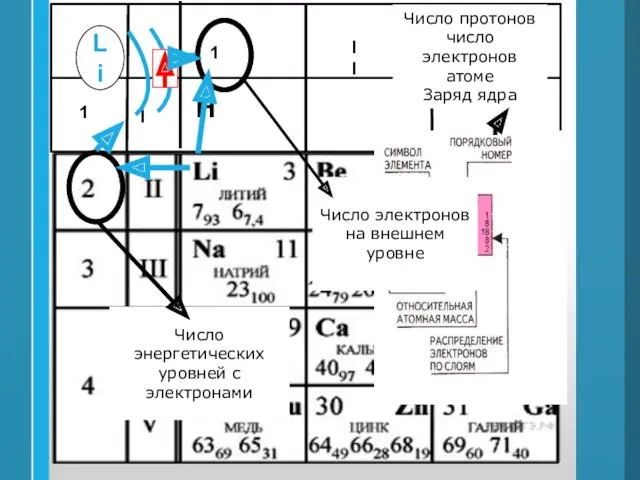
- 33. Число протонов число электронов атоме Заряд ядра Число энергетических уровней с электронами Li Число электронов на
- 34. 8 4 14 2 1s22s22p63s23p2
- 35. Свойства элементов, а также свойства их соединений, находятся в периодической зависимости от зарядов атомных ядер Периодический
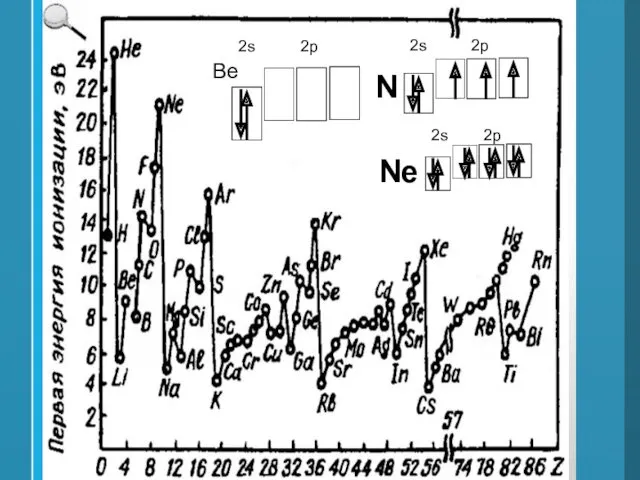
- 36. Свойства атомов 1) Радиус атома 2) Энергия ионизации (I) – это энергия, необходимая для отрыва электрона
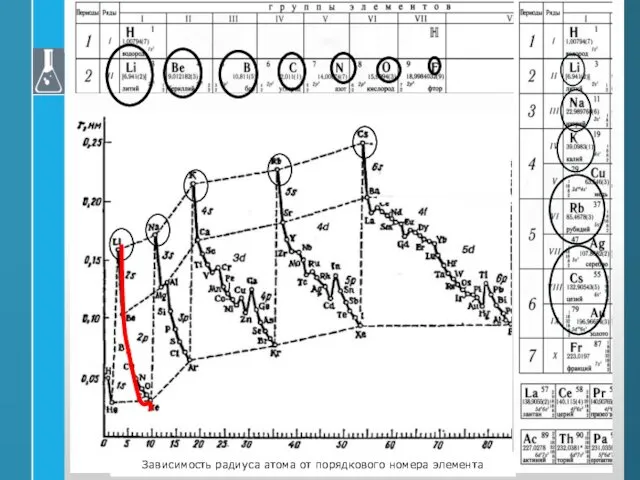
- 37. Зависимость радиуса атома от порядкового номера элемента
- 38. Ве 2s 2p N 2s 2p Ne
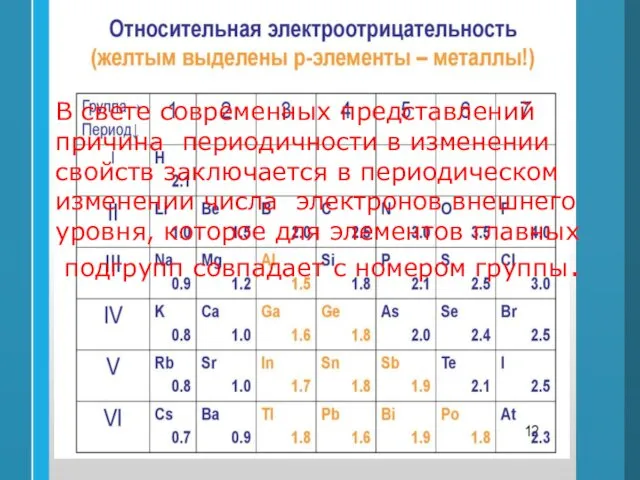
- 39. В свете современных представлений причина периодичности в изменении свойств заключается в периодическом изменении числа электронов внешнего
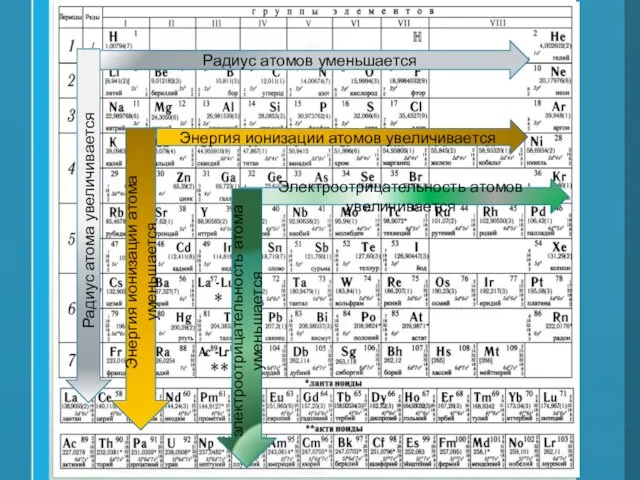
- 40. Радиус атомов уменьшается Радиус атома увеличивается Энергия ионизации атомов увеличивается Энергия ионизации атома уменьшается Электроотрицательность атомов
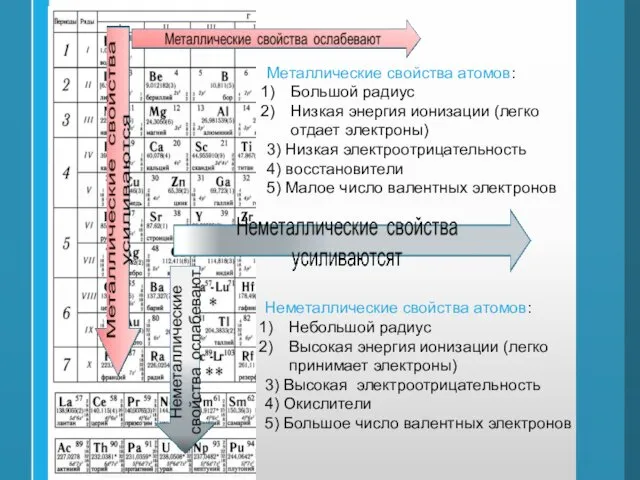
- 41. Металлические свойства атомов: Большой радиус Низкая энергия ионизации (легко отдает электроны) 3) Низкая электроотрицательность 4) восстановители
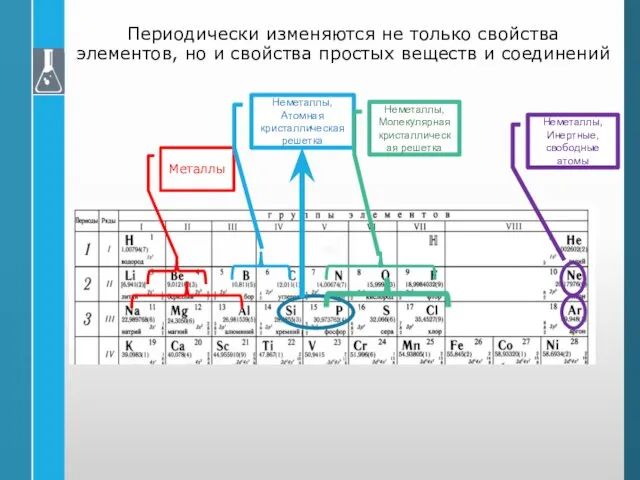
- 42. Периодически изменяются не только свойства элементов, но и свойства простых веществ и соединений Металлы Неметаллы, Атомная
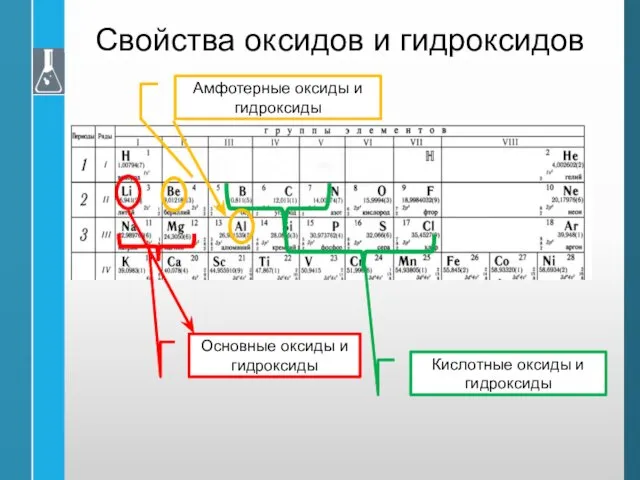
- 43. Свойства оксидов и гидроксидов Основные оксиды и гидроксиды Кислотные оксиды и гидроксиды Амфотерные оксиды и гидроксиды
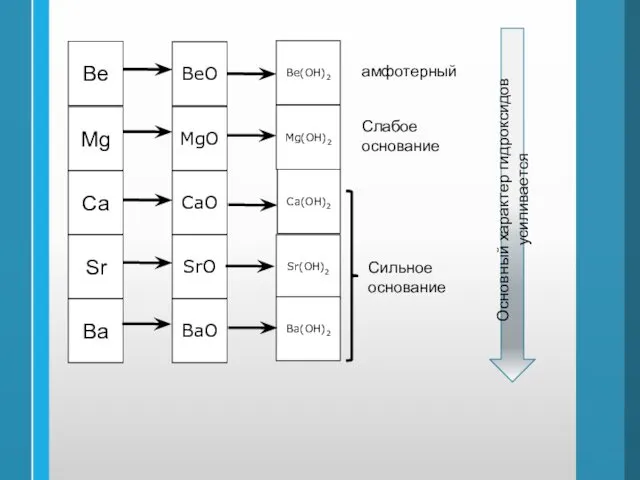
- 44. Ве Mg Ca Sr Вa ВеО Ве(ОН)2 MgО Mg(ОН)2 CaО Ca(ОН)2 SrО Sr(ОН)2 ВaО Вa(ОН)2 амфотерный
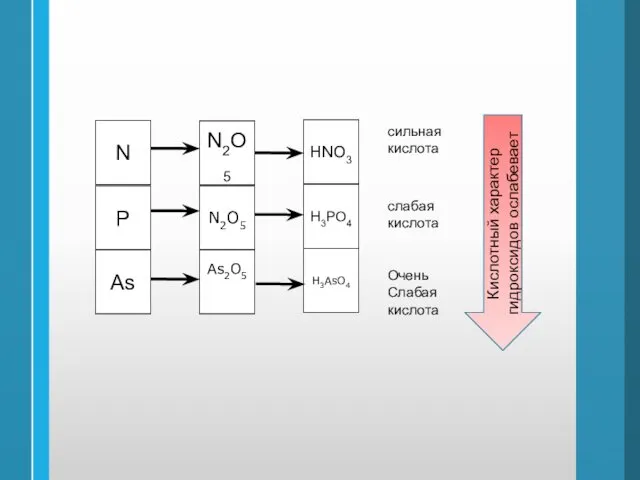
- 45. N P As N2О5 HNO3 N2О5 H3PO4 As2О5 H3AsO4 Очень Слабая кислота слабая кислота сильная кислота
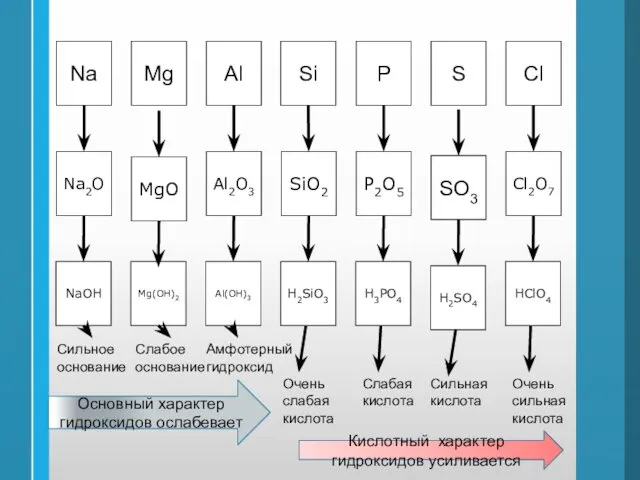
- 46. Mg Al Si P Na S Cl MgO Al2O3 SiO2 P2O5 Na2O SO3 Cl2O7 Mg(OH)2 Al(OH)3
- 47. Выводы о взаимосвязи строения атомов и свойств химических элементов, а также причины периодического изменения их свойств,
- 49. Скачать презентацию
























 Компетенция личностного самосовершенствования
Компетенция личностного самосовершенствования Разработка ресурсосберегающего способа производства топливно-плавильных материалов на основе техногенного сырья (Н3)
Разработка ресурсосберегающего способа производства топливно-плавильных материалов на основе техногенного сырья (Н3) Изготовление декоративного изделия 3D ручкой like
Изготовление декоративного изделия 3D ручкой like Готовая преза с триггерами
Готовая преза с триггерами урок по теме Карбоновые кислоты
урок по теме Карбоновые кислоты Операции Банка России на финансовом рынке. Лекция №4
Операции Банка России на финансовом рынке. Лекция №4 Общая краниология. Общие сведения о черепе
Общая краниология. Общие сведения о черепе Социальная психология личности
Социальная психология личности Роль физической культуры в сохранении здоровья
Роль физической культуры в сохранении здоровья Речь монологическая и диалогическая
Речь монологическая и диалогическая Холокост в литературе. То что забыть нельзя
Холокост в литературе. То что забыть нельзя Земля – уникальная планета (Урок-презентация).
Земля – уникальная планета (Урок-презентация). Мишка. Найди 3 отличия
Мишка. Найди 3 отличия Термодинамические процессы идеальных газов
Термодинамические процессы идеальных газов We're having a great time
We're having a great time Цветотерапия Попугаи
Цветотерапия Попугаи Фестиваль гражданского общества Добрые люди
Фестиваль гражданского общества Добрые люди ПрезентацияХлеб всему голова
ПрезентацияХлеб всему голова Родительское собрание для 1 класса.
Родительское собрание для 1 класса. Ауруханадан тыс пневманиямен ауыратын науқастарды емдеу кезіндегі пенициллин мен цефтриаксонның салыстырмалы
Ауруханадан тыс пневманиямен ауыратын науқастарды емдеу кезіндегі пенициллин мен цефтриаксонның салыстырмалы Обществознание и общественные науки
Обществознание и общественные науки Полиомиелит. Мероприятия в отношении больных полиомиелитом, острыми вялыми параличами
Полиомиелит. Мероприятия в отношении больных полиомиелитом, острыми вялыми параличами Угол. Измерение углов
Угол. Измерение углов Пищевая и легкая промышленность
Пищевая и легкая промышленность Настройка компьютера. Компьютерный вирус
Настройка компьютера. Компьютерный вирус Призентация творческого проекта Мягкая игрушка
Призентация творческого проекта Мягкая игрушка ОГАС 2.0. Программно-техническое решение системы (часть 2)
ОГАС 2.0. Программно-техническое решение системы (часть 2) Формирование стратегии и школы стратегического управления
Формирование стратегии и школы стратегического управления