Слайд 2

Тема урока: Степень окисления. Бинарные соединения
Цели урока:
Познакомится с понятиями –степень окисления
и бинарные соединения
Научится определять степень окисления по формуле и индексы в формуле по степени окисления
Развивать логическое мышление
Слайд 3
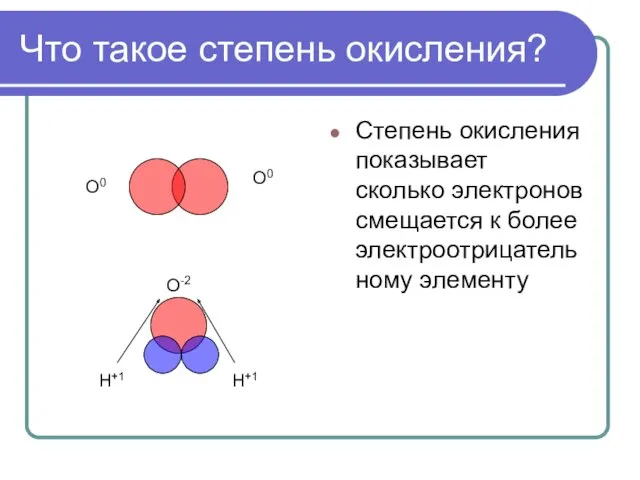
Что такое степень окисления?
Степень окисления показывает сколько электронов смещается к более
электроотрицательному элементу
Слайд 4

Запомним , в соединениях
1. У АТОМОВ В СОСТАВЕ ПРОСТЫХ ВЕЩЕСТВ СТЕПЕНЬ
ОКИСЛЕНИЯ РАВНА 0 –Cl 20,N20
2. СТЕПЕНЬ ОКИСЛЕНИЯ металлов главных подгрупп равна номеру группы- Na+1Cl, Ca+2Cl2, Al+3Cl3.
3. СТЕПЕНЬ ОКИСЛЕНИЯ ФТОРА ВСЕГДА РАВНА -1, А КИСЛОРОДА -2. NaF-1, CaO-2.
4. СТЕПЕНЬ ОКИСЛЕНИЯ ВОДОРОДА С НЕМЕТАЛЛАМИ РАВНА +1, С МЕТАЛЛАМИ -1. H+1Cl, KH-1
Слайд 5

АЛГОРИТМ СОСТАВЛЕНИЯ ФОРМУЛ БИНАРНЫХ СОЕДИНЕНИЙ
1. ОПРЕДЕЛИТЕ БОЛЕЕ ЭЛЕКТРО ОТРИЦАТЕЛЬНЫЙ ЭЛЕМЕНТ. ОН
ПИШЕТСЯ В ФОРМУЛЕ СПРАВА
2. НАД БОЛЕЕ ЭЛЕКТРООТРИЦАТЕЛЬНЫМ ЭЛЕМЕНТОМ СТАВИТСЯ ЕГО СТЕПЕНЬ ОКИСЛЕНИЯ КОТОРАЯ РАВНА:
(№ ГРУППЫ) – 8.
3. НАД МЕНЕЕ ЭЛЕКТРООТРИЦАТЕЛЬНЫМ ЭЛЕМЕНТОМ СТАВИТСЯ ЕГО СТЕПЕНЬ ОКИСЛЕНИЯ КОТОРАЯ РАВНА:
№ ГРУППЫ.
4. МОДУЛИ СТЕПЕНЕЙ ОКИСЛЕНИЯ СНОСЯТСЯ КРЕСТ НА КРЕСТ.
5. ПОЛУЧЕННЫЕ ИНДЕКСЫ СОКРАЩАЮТСЯ
Слайд 6

Закрепление материала
СОСТАВТЕ ФОРМУЛЫ БИНАРНЫХ СОЕДИНЕНИЙ:
C c N, P c
Na, Br c H, Mg c S.
Слайд 7

АЛГОРИТМ ОПРЕДЕЛЕНИЯ СТЕПЕНИ ОКИСЛЕНИЯ ЭЛЕМЕНТОВ В БИНАРНЫХ СОЕДИНЕНИЯХ
1. НАД БОЛЕЕ ЭЛЕКТРООТРИЦАТЕЛЬНЫМ
ЭЛЕМЕНТОМ СТАВИТСЯ ЕГО СТЕПЕНЬ ОКИСЛЕНИЯ КОТОРАЯ РАВНА:
(№ ГРУППЫ) – 8.
2. УМНОЖИТЬ СТЕПЕНЬ ОКИСЛЕНИЯ НА ИНДЕКС КОТОРЫЙ СТОИТ У ЭТОГО ЭЛЕМЕНТА
3. ТАКОЕ ЖЕ ЧИСЛО СО ЗНАКОМ (+)ПОДПИСАТЬ ПОД ДРУГИМ ЭЛЕМЕНТОМ.
4. РАЗДЕЛИТЬ ЧИСЛО НА ИНДЕКС МЕНЕЕ ЭЛЕКТРООТРИЦАТЕЛЬНОГО ЭЛЕМЕНТА
Слайд 8
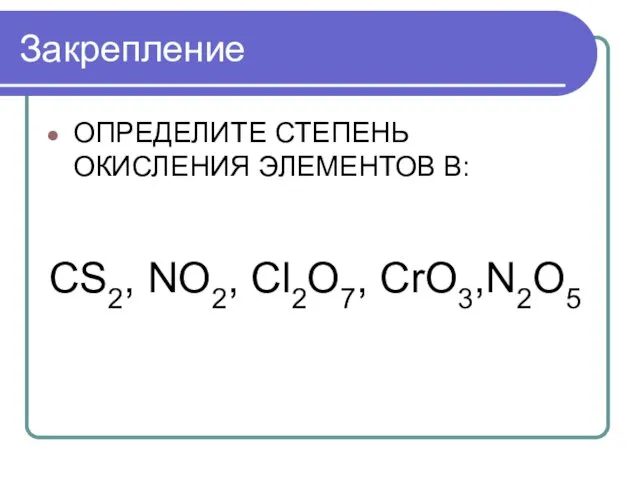
Закрепление
ОПРЕДЕЛИТЕ СТЕПЕНЬ ОКИСЛЕНИЯ ЭЛЕМЕНТОВ В:
CS2, NO2, Cl2O7, CrO3,N2O5
Слайд 9

НОМЕНКЛАТУРА бинарных соединений
ТРИВИАЛЬНАЯ – ИСТОРИЧЕСКИ СЛОЖИВШИЕСЯ НАЗВАНИЯ
НАПРИМЕР СО- УГАРНЫЙ ГАЗ, СО2-
УГЛЕКИСЛЫЙ ГАЗ.
СИСТЕМАТИЧЕСКАЯ- МЕЖДУНАРОДНАЯ, ОТРАЖАЮЩАЯ СОСТАВ ВЕЩЕСТВА
НАПРИМЕР СО- ОКСИД УГЛЕРОДА (II), СО2- ОКСИД УГЛЕРОДА(IV).
Слайд 10

КАК НАЗВАТЬ БИНАРНОЕ СОЕДИНЕНИЕ?
1. ОПРЕДЕЛИТЬ БОЛЕЕ ЭЛЕКТРООТРИЦАТЕЛЬНЫЙ ЭЛЕМЕНТ.
2. ВЗЯТЬ ЕГО ЛАТИНСКИЙ
КОРЕНЬ И ДОБАВИТЬ СУФФИКС- ИД .
3. НАЗВАТЬ В РОДИТЕЛЬНОМ ПАДЕЖЕ РУССКОЕ НАЗВАНИЕ МЕНЕЕ ЭЛЕКТРООТРИЦАТЕЛЬНОГО ЭЛЕМЕНТА.
4.ЕСЛИ У МЕНЕЕ ЭЛЕКТРООТРИЦАТЕЛЬНОГО ЭЛЕМЕНТА ПЕРЕМЕННАЯ СТЕПЕНЬ ОКИСЛЕНИЯ ТО УКАЗЫВАЕТСЯ ЕЕ ЗНАЧЕНИЕ, РИМСКОЙ ЦИФРОЙ, ВКОНЦЕ НАЗВАНИЯ.
Слайд 11

НА ПРИМЕР:
CO2 - оксид углерода(IV)
Mg2C - карбид магния
Li3N - нитрид лития
FeS
- сульфид железа(II)
Слайд 12

ЗАКРЕПЛЕНИЕ
ДАЙТЕ НАЗВАНИЯ И ОПРЕДЕЛИТЕ СТЕПЕНЬ ОКИСЛЕНИЯ ЭЛЕМЕНТОВ В СЛЕДУЮЩИХ ВЕЩЕСТВАХ:
CO2, Na3N,
N2O,
H3P, P2O5, N2O3
Слайд 13

Самопроверка
CO2 - оксид углерода (IV)
Na3N - нитрид натрия
N2O - оксид
азота(I)
H3P - фосфид водорода
P2O5 - оксид фосфора
N2O3 - оксид азота(III)












 Сети электросвязи
Сети электросвязи Становление и развитие реализма как метода и направления. Теоретические споры о реализме
Становление и развитие реализма как метода и направления. Теоретические споры о реализме Театр в Петербурге в 18 веке
Театр в Петербурге в 18 веке Цифровые измерительные приборы (ЦИП)
Цифровые измерительные приборы (ЦИП) УРОК ЗАКРЕПЛЕНИЯ И ОБОБЩЕНИЯ ЗНАНИЙ ПО ТЕМЕ: III-I группы главные подгруппы
УРОК ЗАКРЕПЛЕНИЯ И ОБОБЩЕНИЯ ЗНАНИЙ ПО ТЕМЕ: III-I группы главные подгруппы Презентация по котельным установкам. Типовые компоновки котельных на газомазутном топливе
Презентация по котельным установкам. Типовые компоновки котельных на газомазутном топливе КЛАССИФИКАЦИЯ НЕОРГАНИЧЕСКИХ ВЕЩЕСТВ
КЛАССИФИКАЦИЯ НЕОРГАНИЧЕСКИХ ВЕЩЕСТВ Защита информации. Компьютерные вирусы и антивирусные программы
Защита информации. Компьютерные вирусы и антивирусные программы И чувства добрые я лирой пробуждал...
И чувства добрые я лирой пробуждал... Сәулелік зақымдардың қалыптасуы. Организм деңгейінде иондаушы радиацияның әсері. Адамның сәуле ауруы
Сәулелік зақымдардың қалыптасуы. Организм деңгейінде иондаушы радиацияның әсері. Адамның сәуле ауруы Индивидуальный стиль учебной деятельности ученика, как фактор его учебного успеха
Индивидуальный стиль учебной деятельности ученика, как фактор его учебного успеха Квиллинг для начинающих
Квиллинг для начинающих Создание центра сохранения и реабилитации китообразных Черного моря
Создание центра сохранения и реабилитации китообразных Черного моря Моей любимой подруге
Моей любимой подруге Моделирование как средство развития связной речи
Моделирование как средство развития связной речи Мастер – класс Широкая Масленица!. Интерьерный сувенир
Мастер – класс Широкая Масленица!. Интерьерный сувенир Riddles
Riddles К.Д.Ушинский – основоположник русской педагогической науки
К.Д.Ушинский – основоположник русской педагогической науки Эволюция человеческого дома
Эволюция человеческого дома Старинные единицы объёма
Старинные единицы объёма Игра Звуковые человечки Дифференциация звуков З-Ж
Игра Звуковые человечки Дифференциация звуков З-Ж Что такое этикет.
Что такое этикет. Азот
Азот Система отношений компании со стейкхолдерами
Система отношений компании со стейкхолдерами Бессер-Строй. Строительство коттеджей в Уфе и Республике Башкортостан
Бессер-Строй. Строительство коттеджей в Уфе и Республике Башкортостан Механизмы детоксикации
Механизмы детоксикации pril
pril Проектирование системы электроснабжения ТСН Рябина г. Сосновый Бор
Проектирование системы электроснабжения ТСН Рябина г. Сосновый Бор