Слайд 2

Основные понятия.
Атом – электронейтральная микросистема, состоящая из положительно заряженного ядра и
отрицательно заряженных электронов (размер атома 10-8).
Слайд 3

Протон – это стабильная элементарная частица, входящая в состав всех ядер
атомов,
имеющая массу=1,67310-27 кг и
заряд = +1.
Слайд 4

Нейтрон - это электрически нейтральная элементарная частица, входящая в состав ядра
и имеющая массу = 1, 67510-27 кг
Слайд 5

Электрон – это элементарная частица, материальный носитель наименьшей массы (0,9110-27 г)
и наименьшего электрического заряда в природе (=-1)
Слайд 6

А – массовое число атома.
А = Z+N
Химический элемент – это вид
атомов с одинаковым зарядом ядра.
Изотопы – атомы одного и того же химического элемента, имеющие одинаковое число протонов, но различающиеся массовым числом, за счет разного числа нейтронов в ядре.
Слайд 7

Атомная орбиталь (АО) – область околоядерного пространства, в которой наиболее вероятно
(90%) нахождение электрона.
Слайд 8

Квантовые числа:
Главное (n)
Орбитальное (l)
Магнитное (ml)
Спиновое (ms)
Слайд 9

Главное квантовое число (n).
Характеризует запас энергии электрона.
Определяет энергетический уровень
электрона, удаленность уровня
от ядра,
размер электронного облака.
n= 1,2,3… , соответствует номеру
периода в ПСХЭМ.
Слайд 10

Чем больше n, тем электрон дальше от ядра, тем больше запас
его энергии, тем слабее связь с ядром, тем легче удалить электрон из атома.
Энергетический уровень (ЭУ) – совокупность электронных состояний, имеющих одинаковое значение n.
ЭУ обозначается 1,2,3… или соответствующими буквами K, L, M, N, O...
Слайд 11
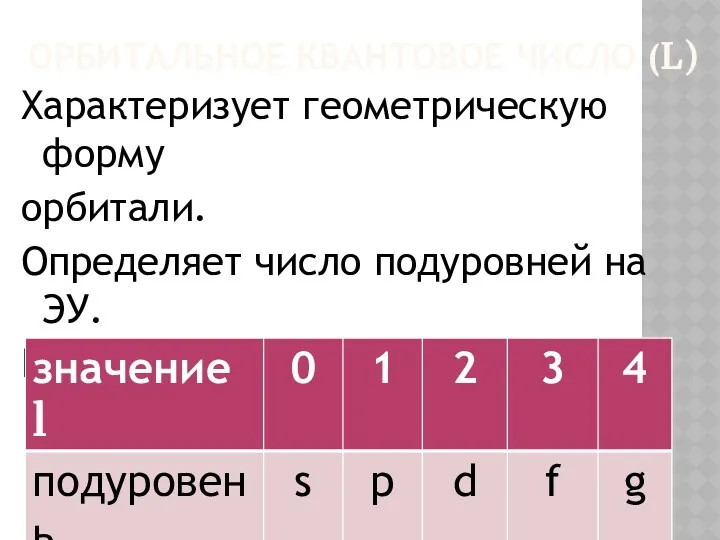
Орбитальное квантовое число (l)
Характеризует геометрическую форму
орбитали.
Определяет число подуровней на ЭУ.
Принимает значения:
от 0 до (n-1).
Слайд 12

При n=1, L=0 (первый ЭУ, один
s-подуровень). Форма орбитали – сферическая.
Слайд 13

При n=2, L=0, 1 (второй ЭУ, два подуровня s и p).
Форма орбитали – гантель.
Слайд 14

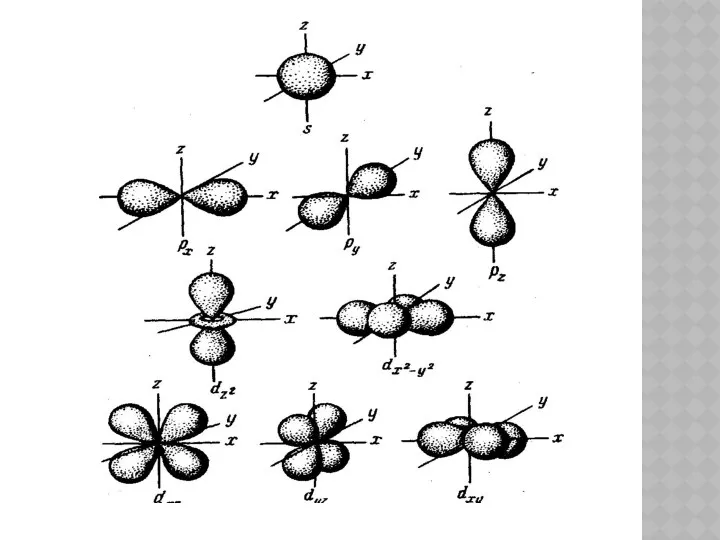
При n=3, L=0,1,2 (третий ЭУ, три подуровня s, p и d).
Форма орбитали сложная.
Возможные форма d-орбиталей:
Слайд 15

Возможные форма f- орбиталей:
Слайд 16

Номер уровня указывает на число подуровней, которыми он располагает.
Энергетический подуровень –
это совокупность электронных состояний, характеризующихся определенным набором квантовых чисел n и l.
Слайд 17

Магнитное квантовое число ml
Характеризует число способов взаимной
ориентации ЭО.
Принимает значения: ml= -l,…0,…+l
Если l=0 (s), то ml =0 (сфера – одна ориентация в
пространстве).
Если l=1 (p), то ml=-1, 0, +1.(три орбитали
гантели, три ориентации p-орбиталей в
пространстве).
Слайд 18
Слайд 19

Общее число орбиталей на энергетическом уровне равно n2.
Число орбиталей на
подуровне равно (2L + 1).
Слайд 20

Спиновое квантовое число ms.
Характеризует собственный момент
импульса электрона, связанный с
вращением
электрона вокруг
собственной оси при его вращении
вокруг ядра.
Принимает значения +1/2 или -1/2
(по часовой стрелке, либо против
часовой стрелки)
Слайд 21
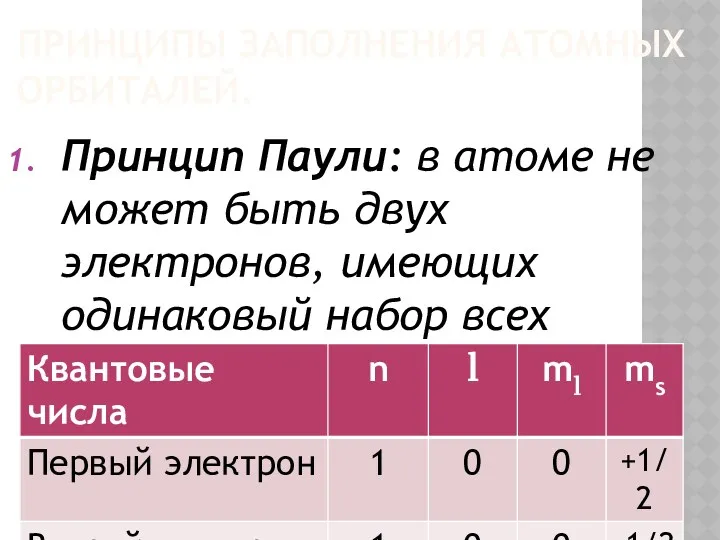
Принципы заполнения атомных орбиталей.
Принцип Паули: в атоме не может быть двух
электронов, имеющих одинаковый набор всех четырех квантовых чисел.
Слайд 22

Каждая орбиталь может вместить только 2 электрона , имеющих противоположно направленные
спины.
Максимальное число электронов на подуровнях:
s2 , p6 , d10, f14
Слайд 23

Максимальное количество
электронов на энергетическом уровне определяется по
формуле:
N = 2n2,
где N –
число электронов,
n – номер энергетического уровня.
Слайд 24

2.Принцип наименьшей энергии.
Основному состоянию атома
соответствует минимальная
суммарная энергия электронов.
Слайд 25

Правило Клечковского.
Увеличение энергии и соответственно
заполнение орбиталей происходит в
порядке возрастания
суммы квантовых
чисел (n+l), а при одинаковых значении
(n+l) в порядке возрастания числа n.
1s,2s,2p,3s,3p,4s,3d,4p,5s,4d,5p,
6s,4f,5d,6р…
Слайд 26

Соответственно правилу Клечковского энергия возрастает в ряду:
1s,2s,2p,3s,3p,4s,3d,4p,5s,4d,5p,
6s,4f,5d,6р…
Слайд 27

3. Правило Гунда (Хунда).
При заполнении электронами орбиталей каждого данного подуровня
число неспаренных электронов на нем должно быть максимальным.
Слайд 28

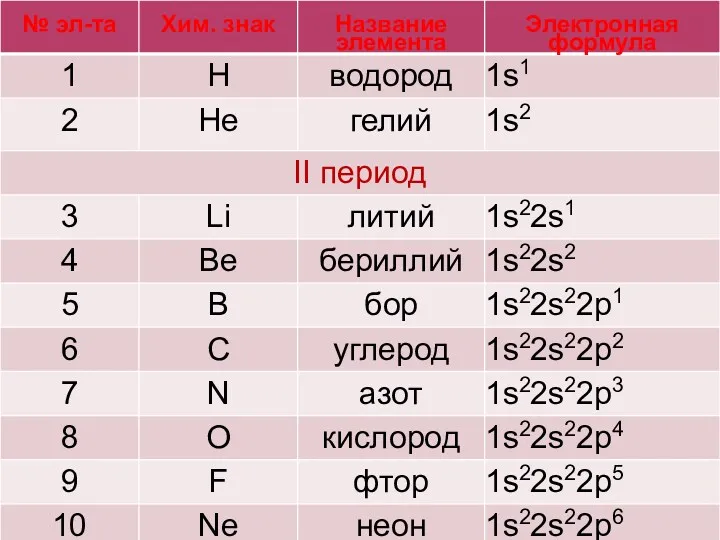
Электронные конфигурации элементов -V периодов.
Слайд 29
Слайд 30
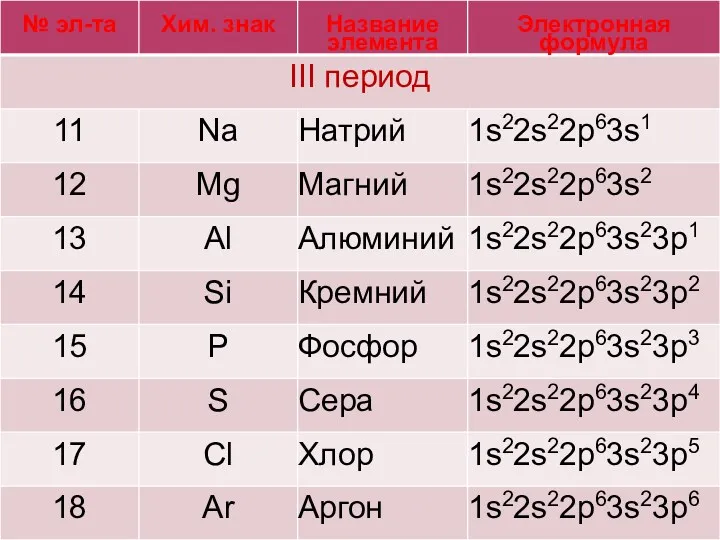
Слайд 31
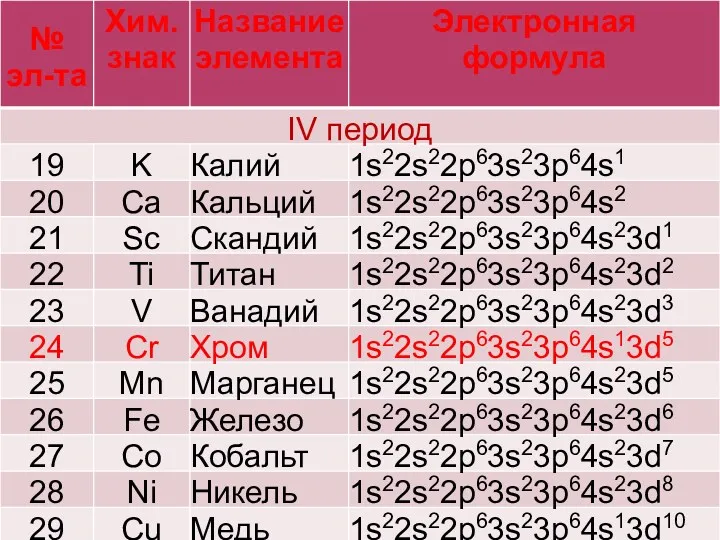
Слайд 32
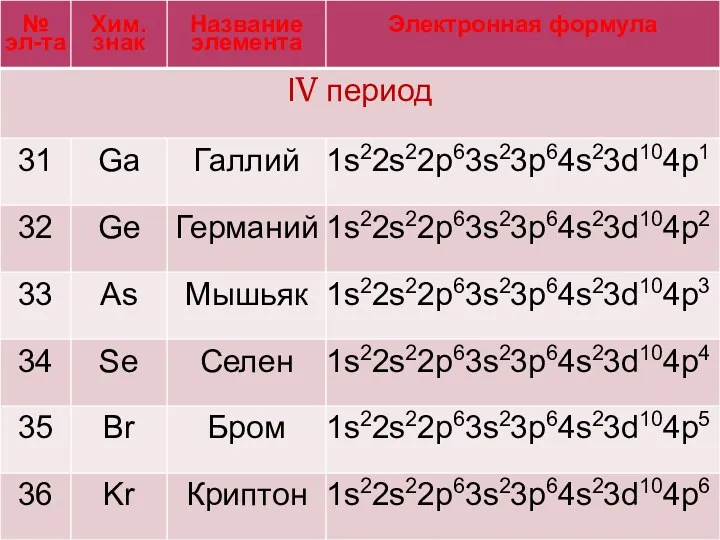
Слайд 33

«провал» или «проскок» электрона
Наибольшая устойчивость у подуровней, заполненных наполовину
или полностью электронами. Конфигурации d5 и d10 устойчивее чем d4 и d9 .
Слайд 34

Элементы с «аномальными» электронными конфигурациями:
Молибден
Рутений
Родий
Палладий
Серебро
Лантан
Платина
Золото
Актиний
Слайд 35

В зависимости от заполняемого в последнюю очередь энергетического подуровня, элементы делятся
на семейства:
s - элементы
p - элементы
d - элементы
f - элементы
Слайд 36

Электронные аналоги – элементы с одинаковым строением внешнего энергетического уровня (например,
элементы группы, гл. подгруппы). Они имеют сходные химические свойства, но различную химическую активность.
Слайд 37

Нормальное и возбужденное состояния атома
При сообщении энергии атом переходит в
возбужденное состояние, характеризующееся перестройкой электронной конфигурации: один из электронов с более низкого по энергии подуровня переходит на другой, энергия которого выше.
Слайд 38

Периодический закон и периодическая система химических элементов Д.И. Менделеева в свете
учения о строении атома.
Слайд 39

Свойства химических элементов, а также формы и свойства образуемых ими соединений,
находятся в периодической зависимости от величины заряда ядер их атомов.
Слайд 40

У элементов периодически повторяются электронные конфигурации атомов и поэтому периодически повторяются
химические свойства, которые определяются электронной конфигурацией атомов.
Слайд 41

Периодически изменяются: атомные радиусы, энергии ионизации и сродства к электрону, электроотрицательности.
Слайд 42

Радиус атома (орбитальный радиус) –теоретически рассчитанное расстояние от центра ядра атома
до максимума электронной плотности внешнего квантового слоя.









































 Студенческий совет экономичесого факультета
Студенческий совет экономичесого факультета Принципы обследования больного в хирургической практике. Современные цифровые диагностические технологии в стоматологии
Принципы обследования больного в хирургической практике. Современные цифровые диагностические технологии в стоматологии Образовательные возможности информационных технологий
Образовательные возможности информационных технологий Пространственные конструкции покрытий зданий
Пространственные конструкции покрытий зданий ПРЕЗЕНТАЦИЯ ЛУКОЙЛ
ПРЕЗЕНТАЦИЯ ЛУКОЙЛ Проект по краеведению Мой отчий край ни в чём не повторим
Проект по краеведению Мой отчий край ни в чём не повторим Детерминированные модели
Детерминированные модели Расчет одиночных трубчатых колодцев (скважин)
Расчет одиночных трубчатых колодцев (скважин) Путешествие по материкам. Евразия
Путешествие по материкам. Евразия Стратегия организации
Стратегия организации презентация Добро пожаловать в интернат
презентация Добро пожаловать в интернат Tehnologii de confecţionare a produselor vestimentare
Tehnologii de confecţionare a produselor vestimentare Строение семян покрытосеменных растений
Строение семян покрытосеменных растений Творческий, информационно – практико-ориентированный проект Прошлое, настоящее, будущее родного края
Творческий, информационно – практико-ориентированный проект Прошлое, настоящее, будущее родного края Погода и климат
Погода и климат Презентация Победапо русскому языку во 2 классе с применением здоровьесберегающих технологий Сочетания ЖИ_ШИ
Презентация Победапо русскому языку во 2 классе с применением здоровьесберегающих технологий Сочетания ЖИ_ШИ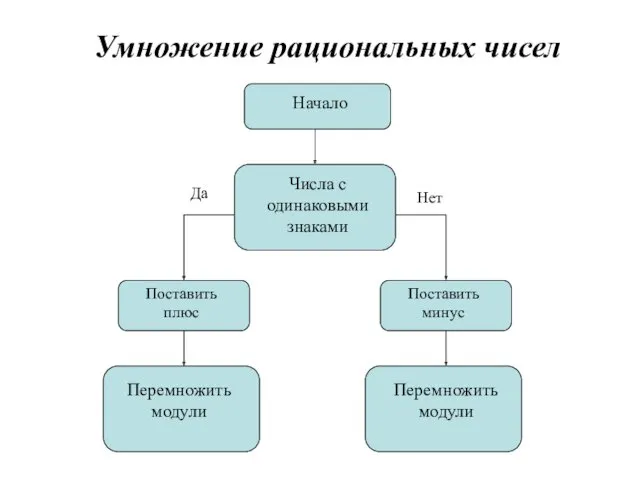 Умножение рациональных чисел
Умножение рациональных чисел ПрезентацияСвященные сооружения
ПрезентацияСвященные сооружения Как человек реагирует на явления в жизни и искусстве
Как человек реагирует на явления в жизни и искусстве Сценарий спектакля Снежная королева
Сценарий спектакля Снежная королева Сказочные лабиринты игр Воскобовича
Сказочные лабиринты игр Воскобовича Технология приготовления и контроль качества блюд из дрожжевого теста. Инвентаризация материально-производственных запасов
Технология приготовления и контроль качества блюд из дрожжевого теста. Инвентаризация материально-производственных запасов Новітній маркетинг в фармації та його основні напрямки
Новітній маркетинг в фармації та його основні напрямки Верхнее строение пути. Устройство железнодорожного пути. Тема 1
Верхнее строение пути. Устройство железнодорожного пути. Тема 1 Города-герои
Города-герои Остров сокровищ
Остров сокровищ Лес - богатство наше
Лес - богатство наше Правила безопасности систем газораспределения и газопотребления. Надзор и обслуживание
Правила безопасности систем газораспределения и газопотребления. Надзор и обслуживание