Содержание
- 2. Теория возникновения электродного потенциала Нернста 1. Физическая или «контактная» теория итальянского физика Вольта (1799 г), согласно
- 3. 2. Химическая теория ЭДС (1857 г. Де-ля-Рив), согласно которой источником электрической энергии являются химические реакции на
- 4. Нернст получил качественную картину возникновения скачка потенциала на границе металл-раствор и вывел количественную зависимость величины этого
- 5. При равновесии = - zFε Отсюда Если С = 1, то Поскольку полагалось, что к растворам
- 6. Теория Нернста имела ряд недостатков: физический смысл стандартного потенциала не ясен, поскольку не ясен смысл электролитической
- 7. Работы Писаржевского и Изгарышева Теория электродного потенциала, учитывающая взаимодействие ионов с растворителем (сольватацию) была развита Писаржевским
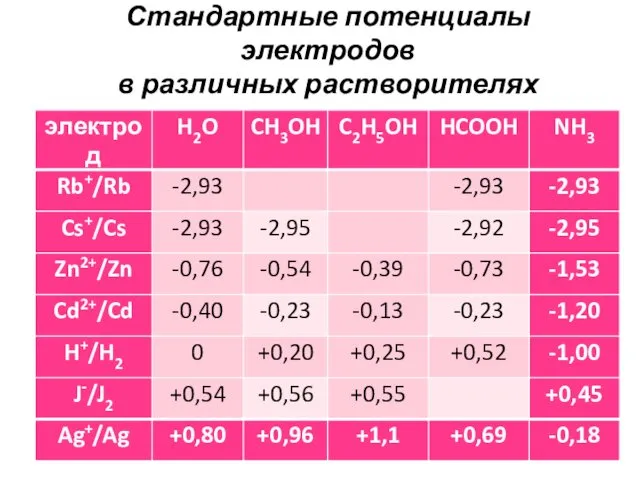
- 8. Стандартные потенциалы электродов в различных растворителях
- 9. Установлено, что изменение электродного потенциала при переходе от одного растворителя к другому тем больше, чем меньше
- 10. Указанные качественные представления Писаржевского о влиянии энергии сольватации на электродный потенциал в 1926-28 гг. были развиты
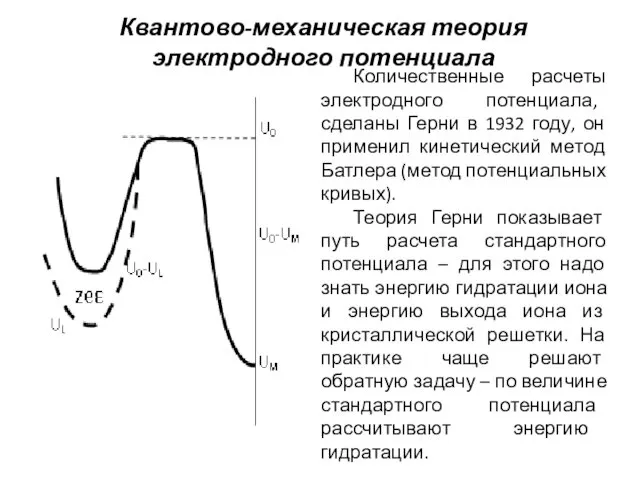
- 11. Квантово-механическая теория электродного потенциала Количественные расчеты электродного потенциала, сделаны Герни в 1932 году, он применил кинетический
- 12. Термодинамический вывод уравнения для обратимой ЭДС и равновесного электродного потенциала 1878 г Гиббс и в 1882
- 13. G = ∑νi μi , где i > 0 для конечных веществ и i ∆G =
- 14. Выразим значение потенциала Е = (*) Если активности всех участников реакции равны 1, то Е =
- 16. Скачать презентацию











 Основы языка ассемблер. Использование массивов
Основы языка ассемблер. Использование массивов Лукойл. Нефтяная компания. Всегда в движении!
Лукойл. Нефтяная компания. Всегда в движении! Введение в послание ап. Павла к Римлянам
Введение в послание ап. Павла к Римлянам Своя игра. Правила дорожные знать каждому положено
Своя игра. Правила дорожные знать каждому положено Тайна имени Софья
Тайна имени Софья Зимнее кружево
Зимнее кружево Тайны природы
Тайны природы Вознаграждение персонала
Вознаграждение персонала Engineering in America
Engineering in America Новогодняя лотерея
Новогодняя лотерея Этносоциальные особенности приграничных субъектов Российской Федерации Центрально-Азиатского направления
Этносоциальные особенности приграничных субъектов Российской Федерации Центрально-Азиатского направления Комплектні трансформаторні підстанції
Комплектні трансформаторні підстанції Образование и просвещение России в XVIII веке
Образование и просвещение России в XVIII веке ФГОС дошкольного образования.
ФГОС дошкольного образования. ДМ Режимы работы СПиР
ДМ Режимы работы СПиР Своя игра
Своя игра Характерные черты русской народной музыки
Характерные черты русской народной музыки Развитие произвольного внимания у детей дошкольного возраста с помощью графических диктантов
Развитие произвольного внимания у детей дошкольного возраста с помощью графических диктантов Объемы. Объем прямоугольного параллелепипеда
Объемы. Объем прямоугольного параллелепипеда Premium Colorful Template
Premium Colorful Template Роль туристских кадров в работе туристского учреждения
Роль туристских кадров в работе туристского учреждения Основы технологии машиностроения
Основы технологии машиностроения Воздушный транспорт
Воздушный транспорт Требования при приемке завершенного ремонта подъездов МКД (для управляющих организаций)
Требования при приемке завершенного ремонта подъездов МКД (для управляющих организаций) Геномные проекты
Геномные проекты Магнит. Магнит өріс бағыты
Магнит. Магнит өріс бағыты Страны Западной Европы
Страны Западной Европы Годівля коней
Годівля коней