Содержание
- 2. Согласно проекту КИМ 2014 года в содержание и структуру ЕГЭ по химии могут быть внесены следующие
- 3. rischat.g@yandex.ru
- 4. Характерные получения и химические свойства углеводородов: алканов, циклоалканов, алкенов, диенов, алкинов, ароматических углеводородов (А13,14,17, В1,6, С3,5)
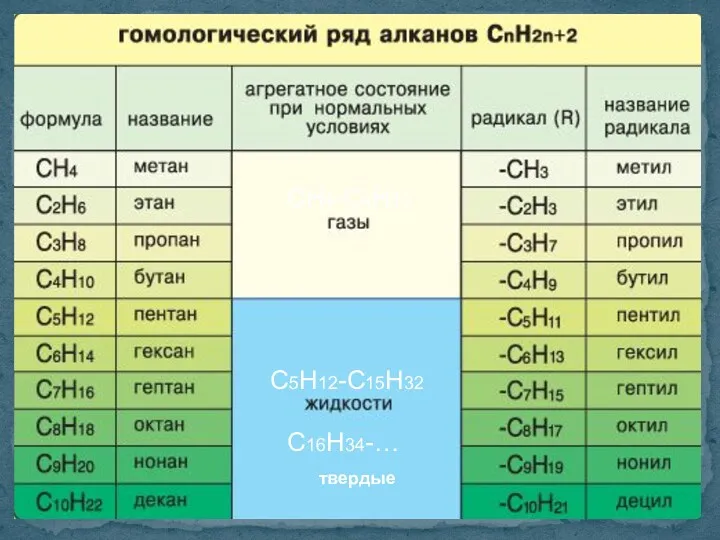
- 5. АЛКАНЫ СnH2n+2 -ан
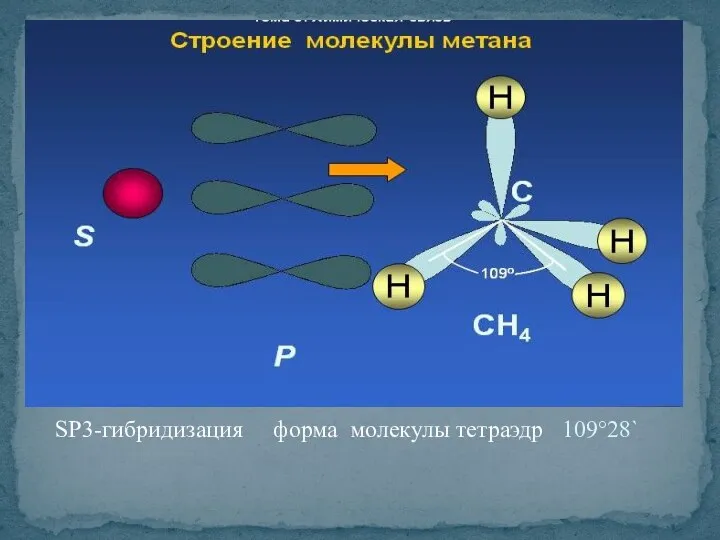
- 6. SP3-гибридизация форма молекулы тетраэдр 109°28`
- 7. СН4-С4Н10 С5Н12-С15Н32 С16Н34-… твердые
- 8. АЛКАНЫ (ПАРАФИНЫ)
- 9. Химические свойства
- 10. Химические свойства
- 11. Химические свойства
- 12. ЦИКЛОАЛКАНЫ CnH2n цикло-
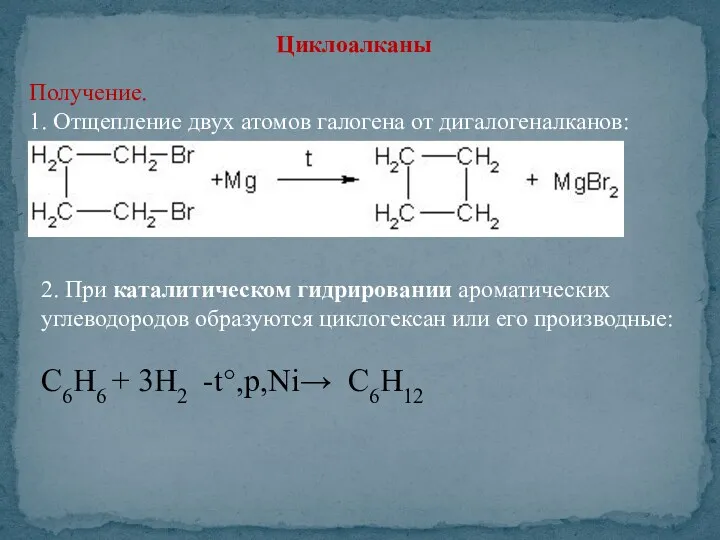
- 13. Циклоалканы Получение. 1. Отщепление двух атомов галогена от дигалогеналканов: 2. При каталитическом гидрировании ароматических углеводородов образуются
- 14. Химические свойства 1) Гидрирование. При каталитическом гидрировании разрываются с образованием алканов. С3Н6+ H2 -120ºC,Ni CH3–CH2–CH3 2)
- 15. 5) Галогенирование: циклопентан реагируют с галогенами на свету, вступая в реакцию замещения С5Н10 + С12-(свет) С5Н10+НС1
- 16. АЛКЕНЫ CnH2n
- 18. Алкены
- 20. Химические свойства
- 23. АЛКАДИЕНЫ CnH2n-2 -диен
- 24. АЛКАДИЕНЫ
- 26. ХИМИЧЕСКИЕ СВОЙСТВА
- 29. АЛКИНЫ CnH2n-2 -ин
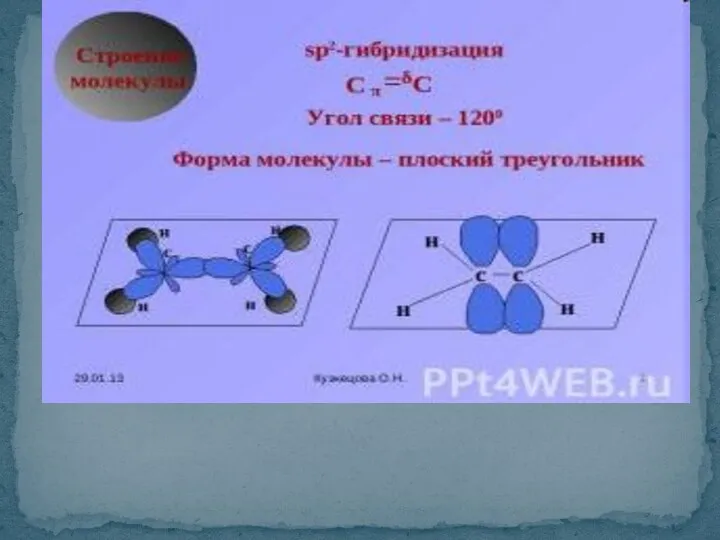
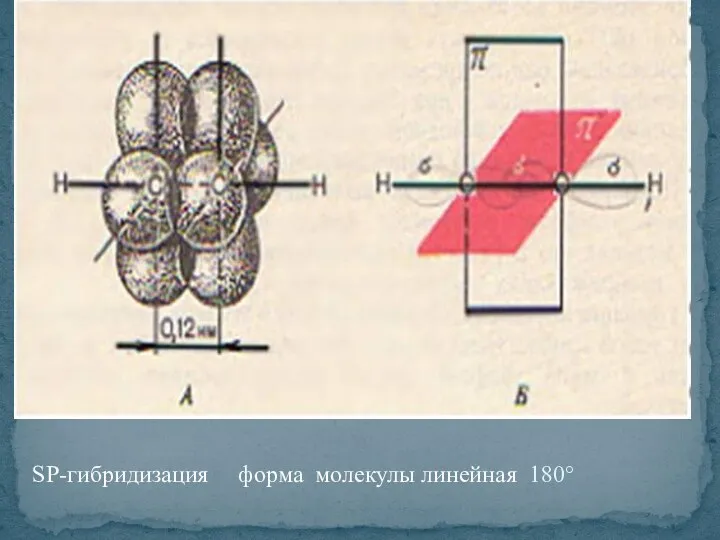
- 30. SP-гибридизация форма молекулы линейная 180°
- 31. АЛКИНЫ
- 33. 1. Реакции присоединения. А. Гидрирование: В присутствии металлических катализаторов (Pt, Ni) алкины присоединяют водород с образованием
- 34. В. Гидрогалогенирование. Присоединение галогеноводородов также идет по электрофильному механизму. Продукты присоединения к несимметричным алкинам определяются правилом
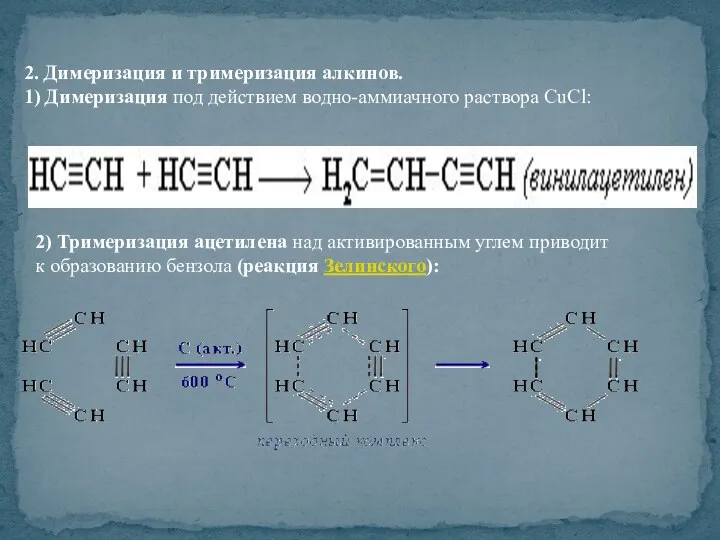
- 35. 2. Димеризация и тримеризация алкинов. 1) Димеризация под действием водно-аммиачного раствора CuCl: 2) Тримеризация ацетилена над
- 36. 3. Кислотные свойства алкинов с концевой тройной связью. Образование солей: концевые атомы водорода у ацетилена и
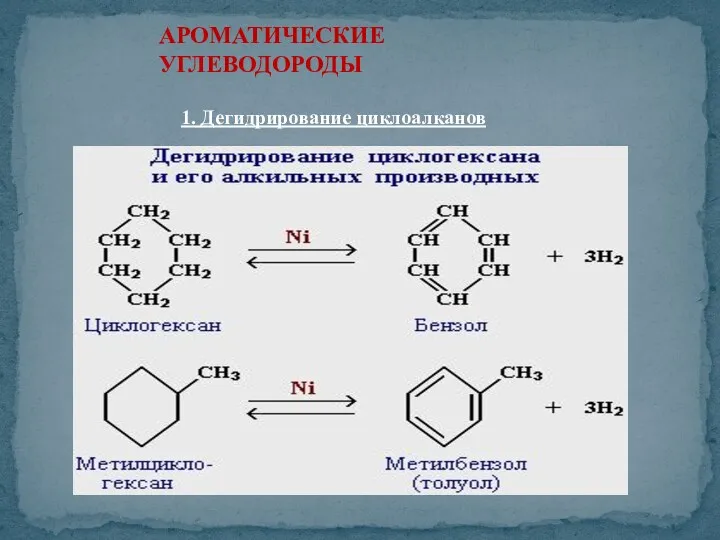
- 37. АРОМАТИЧЕСКИЕ УГЛЕВОДОРОДЫ 1. Дегидрирование циклоалканов
- 38. АРОМАТИЧЕСКИЕ УГЛЕВОДОРОДЫ CnH2n-6
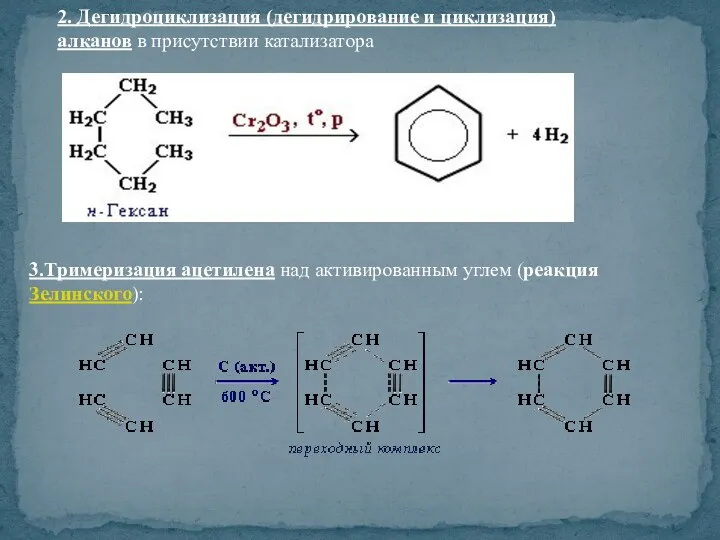
- 39. 2. Дегидроциклизация (дегидрирование и циклизация) алканов в присутствии катализатора 3.Тримеризация ацетилена над активированным углем (реакция Зелинского):
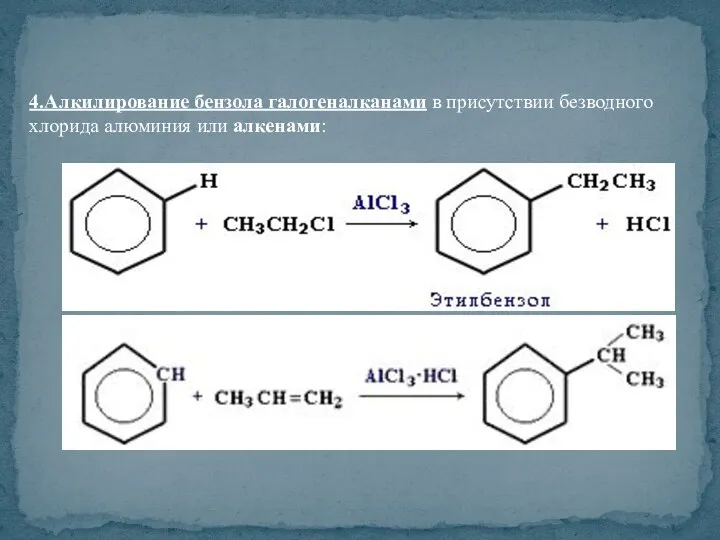
- 40. 4.Алкилирование бензола галогеналканами в присутствии безводного хлорида алюминия или алкенами:
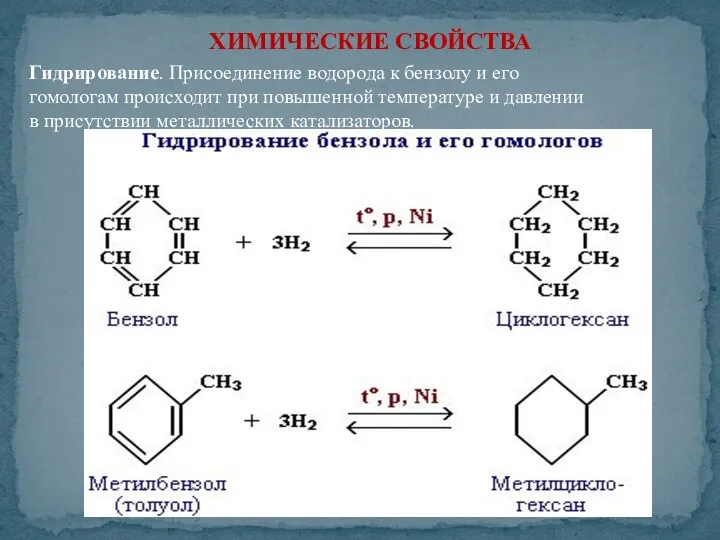
- 41. ХИМИЧЕСКИЕ СВОЙСТВА Гидрирование. Присоединение водорода к бензолу и его гомологам происходит при повышенной температуре и давлении
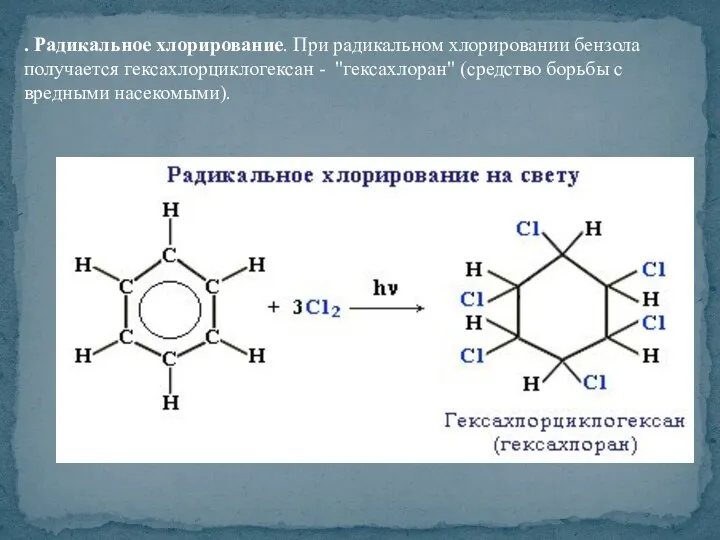
- 42. . Радикальное хлорирование. При радикальном хлорировании бензола получается гексахлорциклогексан - "гексахлоран" (средство борьбы с вредными насекомыми).
- 43. Галогенирование Замещение атома водорода в бензольном кольце на галоген происходит в присутствии катализаторов AlCl3, AlBr3, FeCl3
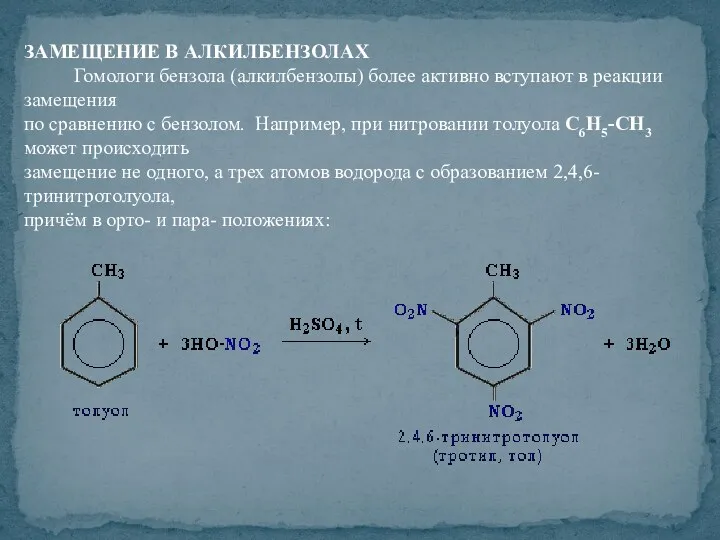
- 44. ЗАМЕЩЕНИЕ В АЛКИЛБЕНЗОЛАХ Гомологи бензола (алкилбензолы) более активно вступают в реакции замещения по сравнению с бензолом.
- 45. А13. Бутен-1 является структурным изомером 1)бутана 3)бутина 2)циклобутана 4) бутадиена
- 46. А17. Бутанол-1 образуется в результате взаимодействия бутана с гидроксидом натрия бутена-1 с водородом бутаналя с водородом
- 47. А14. В соответствии с правилом Марковникова присоединение бромоводорода к 2-метилпропену приводит к образованию 2-метил-1-бромпропена 2-метил-1-бромпропана 2-метил-2-бромпропана
- 48. В1. Установите соответствие между названием соединения и общей формулой гомологического ряда, к которому оно принадлежит. НАЗВАНИЕ
- 49. В6 С этином могут взаимодействовать 1)иодоводород 4) этилацетат 2)метан 5) натрий 3)вода 6) азот Ответ:
- 51. Скачать презентацию




































 Орган слуха, равновесия. Тестирование
Орган слуха, равновесия. Тестирование O’zbekistonda neft va gaz sanoatining tarixi, rivojlanish bosqichlar va istiqbollari
O’zbekistonda neft va gaz sanoatining tarixi, rivojlanish bosqichlar va istiqbollari В память о Великой войне и ее героях ст. Крымской
В память о Великой войне и ее героях ст. Крымской Занимательная атмосфера
Занимательная атмосфера Дигибридное скрещивание
Дигибридное скрещивание Методика расследования изнасилований
Методика расследования изнасилований Analisis of the natural moving the population
Analisis of the natural moving the population Устройство сверлильного станка
Устройство сверлильного станка Маркетинговые коммуникации в образовании
Маркетинговые коммуникации в образовании День гимназиста
День гимназиста Сравнение условий строительства автомобильных и железнодорожных магистралей в Финляндии и России
Сравнение условий строительства автомобильных и железнодорожных магистралей в Финляндии и России Организация ремонта колесных пар в локомотивном депо
Организация ремонта колесных пар в локомотивном депо Роль Д.А.Поспелова в отечественной кибернетике и искусственном интеллекте
Роль Д.А.Поспелова в отечественной кибернетике и искусственном интеллекте Гигиена и здоровье
Гигиена и здоровье Презентация Индийский океан
Презентация Индийский океан Презентация к классному часу по теме Отечественная война 1812 года
Презентация к классному часу по теме Отечественная война 1812 года Топливная промышленность России
Топливная промышленность России 24 мая – День славянской письменности и культуры
24 мая – День славянской письменности и культуры Религиозная организация христиан веры евангельской (пятидесятников), г. Ярославля
Религиозная организация христиан веры евангельской (пятидесятников), г. Ярославля Сравнение обыкновенных дробей
Сравнение обыкновенных дробей Презентация НОД Путешествие по русским народным сказкам
Презентация НОД Путешествие по русским народным сказкам Рынки. Рынок ценных бумаг. (Урок 11-12)
Рынки. Рынок ценных бумаг. (Урок 11-12) 9 Мая - День Победы (открытки учеников)
9 Мая - День Победы (открытки учеников) Урок внеклассного чтения В свои стихи я вкладываю душу
Урок внеклассного чтения В свои стихи я вкладываю душу Лента Мёбиуса
Лента Мёбиуса Сервисный тренинг EXD06 Экспертный тренинг
Сервисный тренинг EXD06 Экспертный тренинг Презентация сложение целых чисел
Презентация сложение целых чисел Взаимодействие лазерного излучения с веществом: спектроскопия и фазовое управление молекулярными колебаниями. Лекция 4
Взаимодействие лазерного излучения с веществом: спектроскопия и фазовое управление молекулярными колебаниями. Лекция 4