Содержание
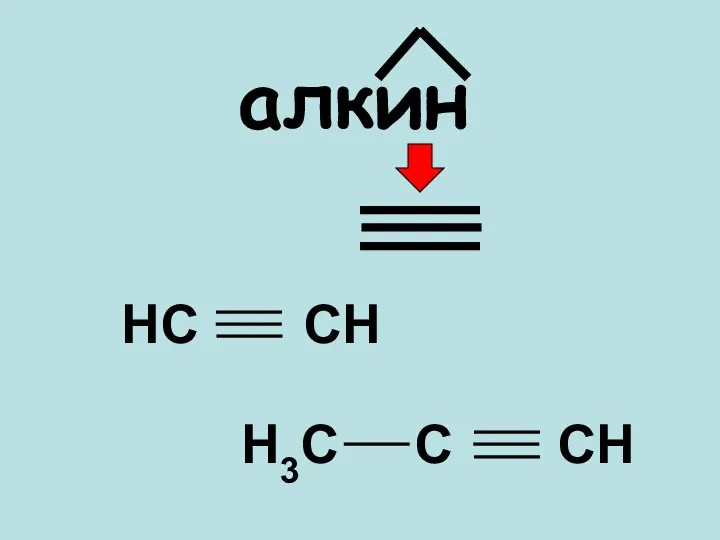
- 2. алкин НС СН Н3С С СН
- 3. Общая формула алкинов CnH2n-2
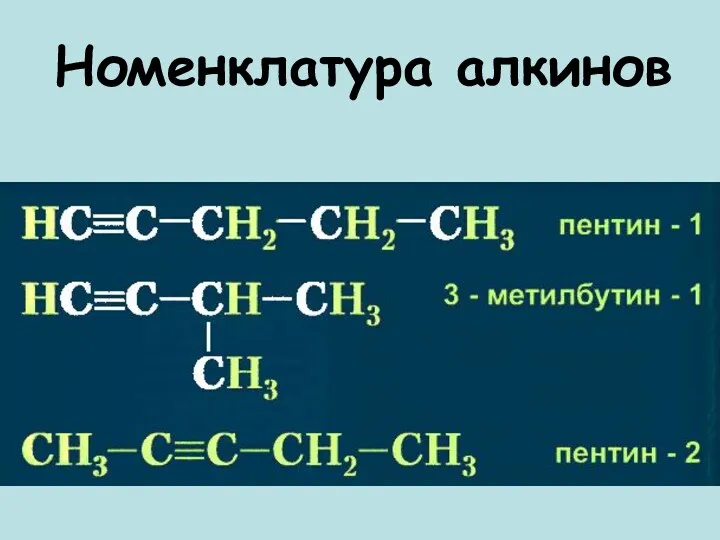
- 4. Номенклатура алкинов
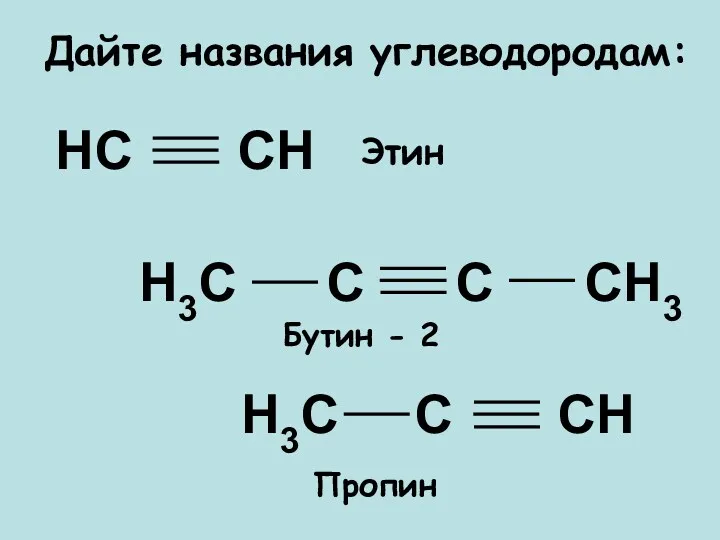
- 5. Дайте названия углеводородам: НС СН Н3С С СН Н3С С С СН3 Этин Бутин - 2
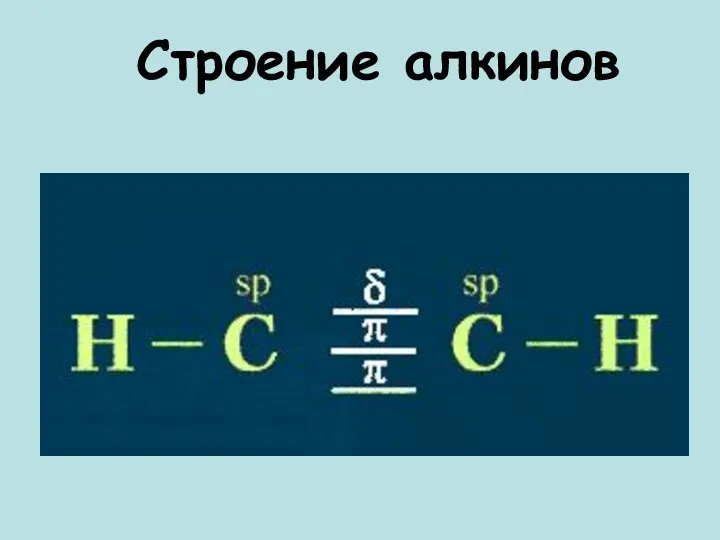
- 6. Строение алкинов
- 7. Получение алкинов 1. Карбидный способ (гидролиз карбида кальция): Основной недостаток – большие затраты электроэнергии на производство
- 8. 2. Термический крекинг метана.
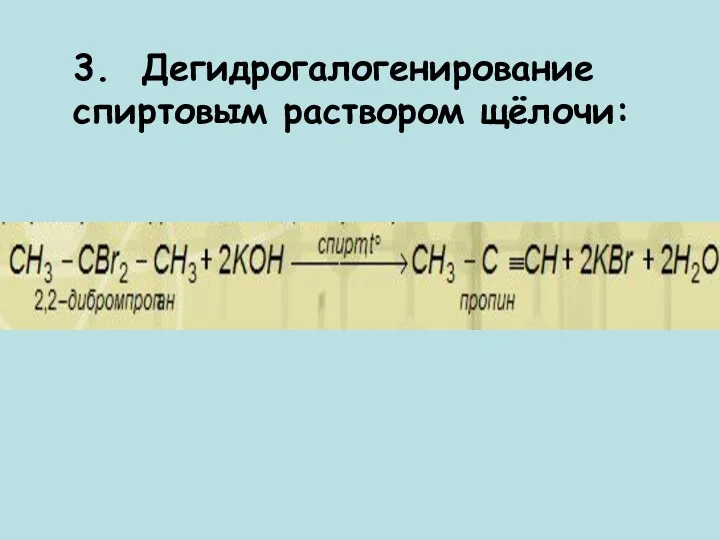
- 9. 3. Дегидрогалогенирование спиртовым раствором щёлочи:
- 10. Физические свойства алкинов
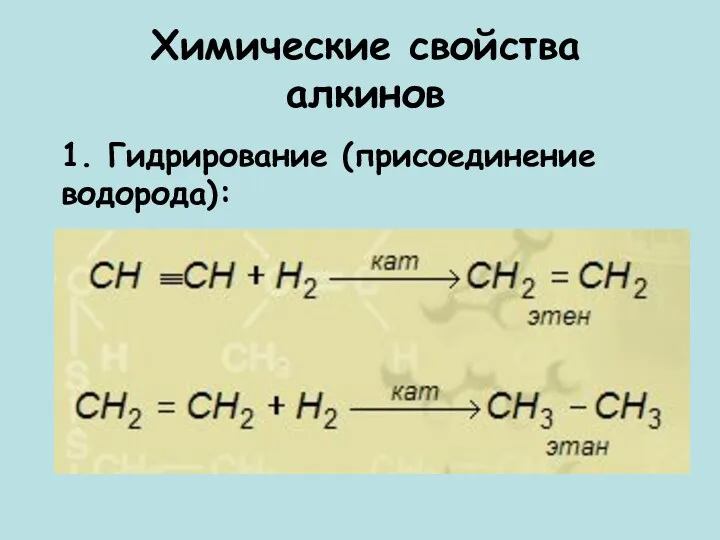
- 11. Химические свойства алкинов 1. Гидрирование (присоединение водорода):
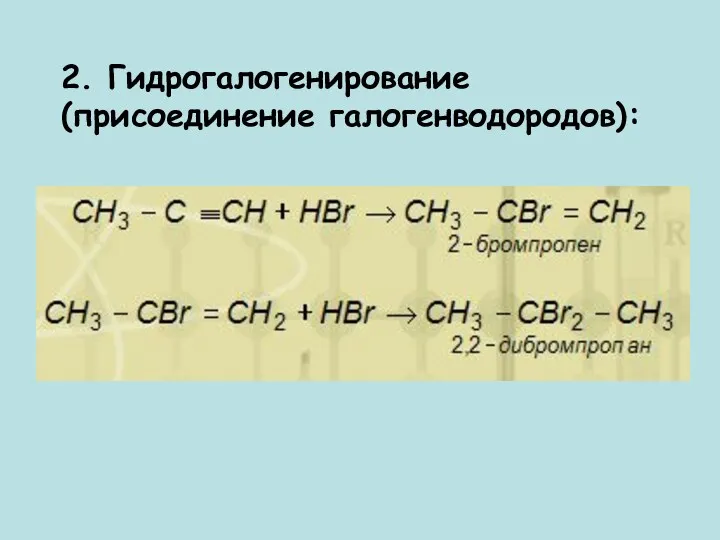
- 12. 2. Гидрогалогенирование (присоединение галогенводородов):
- 13. 3. Реакция полимеризации (тримеризации): Реакция Зелинского
- 14. 4. Реакция Кучерова (присоединение воды к ацетилену в присутствии солей ртути с образованием альдегида): этин уксусный
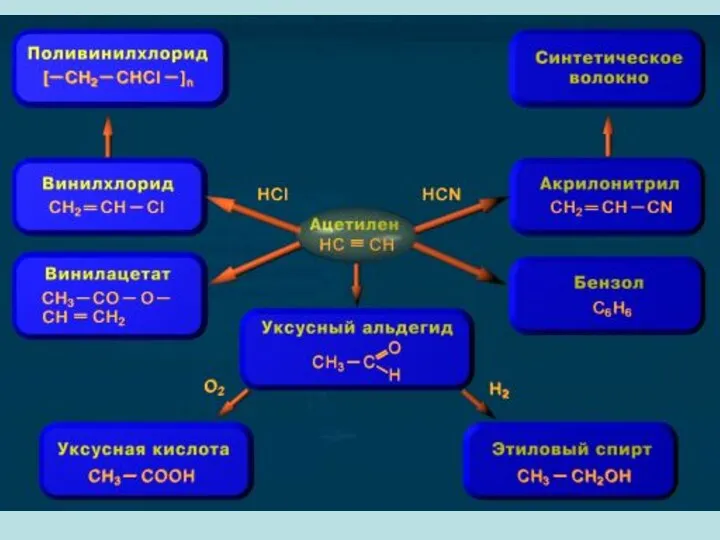
- 15. Применение алкинов
- 20. Выводы: Углеводороды с общей формулой СnH2n-2, в молекулах которых имеется одна тройная связь, называются алкинами. Наиболее
- 22. Скачать презентацию











 Патология гемостаза
Патология гемостаза Человек познает мир
Человек познает мир Развитие конфликтной компетентности подростков
Развитие конфликтной компетентности подростков Европа в XIX веке
Европа в XIX веке Утверждение авторитарных и тоталитарных режимов в Италии и Испании
Утверждение авторитарных и тоталитарных режимов в Италии и Испании Доноведение 4 класс Мой крайпрезентация
Доноведение 4 класс Мой крайпрезентация Grammar A2+articles
Grammar A2+articles Электрические станции и подстанции. Главные схемы распределительных устройств электростанций и подстанций. (Лекция 3)
Электрические станции и подстанции. Главные схемы распределительных устройств электростанций и подстанций. (Лекция 3) Самый умный. Игра
Самый умный. Игра Что означают английские надписи на одежде
Что означают английские надписи на одежде Урок труда Волшебные нитки, иголки и пуговицы
Урок труда Волшебные нитки, иголки и пуговицы 01 .НТД. ГФ
01 .НТД. ГФ Фотоальбом. Для Алексея
Фотоальбом. Для Алексея Деление с остатком
Деление с остатком Производство окиси этилена окислением этилена кислородом
Производство окиси этилена окислением этилена кислородом Охранно - пожарная сигнализация. Виды сигнализаций
Охранно - пожарная сигнализация. Виды сигнализаций Создание программы
Создание программы Аудирование как средство совершенствования лексического навыка
Аудирование как средство совершенствования лексического навыка Тренажёр Табличное умножение
Тренажёр Табличное умножение Мой любимый детский сад. Экскурсия в медицинский кабинет
Мой любимый детский сад. Экскурсия в медицинский кабинет Состав языка C#. Тема 2
Состав языка C#. Тема 2 Христианин в труде. 4 класс
Христианин в труде. 4 класс Михаил Юрьевич Лермонтов
Михаил Юрьевич Лермонтов Организация процесса приготовления и разработка ассортимента изделий из пряничного теста
Организация процесса приготовления и разработка ассортимента изделий из пряничного теста OECD_RU
OECD_RU Новогодний праздник Святки для 3-4 классов
Новогодний праздник Святки для 3-4 классов Светлая Пасха. История и традиции
Светлая Пасха. История и традиции Энергосбережение – умное потребление
Энергосбережение – умное потребление