Слайд 2

Слайд 3

Вода в природе
Физические свойства воды
Вода как растворитель
Химические свойства воды
Экологические проблемы
Слайд 4

Бесцветное вещество, без вкуса и запаха, плотность 1 г/см3, температура кипения
1000С , температура плавления (замерзания) – 00С.
Слайд 5

В отличие от большинства других веществ плотность воды в твёрдом состоянии
(льда) меньше, чем в жидком. Поэтому лёд плавает, что имеет огромное значение для жизни природы.
Слайд 6

Вода – единственное вещество в природе, которое в земных условиях существует
в трех агрегатных состояниях: жидком, газообразном и твёрдом.
Слайд 7

Слайд 8

Слайд 9

Слайд 10

Слайд 11

Вода – хороший растворитель. В ней растворяются твёрдые, жидкие и газообразные
вещества.
Слайд 12

Растворение перманганата калия (марганцовки).
Слайд 13

Растворённый кислород воздуха обеспечивает жизнь водных организмов.
Слайд 14

Не все вещества растворяются в воде. Например: глина, песок.
Слайд 15

...бензин, растительное масло.
Слайд 16

Химические свойства воды
Взаимодействие с металлами
Взаимодействие с кислотными оксидами
Взаимодействие с основными
оксидами
Взаимодействие с другими веществами
Слайд 17

Вода реагирует со многими металлами.
С наиболее активными образует щёлочи и
водород:
2Na +2Н2О = 2NаОН + Н2 (видео)
С металлами средней активности (при нагревании) образуется оксид металла и водород.
3Fe + 4H2O = Fe3O4 = 4H2
Слайд 18

Оксиды активных металлов (щелочных и щелочно-земельных) реагируют с водой с образованием
растворимых оснований (щелочей). Такие оксиды называют основными оксидами.
СаО + Н2О = Са(ОН)2
Na2О +Н2О = 2NаОН
Слайд 19

Оксиды неметаллов (кроме оксида кремния) реагируют с водой с образованием кислот.
Такие оксиды называют кислотными оксидами.
SО3 + Н2О = H2SO4
P2O5 +3Н2О = 2H3PO4
Слайд 20

Вода взаимодействует с некоторыми неметаллами:
С + 2Н2О = СО2 = 2Н2
С
солями, кислотами (образуя гидраты и кристаллогидраты):
CuSO4 +5H2O = CuSO4.5H2O (медный купорос)
С органическими веществами:
С2Н4 + Н2О = С2Н5ОН (получение этилового спирта из этилена)
Слайд 21

Вода используется в самых разных областях деятельности человека. Без воды нет
жизни. Поэтому важное значение имеет забота о чистоте природных вод.
Слайд 22

Слайд 23

Слайд 24

Слайд 25

Источниками загрязнения могут быть промышленные предприятия, транспорт, аварии…
Слайд 26

Слайд 27

Слайд 28

Слайд 29

Загрязнению водоёмов способствует нерациональное использование сельскохозяйственных угодий.




























 Имена героев в названиях улиц города Советска
Имена героев в названиях улиц города Советска Навесное оборудование для малогабиритной тяговой установки
Навесное оборудование для малогабиритной тяговой установки Сварочные выпрямители
Сварочные выпрямители Аналитический обзор современных швейных машин потайного стежка
Аналитический обзор современных швейных машин потайного стежка Удостоверение сделок. Доверенность. Завещание и его формы
Удостоверение сделок. Доверенность. Завещание и его формы Устройство карпового прудового рыбхоза
Устройство карпового прудового рыбхоза Класс Пресмыкающиеся
Класс Пресмыкающиеся Парк флоры и фауны Роев ручей
Парк флоры и фауны Роев ручей Поздравляем с Днём МАМ!
Поздравляем с Днём МАМ! Конкурс рисунков
Конкурс рисунков Призентация к общешкольному мероприятию 9 Мая- День Победы
Призентация к общешкольному мероприятию 9 Мая- День Победы Наладка технологического оборудования на производстве
Наладка технологического оборудования на производстве Желаемые объекты Чкаловского парка
Желаемые объекты Чкаловского парка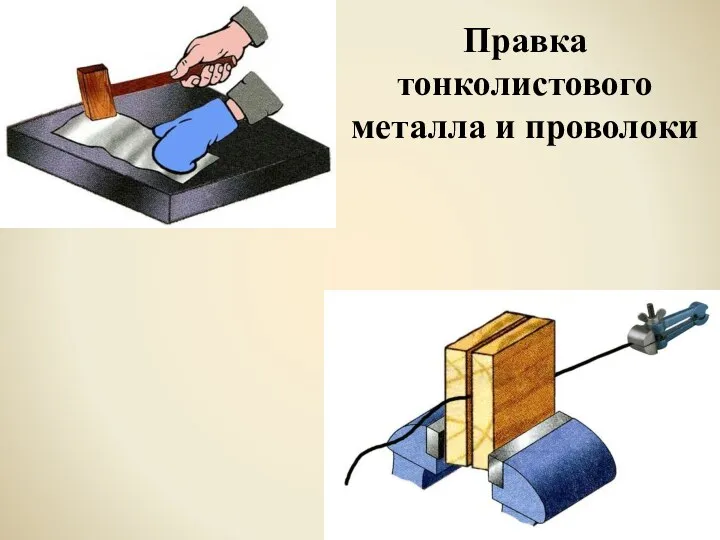 Правка тонколистового металла и проволоки. Проверь свои знания
Правка тонколистового металла и проволоки. Проверь свои знания ВЛИЯНИЕ УСТНОГО НАРОДНОГО ТВОРЧЕСТВА НА РАЗВИТИЕ РЕЧИ ДЕТЕЙ 3 – 4 ЛЕТ.
ВЛИЯНИЕ УСТНОГО НАРОДНОГО ТВОРЧЕСТВА НА РАЗВИТИЕ РЕЧИ ДЕТЕЙ 3 – 4 ЛЕТ. Логопедическое занятие для учащихся 3 класса (развитие связной речи) . Тема Плохо (по В. Осеевой)
Логопедическое занятие для учащихся 3 класса (развитие связной речи) . Тема Плохо (по В. Осеевой) Блокада Ленинграда
Блокада Ленинграда Проблемы корейского общества сквозь призму современной художественной литературы
Проблемы корейского общества сквозь призму современной художественной литературы Презентация Православие и язычество на Руси.
Презентация Православие и язычество на Руси. Презентация Нижний Новгород
Презентация Нижний Новгород презентация Посуда
презентация Посуда Презентация кружка Волшебные краски часть 1
Презентация кружка Волшебные краски часть 1 Эмбриогенез человека
Эмбриогенез человека Смутное время
Смутное время Реализация комплекса ГТО на территории Семикаракорского района
Реализация комплекса ГТО на территории Семикаракорского района Криминалистика как юридическая дисциплина
Криминалистика как юридическая дисциплина Розвиток мовлення 4 клас ІІ семестр
Розвиток мовлення 4 клас ІІ семестр Международные отношения, мировая политика, внешняя политика и дипломатия в контексте новой научной парадигмы
Международные отношения, мировая политика, внешняя политика и дипломатия в контексте новой научной парадигмы