Содержание
- 2. Иммунитет Иммунитет — способ защиты организма от живых тел и веществ, несущих на себе признаки генетической
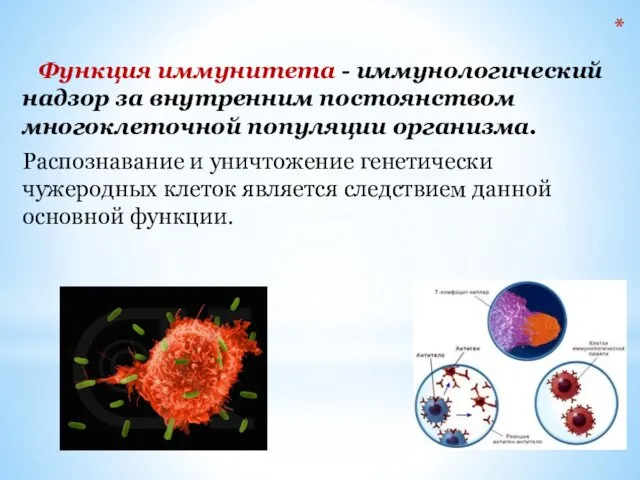
- 3. Функция иммунитета - иммунологический надзор за внутренним постоянством многоклеточной популяции организма. Распознавание и уничтожение генетически чужеродных
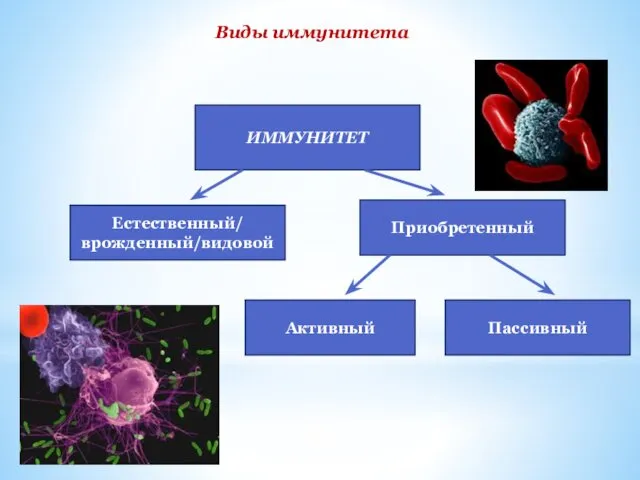
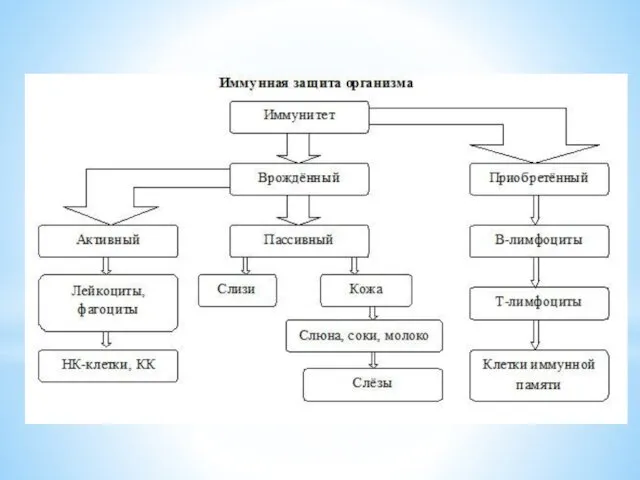
- 4. Виды иммунитета ИММУНИТЕТ Естественный/ врожденный/видовой Приобретенный Активный Пассивный
- 6. Естественный, или врожденный (видовой), иммунитет представляет собой невосприимчивость одного вида животных или человека к микроорганизмам, вызывающим
- 7. Приобретенным иммунитетом называют такую невосприимчивость организма к инфекционным агентам, которая формируется в процессе его жизнедеятельности и
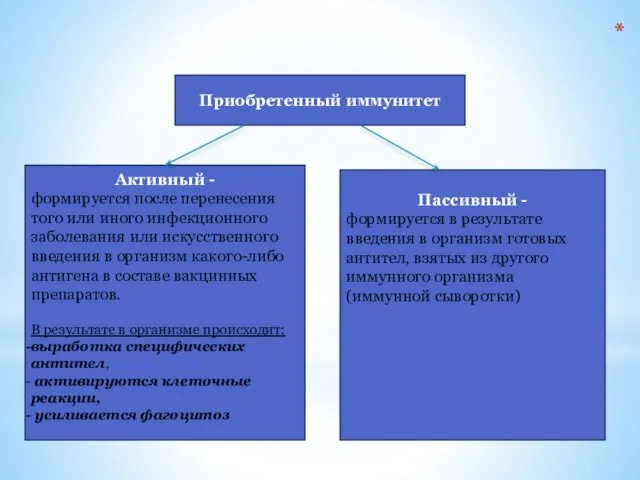
- 8. Приобретенный иммунитет Активный - формируется после перенесения того или иного инфекционного заболевания или искусственного введения в
- 9. Плацентарный иммунитет — передача антител плоду через плаценту или ребенку с материнским молоком. Антимикробный (инфекционный) приобретенный
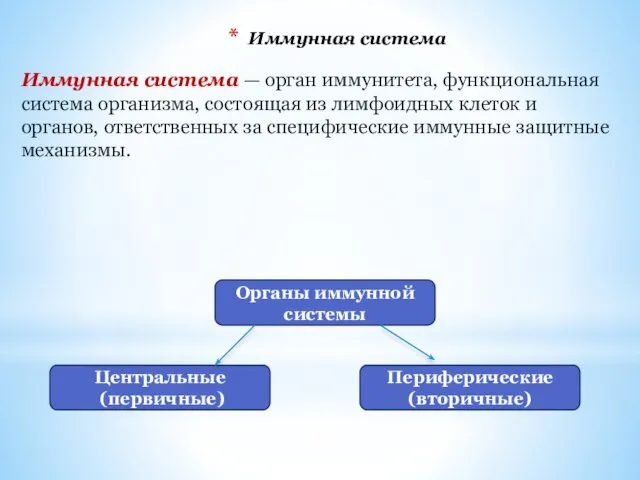
- 10. Иммунная система Иммунная система — орган иммунитета, функциональная система организма, состоящая из лимфоидных клеток и органов,
- 11. Иммунная система Центральные органы иммунитета являются местами дифференцировки лимфоцитов: - вилочковая железа; - сумка Фабрициуса (только
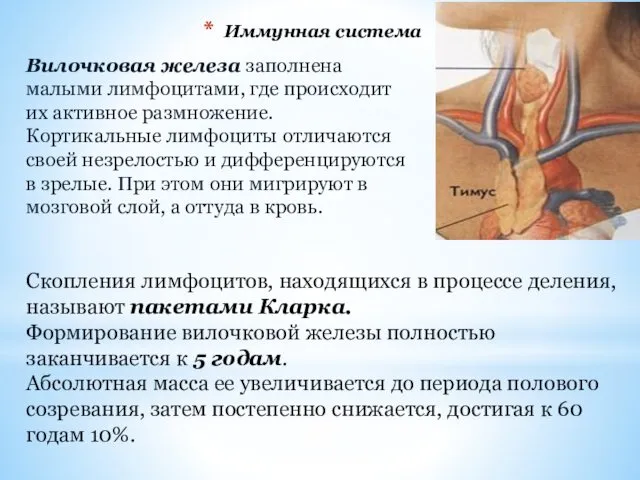
- 12. Иммунная система Вилочковая железа заполнена малыми лимфоцитами, где происходит их активное размножение. Кортикальные лимфоциты отличаются своей
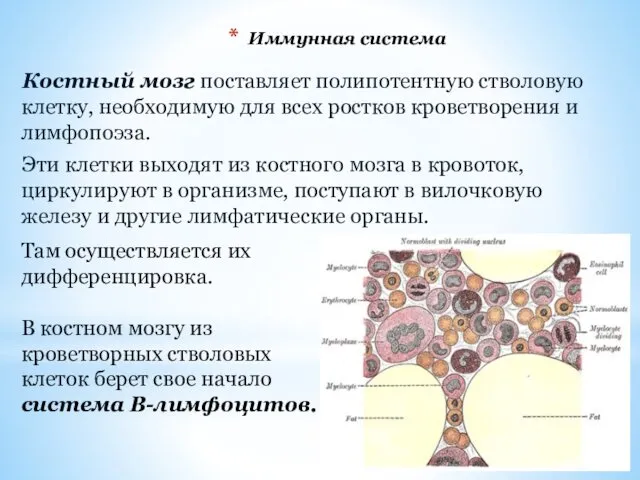
- 13. Иммунная система Костный мозг поставляет полипотентную стволовую клетку, необходимую для всех ростков кроветворения и лимфопоэза. Эти
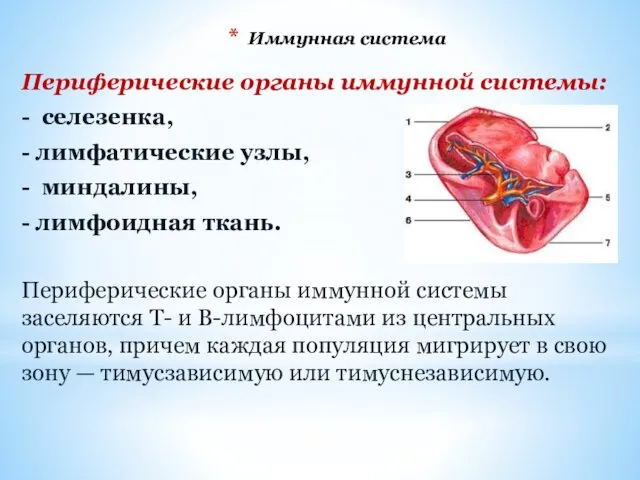
- 14. Иммунная система Периферические органы иммунной системы: - селезенка, - лимфатические узлы, - миндалины, - лимфоидная ткань.
- 15. Иммунная система Селезенка: - осуществляет контроль за клеточным составом крови; - удаляет из кровотока утратившие функциональную
- 16. Иммунная система В лимфатическом узле кортикальная зона заполнена В-лимфоцитами. Скопления Т-клеток находятся в паракортикальной области .
- 17. Иммунная система Лимфоидная ткань, диффузно распределена в слизистых покровах организма - самый первый барьер на пути
- 18. Иммунная система Лимфоидная ткань, ассоциированная со слизистыми оболочками, имеет также особую защитную секреторную систему. Взаимодействие между
- 19. Клетки иммунной системы 2 типа иммунных механизма Клеточные реакции обеспечивают защиту организма от внутриклеточных и грибковых
- 20. Система гуморального иммунитета. СГИ- это специализированная система, главной функцией которого является синтез антител против антигенов. Функциональная
- 21. В периферической крови содержится не более 20-30% В-лимфоцитов. В основном, это не зрелые клетки, прошедшие первые
- 22. Каждый организм обладает громадным набором В-лимфоцитов, несущих иммуноглобулиновые рецепторы самой разнообразной специфичности, что дает возможность синтезировать
- 23. Основные этапы дифференцировки В-лимфоцитов -полипотентная стволовая клетка -лимфойдная стволовая клетка -предшественник В-лимфоцитов(nВ) -В0-лимфоциты -В1-лимфоциты -В2-лимфоциты Этап
- 24. Иммуноглобулины На стадии В2 в результате антигензависимой дифференцировки внутри каждого клона В-лимфоцитов, реагирующий на данный антиген,
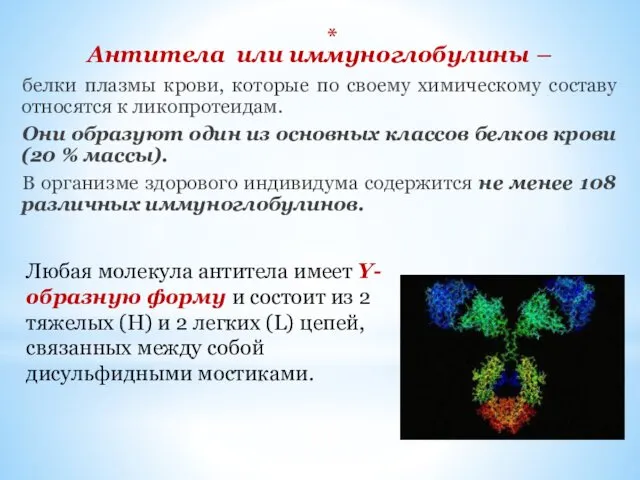
- 25. Антитела или иммуноглобулины – белки плазмы крови, которые по своему химическому составу относятся к ликопротеидам. Они
- 26. IgG (Иммуноглобулин G) IgG вырабатываются как при первичном , так и при вторичном иммунном ответе .
- 27. IgA (Иммуноглобулин A) Иммуноглобулин A содержится преимущественно в выделениях слизистых оболочек - в слюне, слезной жидкости,
- 28. IgE (Иммуноглобулин E) Основная физиологическая функция IgE, очевидно, защита внешних слизистых оболочек организма путем локальной активации
- 29. IgM (Иммуноглобулин M) IgM вырабатываются при первичном иммунном ответе . IgM эффективно связывают комплемент и активируют
- 30. Система клеточного иммунитета СКИ включает тимус-место дифференцировки костномозговых предшественников Т-лимфоцитов(nT) до потенциально зрелых форм; периферические органы
- 31. Основные функции Т-системы иммунитета. 1) Главная функция Т-системы связана с обеспечением клеточной формы иммунного ответа: Т-лимфоциты
- 32. Дифференцировка Т-лимфоцитов Антигеннезависимая дифференцировка: Предшественники Т-лимфоцитов(nT), образовавшиеся в костном мозге, мигрируют в тимус и залегают его
- 33. Положительная селекция Взаимодействие nT со стромой субкапсулярной зоны приводит к экспрессии первого специфического маркера Т-клеток-белка CD2.
- 34. Отрицательная селекция В кортико-медулярной зоне и в мезенхиме тимуса образовавшиеся CD4 и CD8 Т-лимфоциты, еще недостаточно
- 35. Дифференцировка Т-лимфоцитов Антигензависимая дифференцировка Т-лимфоциты покидают тимус и с током крови мигрируют в периферические органы иммунной
- 36. Нейроэндокринная регуляция иммунного ответа
- 37. Нейроэндокринная регуляция иммунного ответа В целостном организме работа иммунной системы коррегируется мозгом. К структурам мозга, модулирующим
- 38. Пути и механизмы регуляции иммунного ответа. Гормональные, нервные и нервнопептидные пути относят к основным способам передачи
- 39. Симпатический отдел вегетативной нервной системы и регуляция иммунного ответа. Можно полагать, что, несмотря на отсутствие подробных
- 40. Парасимпатический отдел вегетативной нервной системы и регуляция иммунного ответа. Как в строме, так и в паренхеме
- 41. Регуляция иммунного ответа адренокортикотропным гормоном. АКТГ оказывает влияние на функцию, по крайней мере, трех типов иммунокомпетентных
- 42. Регуляция иммунного ответа тиротропином. ТТГ является одним из первых гормонов гипофиза, иммуннорегуляторные свойства которого были хорошо
- 43. Регуляция иммунного ответа соматотропином. СТГ, продуцируемый гипофизом, является следующим после тиротропина гормоном, иммуннорегуляторные свойства которого хорошо
- 44. Регуляция иммунного ответа веществом p и соматостатином Пептиды периферической нервной системы вещество p и соматостатин, принимают
- 45. Регуляция иммунного ответа опиоидными пептидами. Биологические эффекты опиоидов на иммунную систему строго дозозависимы, при различных дозах
- 46. Гормональная регуляция иммунного ответа. Как свидетельствуют современные данные, практически все популяции клеток, участвующих в иммунных реакциях,
- 47. Глюкокортикоидные гормоны и иммунологические процессы. Большие фармакологические дозы глюкокортикоидных гормонов, особенно при длительном их применении, вызывают
- 48. Гормоны половых желез и функции иммунной системы. Гормоны репродуктивной системы способны влиять на иммунологические функции. Это
- 49. Гормоны щитовидной железы и паращитовидной желез и иммунологические процессы. Гормоны щитовидной железы тироксин и трийодтиронин при
- 51. Скачать презентацию







































 Транспортное право
Транспортное право Ярослав Мудрый и Русская Правда
Ярослав Мудрый и Русская Правда Презентация программы старшей группы МДОУ, ориентированная на родителей, с учетом регионального компонента.
Презентация программы старшей группы МДОУ, ориентированная на родителей, с учетом регионального компонента. Презентация юбилея школы Диск Диск Диск Диск
Презентация юбилея школы Диск Диск Диск Диск Основы учебной деятельности, Преобразование учебного текста в табличную форму
Основы учебной деятельности, Преобразование учебного текста в табличную форму Эластичность спроса
Эластичность спроса Философия человека, общества и истории
Философия человека, общества и истории Книр: Процессы внепечной металлургии стали
Книр: Процессы внепечной металлургии стали Вступ до комп’ютерної техники
Вступ до комп’ютерної техники Пожелания к 8 марта
Пожелания к 8 марта Білім алушыларды қорытынды аттестаттау презентация
Білім алушыларды қорытынды аттестаттау презентация Основні поняття загальної теорії держави та права
Основні поняття загальної теорії держави та права Антенна для Wi-Fi систем
Антенна для Wi-Fi систем Из военной энциклопедии Диск
Из военной энциклопедии Диск Автоматизация звука Л в словах и предложениях.
Автоматизация звука Л в словах и предложениях. Орган - духовой клавишный музыкальный инструмент
Орган - духовой клавишный музыкальный инструмент Презентация Оформление новогоднего интерьера
Презентация Оформление новогоднего интерьера Как работает наш организм Диск
Как работает наш организм Диск Основы проводной связи. Телефонная связь. Звуковые колебания. Коммутируемые сети
Основы проводной связи. Телефонная связь. Звуковые колебания. Коммутируемые сети Алгоритм составления социального проекта
Алгоритм составления социального проекта Приемы компрессии (сжатия) на примере текста Как раньше взрослели
Приемы компрессии (сжатия) на примере текста Как раньше взрослели Духовно-нравственное воспитание в ДОУ
Духовно-нравственное воспитание в ДОУ Синтоизм
Синтоизм Михаил Юрьевич Лермонтов. Бородино
Михаил Юрьевич Лермонтов. Бородино Водоэмульсионые краски
Водоэмульсионые краски Стандарты высшего профессионального образования
Стандарты высшего профессионального образования Psychophysik Hören
Psychophysik Hören Наследственные заболевания и синдромы с аномалиями размеров и формы зубов
Наследственные заболевания и синдромы с аномалиями размеров и формы зубов