Слайд 2

ПРАВИЛО ВАНТ-ГОФФА
При увеличении температуры на 10 градусов скорость реакции возрастает
в 2-4 раза.
Слайд 3

Слайд 4

ТЕОРИЯ АРРЕНИУСА.
ЭНЕРГИЯ АКТИВАЦИИ РЕАКЦИИ
Основные модельные представления теории:
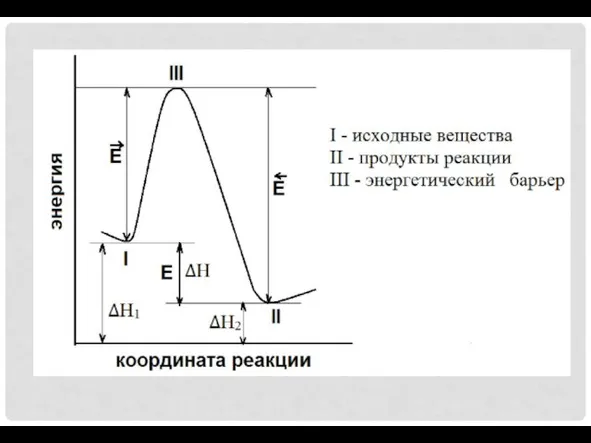
В реакцию способны вступать лишь
те частицы реагентов, которые обладают некоторой избыточной энергией, позволяющей им преодолеть энергетический барьер.
Минимально необходимый запас энергии называют энергией активации.
Слайд 5

Энергию активации (Е) можно трактовать как избыток энергии по сравнению со
средней энергией молекул при данной температуре, которой должны обладать молекулы, чтобы они могли вступить в химическую реакцию.
Источники получения избыточной энергии:
термическая активация;
действие различных излучений (свет, ультразвук, радиация);
действие быстрых частиц (радикалов).
Слайд 6
Слайд 7

Слайд 8
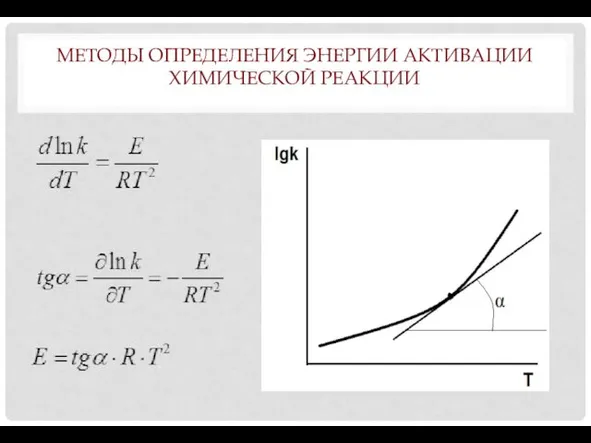
МЕТОДЫ ОПРЕДЕЛЕНИЯ ЭНЕРГИИ АКТИВАЦИИ
ХИМИЧЕСКОЙ РЕАКЦИИ
Слайд 9

Слайд 10

Слайд 11










 Инновационный олыт
Инновационный олыт Нанотехнології наноматеріалу
Нанотехнології наноматеріалу Колониальная политика европейских государств и США
Колониальная политика европейских государств и США Особенности оценивания экспериментальных заданий в ОГЭ – 9 кл по физике
Особенности оценивания экспериментальных заданий в ОГЭ – 9 кл по физике Аргументация и доказательство
Аргументация и доказательство Тема 1.6.2
Тема 1.6.2 Устюженский кедровник - гордость Вологодчины
Устюженский кедровник - гордость Вологодчины Имидж делового мужчины
Имидж делового мужчины Храмы Крыма и их история
Храмы Крыма и их история Новые логопедические технологии в работе с учащимися на школьном логопункте
Новые логопедические технологии в работе с учащимися на школьном логопункте Презентация Масленица.
Презентация Масленица. Методы нанесения лакокрасочных материалов Технологический процесс получения системы ЛКП. (Лекция 4)
Методы нанесения лакокрасочных материалов Технологический процесс получения системы ЛКП. (Лекция 4) ФГОС ДО. Особенности построения образовательного процесса
ФГОС ДО. Особенности построения образовательного процесса Аварийно химические опасные вещества - АХОВ
Аварийно химические опасные вещества - АХОВ Возникновение дизайна в России. Русский модерн. Поиски стиля
Возникновение дизайна в России. Русский модерн. Поиски стиля Текстильные волокна. 7 класс
Текстильные волокна. 7 класс Социальный контракт
Социальный контракт Системы кондиционирования и вентиляции Аэрация
Системы кондиционирования и вентиляции Аэрация Презентация к уроку по теме Основания 8 класс
Презентация к уроку по теме Основания 8 класс Көпіртәрізді протездер дайындағанда жіберілетін қателіктер мен асқынулар, оларды жою
Көпіртәрізді протездер дайындағанда жіберілетін қателіктер мен асқынулар, оларды жою Организация НОД по развитию речи и художественной литературе через метод наглядного моделирования
Организация НОД по развитию речи и художественной литературе через метод наглядного моделирования История японского производителя автомобилей Mitsubishi
История японского производителя автомобилей Mitsubishi ТРЕНАЖЕРНО- ИНФОРМАЦИОННАЯ СИСТЕМА ТИСА В ШКОЛЬНОЙ ПРОГРАММЕ НА УРОКАХ ЛФК
ТРЕНАЖЕРНО- ИНФОРМАЦИОННАЯ СИСТЕМА ТИСА В ШКОЛЬНОЙ ПРОГРАММЕ НА УРОКАХ ЛФК Презентация проекта Формирование и развитие социально значимых ценностей, гражданственности и патриотизма у детей дошкольного возраста.
Презентация проекта Формирование и развитие социально значимых ценностей, гражданственности и патриотизма у детей дошкольного возраста. Образ женщины-матери – идеал женской красоты
Образ женщины-матери – идеал женской красоты Развитие речи детей-билингвов на логопедических занятиях с использованием предметно-практической деятельности
Развитие речи детей-билингвов на логопедических занятиях с использованием предметно-практической деятельности В поисках своей профессии: мой выбор
В поисках своей профессии: мой выбор Отделка изделия из тонколистового металла, проволоки, пластмассы
Отделка изделия из тонколистового металла, проволоки, пластмассы